微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 [化学--物质的结构与性质]
砷化镓属于第三代半导体,它能直接将电能转变为光能,砷化镓灯泡寿命是普通灯泡的100倍,而耗能只有其10%,推广砷化镓等发光二极管(LED)照明,是节能减排的有效举措,已知砷化镓的晶胞结构如图.试回答下列问题
(1)下列说法正确的是______(选填序号).
A.砷化镓晶胞结构与NaCl相同
B.第一电离能:As>Ga
C.电负性:As>Ga
D.砷和镓都属于p区元素
E.半导体GaP、SiC与砷化镓为等电子体
(2)砷化镓是将(CH3)3Ga和AsH3用MOCVD方法制备得到,该反应在700℃进行,反应的方程式为:______.
AsH3空间形状为:______(CH3)3Ga中镓原子杂化方式为:______.
(3)Ga的核外电子排布式为:______.
(4)AsH3沸点比NH3低,其原因是:______.
参考答案:(1)A.GaAs晶体中As分布于晶胞体心,Ga分布于顶点和面心,而NaCl中阴阳离子分别位于晶胞的顶点、面心以及棱和体心,二者结构不同,故A错误;
B.同周期元素从左到右第一电离能逐渐增大,则第一电离能:As>Ga,故B正确;
C.同周期元素从左到右电负性逐渐增大,则电负性:As>Ga,故C正确;
D.砷和镓的价层电子都为sp电子,位于周期表p区,故D正确;
E.GaP的价层电子为3+5=8,SiC的价层电子为4+4=8,GaAs价层电子数为3+5=8,则为等电子体,故E正确;
故答案为:BCDE;
(2)反应为(CH3)3Ga和AsH3,生成为GaAs,根据质量守恒可知还应有和CH4,反应的化学方程式为:(CH3)3Ga+AsH3700℃
本题解析:
本题难度:一般
2、选择题 某原子核外共有6个电子,分布在K与L电子层上,其基态原子在L层分布中正确的是( )
A.

B.
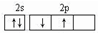
C.

D.

参考答案:D
本题解析:
本题难度:简单
3、选择题 某主族元素的原子的最外层电子数是次外层的a倍(a>1),则该原子核内质子数是( )
A.2a
B.a+2
C.2a+10
D.2a+2
参考答案:D
本题解析:
本题难度:简单
4、选择题 下列说法中正确的是
[? ]
A.处于最低能量的原子叫做基态原子
B.3p2表示3p能级有两个轨道
C.同一原子中,1s、2s、3s电子的能量逐渐减小
D.同一原子中,2p、3p、4p能级的轨道数依次增多
参考答案:A
本题解析:
本题难度:简单
5、填空题 (1)
O2-中的质子数是______,中子数是______,核外电子数是______,质量数是______,画出此微粒的离子结构示意图:______
(2)写出下列元素的电子排布式
A题:
某原子3p轨道上得到1个电子后不能再容纳外来电子,其基态原子的电子排布式为:______
某元素的正三价离子的3d轨道为半充满,其基态原子的电子排布式为:______
B题:
Mg:______K:______Cr:______(以原子实表示法表示).
(3)画出下列元素的轨道表示式:C:______N:______.
参考答案:(1)?188O2-中的质子数是8,质量数是18,;质子数+中子数=质量数,所以其中子数为10,阴离子的电子数=质子数+电荷数.所以其电子数为10,离子结构示意图为:
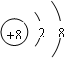
,故答案为:8;8;10;
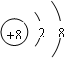
;
(2)A题:根据核外电子排布规律,该基态原子的电子排布式为:1s22s22p63s23p5,故答案为:1s22s22p63s23p5;
元素的正三价离子的3d轨道为半充满,其基态原子的电子排布式为:1s22s22p63s23p63d64s2,为Fe,故答案为:1s22s22p63s23p63d64s2;
B题:Mg用原子实表示为:[Ne]3s2,K用原子实表示为:[Ar]4s1,Cr用原子实表示为:[Ar]3d54s1,故答案为:[Ne]3s2;[Ar]4s1;[Ar]3d54s1.
(3)C原子基态时的电子排布式为1s22s22p2,其电子的轨道表示式为:
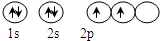
;
N原子基态时的电子排布式为1s22s22p3,其电子的轨道表示式为:
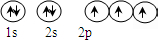
,
故答案为:

;

.
本题解析:
本题难度:一般