微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (12分)下图所示为某化学兴趣小组设计的乙醇氧化的实验装置(图中加热仪器、铁架台、铁夹等均未画出)。
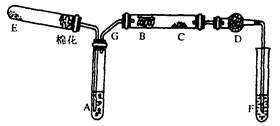
图中:A为无水乙醇(沸点为78℃),B为绕成螺旋状的细铜丝,C为无水CuSO4粉末,D为碱石灰,F为新制的碱性Cu(OH)2悬浊液。
(1) E处是一种纯净物,其发生反应的化学方程式为___? _____。
(2)为使A中乙醇平稳汽化成乙醇蒸气,常采用的方法是_______? ______。
D处使用碱石灰的作用是__? _____。?
(3)能证明乙醇反应后产物的实验现象是?
?。
(4)本实验中若不加热E处,其他操作不变,则发现C处无明显变化,而F处现象与(3)相同。推断B处发生反应的化学方程式____?。
参考答案:(12分) (1)2KMnO4? K2MnO4+MnO2+O2↑(2分)
(2)水浴加热试管A,(2分)防止F试管中的水蒸汽进入到C,干扰生成物水的检验。(2分)
(3)无水硫酸铜变蓝色,说明有水生成,(2分)
加热煮沸F试管,产生砖红色的沉淀,说明有乙醛生成。(2分)
(4) CH3CH2OH? CH3CHO+H2?(2分)
本题解析:略
本题难度:一般
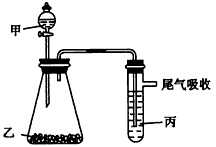
2、选择题 用下图所示装置进行实验,下表中实验结果能说明结论的是
[? ]
甲?
乙
丙
结论
A.
水?
电石
溴水
稳定性:水> C2H2> Br2
B.
盐酸?
石灰石
苯酚钠溶液
酸性:HCl> H2CO3>苯酚
C.
盐酸?
FeS
?溴水
还原性:S2- >Br- >Cl-
D.
浓盐酸?
KMnO4
KBr溶液
氧化性:KMnO4< Cl2< Br2
参考答案:B
本题解析:
本题难度:一般
3、实验题 某研究性学习小组研究HNO3的氧化性,设计了如下实验:
在盛有新制FeSO4溶液的试管中滴入2滴KSCN溶液,观察现象,然后再滴入几滴浓HNO3,溶液的颜色变红,但是将红色溶液放置一会儿则发现溶液由红色快速变为蓝色,并产生红棕色气体,这一奇特现象激起了同学的好奇心与求知欲望,对此现象设计了探究性实验。
⑴甲同学认为是溶液中的Fe2+的干扰造成的,大家经过理性分析,认为可以排除Fe2+的干扰,理由是?。
⑵乙同学认为红色消失,说明Fe(SCN)3被破坏,红棕色NO2说明了某些离子与HNO3发生了氧化还原反应,推测可能是KSCN与HNO3作用。KSCN溶液是一种无色液体,根据C、S、N的原子结构和共价键的相关知识推测SCN-的结构式为?。
⑶根据乙同学的观点,设计了实验方案1,往浓HNO3中逐滴加入KSCN溶液,实验开始时无明显现象,一段时间后溶液慢慢变红色至深红色,突然剧烈反应产生大量气泡,放出红棕色气体,而溶液红色消失变为浅绿色,溶液温度升高;继续滴入KSCN,溶液变为浅蓝色,最后变成无色。将产生的气体通入过量的Ba(OH)2溶液,产生浑浊,并剩余一种非极性气体;向反应后的溶液中加入BaCl2溶液产生白色沉淀,写出向浓HNO3中滴入KSCN的离子方程式
??
⑷丙同学认为SCN-的性质还可进一步探究,设计了方案2,向Fe(SCN)3中分别滴加过量的氯水、溴水,溶液的红色均消失变为黄色,而加入碘水时溶液的颜色基本不变。丙同学的设计意图是?__??
⑸通过本次探究,可以得出以下结论,a、用SCN-间接检验Fe2+时应注意?;b、与SCN-反应使溶液变红的?是Fe3+。(填“一定”或“不一定”)
参考答案:(12分)⑴如果是亚铁离子干扰,不可能变红之后,一段时间之后变成蓝色?
⑵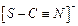 ?
?
⑶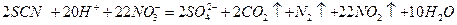
⑷比较硫氰根离子与氯离子、溴离子、碘离子的还原性强弱?
⑸a、加入氧化剂如氯气等必须少量? ? b、不一定
本题解析:略
本题难度:简单
4、实验题 某校实验小组进行实验研究(实验装置示意图如下)。
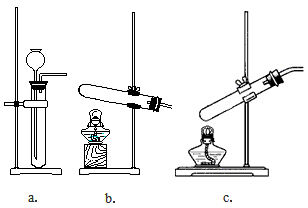
(1)制取氧气可选用的发生装置是_________(填字母序号)。该小组用制取的氧气进行硫在氧气中燃烧的性质实验时,在集气瓶底加入了少量氢氧化钠溶液。盛放该溶液的目的是__________________。
(2)①该小组用装置b制得NH3。其反应的化学方程式为__________________。
②该小组用装置b进行铁和水蒸气的反应,其化学方程式为__________________。
(3)该小组用装置c可进行的实验有__________________(写出一个即可)。
参考答案:(1)a、b;充分吸收生成的二氧化硫,减少污染空气(2)①2NH4Cl + Ca(OH)2 CaCl2 + 2H2O + 2NH3↑;②3Fe +4H2O
CaCl2 + 2H2O + 2NH3↑;②3Fe +4H2O Fe3O4 + 4H2(3)浓硫酸和铜反应
Fe3O4 + 4H2(3)浓硫酸和铜反应
本题解析:
本题难度:一般
5、实验题 酸碱中和滴定常用于测定酸碱溶液的浓度。
(1)实践中,在正式测定前,常常用已知浓度的酸(或碱)滴定已知浓度的碱(或酸),测定滴定曲线,然后选择合适的指示剂指示滴定终点,以保证数据的准确性。如:用0.100 0 mol/L NaOH溶液滴定20.00 mL 0.100 0 mol/L醋酸(CH3COOH) 溶液,有关数据记录如下表:
V/(NaOH)/mL
| 0.00
| 10.00
| 18.00
| 19.80
| 19.98
| 20.00
| 20.02
| 20.20
| 22.00
| 40.00
|
溶液pH
| 2.87
| 4.74
| 5.70
| 6.74
| 7.74
| 8.72
| 9.70
| 10.70
| 11.70
| 12.50
|
①根据上表数据绘制0.100 0 mol/L NaOH溶液滴定20.00 mL 0.100 0 mol/L醋酸(HAc)溶液的滴定曲线。
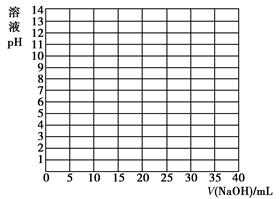
②根据你所绘制的曲线,确定pH的突变范围是________。
③下列指示剂中适合于本实验的是________。(填序号)
A.甲基橙 ? B.石蕊 ? C.酚酞
判断到达滴定终点的实验现象?
(2)滴定过程中,眼睛应重点观察_?_。
参考答案:①略
②7.74~9.70 ③C 无色变为浅红色,且半分钟内颜色不再发生变化?
(2)锥形瓶内溶液颜色的变化
本题解析:略
本题难度:简单