微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电。其电池反应为:2CH3OH+3O2+4OH-  ?2CO32-+6H2O,则下列说法正确的是?
?2CO32-+6H2O,则下列说法正确的是?
[? ]
A.构成该电池的正极和负极必须是两种活性不同的金属
B.充电时有CH3OH生成的电极为阳极
C.放电时电解质溶液的pH逐渐增大
D.放电时负极的电极反应为:CH3OH-6e-+8OH-=CO32-+6H2O
E.充电时每生成1 mol CH3OH转移12mol电子
参考答案:D
本题解析:
本题难度:一般
2、填空题 (15分)在下图中,E和F分别为电源两极;甲烧杯中盛有100 mL 0.2mol・L-1 AgNO3溶液,乙烧杯中盛有100 mL 0.15 mol・L-1 CuCl2溶液,A、B、C、D均为石墨电极,如果电解一段时间后,发现B极增重1.08g,则
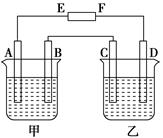
(1)E为________极,C为________极。
(2)A极的电极反应式为_________________________,析出气体________mL。(标准状况)
(3)若乙烧杯溶液体积不变,则此时溶液的物质的量浓度将变为 mol・L-1。
(4)甲烧杯中滴入石蕊试液,________极附近变红(填A或B);如果继续电解,在甲烧杯中最终得到________溶液(填溶质的化学式)。
参考答案:(15分)(1)正 阳 (各2分)
(2)4OH--4e-===2H2O+O2↑(3分) 56(2分)
(3)0.1 (2分)
(4)A HNO3(各2分)
本题解析:(1)甲烧杯中B极增重,说明B极有Ag析出,则B是阴极,所以A是阳极,E是电源的正极,F是电源的负极,D是电解池的阴极,C是电解池的阳极;
(2)甲烧杯是电解硝酸银溶液,所以A极是氢氧根离子放电生成氧气,电极反应式为4OH--4e-===2H2O+O2↑;B极增重1.08g,说明析出Ag的物质的量是0.01mol,转移电子的物质的量是0.01mol,则产生的氧气的物质的量是0.01mol/4=0.0025mol,标准状况下的体积是0.0025mol×22.4L/mol=0.056L=56mL;
(3)乙烧杯是氯化铜溶液,电解氯化铜溶液,阳极的产物是氯气,阴极 的产物是Cu,当有0.01mol电子通过时电解CuCl2的物质的量是0.01mol/2=0.005mol,原来溶液中CuCl2的物质的量是0.1L×0.15 mol・L-1=0.015mol,则溶液中还剩余CuCl2的物质的量是0.015-0.005=0.01mol,所以此时溶液的物质的量浓度将变为0.01mol/0.1L=0.1mol/L;
(4)使紫色石蕊试液变红色的物质是酸,A极上是氢氧根离子放电,氢离子浓度增大,酸性增强,所以A及附近的溶液变红;电解硝酸银溶液的总方程式为4 AgNO3+2H2O 4H NO3+O2↑+4Ag,所以最终得到的溶液是硝酸溶液。
4H NO3+O2↑+4Ag,所以最终得到的溶液是硝酸溶液。
考点:考查电解原理的应用,正负极的判断,电极反应式的书写与计算,电极产物的判断
本题难度:困难
3、填空题 电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答
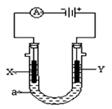
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式为 。在X极附近观察到的实验现象是 。
②Y电极上的电极反应式为 。检验该电极反应产物的方法是 。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是 ,电极反应为 。
②Y电极的材料是 ,电极反应式为 。
(说明:杂质发生的电极反应不必写出)
参考答案:(1)①2H++2e-=H2↑ 放出气体,溶液变红
②2Cl―2e-=Cl2↑ 把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色。
(2)①纯铜 Cu2++2e-=Cu ②粗铜 Cu―2e-=Cu2+
本题解析:(1)①X电极与电源的负极相连,做阴极,溶液中的氢离子放电,电极反应式是2H++2e-=H2↑。由于溶液中氢离子放电,破坏力阴极周围水的电离平衡,导致溶液中OH-浓度增大,溶液碱性增强,即在X极附近观察到的实验现象是放出气体,溶液变红。
②Y电极是阳极,溶液中的氯离子放电,电极反应式是2Cl―2e-=Cl2↑。氯气具有强氧化性,据此可以进行检验,具体方法是把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色。
(2)粗铜精炼时,粗铜做阳极和电源的正极相连,发生氧化反应。纯铜做阴极,和电源的负极相连,溶液中的铜离子放电,发生还原反应。
考点:考查电解饱和食盐水以及纯铜精炼的有关判断和电极反应式的书写
点评:该题是高考中额常见题型和重要的考点,属于基础性试题的考查,难度不大。该题的关键是明确电解原理,以及溶液中离子的放电顺序,有助于培养学生的应试能力和规范的答题能力,提高学生灵活运用基础知识解决实际问题的能力。
本题难度:一般
4、选择题 有关下图的说法正确的是
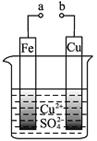
A.构成原电池时Cu极反应为: Cu