��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����(Ni��Cd)�ɳ�������ִ��������й㷺Ӧ�á���֪ij���ӵ�صĵ������ҺΪKOH��Һ����䡢�ŵ簴��ʽ���У�Cd��2NiO(OH)��2H2O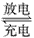 Cd(OH)2��2Ni(OH)2���йظõ�ص�˵����ȷ����
Cd(OH)2��2Ni(OH)2���йظõ�ص�˵����ȷ����
[? ]
A�����ʱ������Ӧ��Ni(OH)2��e-��OH-��NiO(OH)��H2O
B���������ǻ�ѧ��ת��Ϊ���ܵĹ���
C���ŵ�ʱ����������Һ�ļ��Բ���
D���ŵ�ʱ�������Һ�е�OH-�������ƶ�
�ο��𰸣�A
���������
�����Ѷȣ�һ��
2��ѡ���� ��ͼ��ʾ�����δ���Ʊ���ʳ��ˮ����������Mg2+������̼������Ƭ��������������ɣ�һ��ʱ�����Ƭ�������ֻ�����������������ȷ����
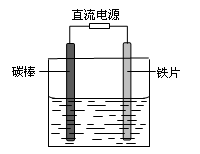
A��̼����ֱ����Դ�ĸ���
B��̼���Ϸ���������Ӧ
C����Ƭ�ϵĵ缫��ӦʽΪ2Cl�D�D2e���� Cl2��
D����Ƭ�������ֵĻ�������Mg(OH)2
�ο��𰸣�BD
��������������Ƭ�ӵ�Դ���������ʧ�����ܽ⣬�����ܲ������壬����Ƭ���ӵ�Դ������̼�����ӵ�Դ������
̼��������2Cl�D�D2e���� Cl2��
��Ƭ������2H����2e��=H2�����ƻ���ˮ�ĵ���ƽ�⣬ʹ��Һ�ʼ��ԣ���Mg(OH)2�����ϣ�Mg2����2OH��=Mg(OH)2��
��ΪBD
�����Ѷȣ�һ��
3��ѡ���� ����������ȷ���ǣ� ��
A���������ζ���������ʣ��������ᶼ��ǿ�����
B��ǿ����Һ�е�������Ũ��һ������������Һ�е�������Ũ��
C������������Ҵ��������ۻ�����Ƿǵ����
D��NaOH��Һ�ĵ�����һ���Ȱ�ˮ��Һ�ĵ�����ǿ
�ο��𰸣�C
�����������
�����Ѷȣ���
4��ʵ���� ��17�֣������ڹ�ũҵ������Ӧ�÷dz��㷺����ش��������⣺
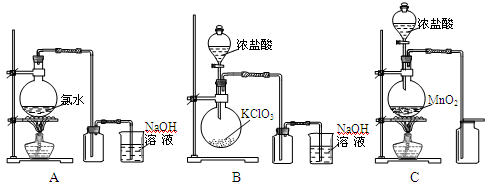
��1����������λͬѧ�ֱ���Ƶ�ʵ������ȡ���ռ�������װ�ã�������õ��� ������ţ���
��2��ij����С��ͬѧ����ͼ��ʾװ��ͨ�����ʳ��ˮ��̽������������ʣ���ش�
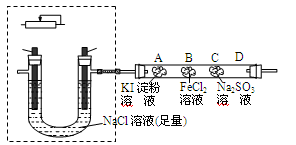
�����е缫:C��Fe��ѡ����������в������ߡ���Դ�� ���������������Ե��ڵ�����ͬʱ����缫���ϣ��������ӷ�Ӧ����ʽΪ ��
���������������Ե��ڵ�����ͬʱ����缫���ϣ��������ӷ�Ӧ����ʽΪ ��
��ͨ��һ��ʱ�������A��B��C�����ǽ��в�ͬ��Һ����������A��B��������ɫ�仯�ֱ�Ϊ �� ��C�����������ӷ�Ӧ����ʽΪ ��
��Ϊ��ֹ�����ݳ������Ⱦ��Ӧ��ȡ�Ĵ�ʩ�� ��
��3�����������ռ�������448mL����״������ֹͣʵ�飬��U�ι���Һ������Ͳ�в�����Ϊ400mL����ҡ�Ⱥ������ϼ������ҺpH= ��
�ο��𰸣���1����2�֣�B
��2���ټ���ͼ��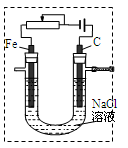 ��2�֣� 2Cl-+2H2O====Cl2��+H2��+2OH-��3�֣�
��2�֣� 2Cl-+2H2O====Cl2��+H2��+2OH-��3�֣�
����ɫ����ɫ��2�֣���dz��ɫ���ɫ��2�֣�
Cl2+SO32-+H2O==2Cl-+ SO42-+2H+��2�֣�
����D����һ�Ž���NaOH��Һ��������β��ͨ��ʢ��NaOH��Һ���ձ��С�2�֣�
��3����2�֣�13
�����������1��������ˮ�е��ܽ�Ȳ���Aװ���ü�����ˮ�ķ����������õ����������٣������ж���Ӧ����β��������װ��Cȱ��β������װ�ã�ʵ������ȡ���ռ�������װ����õ���B����2����ͨ�����ʳ��ˮ�Ʊ�������̽������������ʣ�����Ϊ����������������ĵ缫Ӧ���Դ������������װ��ͼ���𰸣��������ӷ�Ӧ����ʽΪ2Cl-+2H2O Cl2��+H2��+2OH-����ͨ��һ��ʱ�������A��������⻯�ط�Ӧ���ɵ��ʵ⣬�������۱���ɫ��B���������Ȼ�������Ӧ�����Ȼ�������dz��ɫ���ɫ��C������������������Һ��Ӧ���������ƺ����ᣬ���������ӷ�Ӧ����ʽΪCl2+SO32-+H2O==2Cl-+ SO42-+2H+����Ϊ��ֹ�����ݳ������Ⱦ��Ӧ��ȡ�Ĵ�ʩ����D����һ�Ž���NaOH��Һ��������β��ͨ��ʢ��NaOH��Һ���ձ��У�����3�������ռ���������ΪH20.448L��n(H2)=0.448L��22.4L/mol=0.02mol���ɷ���ʽ��2Cl-+2H2O
Cl2��+H2��+2OH-����ͨ��һ��ʱ�������A��������⻯�ط�Ӧ���ɵ��ʵ⣬�������۱���ɫ��B���������Ȼ�������Ӧ�����Ȼ�������dz��ɫ���ɫ��C������������������Һ��Ӧ���������ƺ����ᣬ���������ӷ�Ӧ����ʽΪCl2+SO32-+H2O==2Cl-+ SO42-+2H+����Ϊ��ֹ�����ݳ������Ⱦ��Ӧ��ȡ�Ĵ�ʩ����D����һ�Ž���NaOH��Һ��������β��ͨ��ʢ��NaOH��Һ���ձ��У�����3�������ռ���������ΪH20.448L��n(H2)=0.448L��22.4L/mol=0.02mol���ɷ���ʽ��2Cl-+2H2O Cl2��+H2��+2OH- �ã�
Cl2��+H2��+2OH- �ã�
n(OH-)=0.02mol��2=0.04mol��c(OH-)="0.04mol��0.4L=0.1mol/L" ��pH=14-(-lg10-1)=13��
���㣺�����������Ʊ������ʣ����ԭ����Ӧ�á�
�����Ѷȣ�����
5��ѡ���� �������������ֱ�Ϊ̼���������NaOH��Һʱ��������10.7g?Fe��OH��3����ʱ��������a?molH2O������b?LH2����״��������a��b�ֱ�Ϊ��������
A��a=0.25��b=4.48
B��a=0.3��b=3.36
C��a=0.25��b=2.24
D��a=0.2��b=22.24
�ο��𰸣��缫��Ӧ�ֱ�Ϊ��������Fe��Fe2++2e-��������2H++2e-��H2�����ܵķ�ӦΪ��Fe+2H2O?ͨ��?.?Fe��OH��2+H2����
4Fe��OH��2+O2+2H2O�T4Fe��OH��3�����ݷ���ʽ�õ���������0.1mol?Fe��OH��3����ʱ��������H2O=0.2mol+0.05mol=0.025mol������0.1molH2������״����2.24L������
��ѡC��
���������
�����Ѷȣ���