微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 氯碱工业的基本原理就是电解饱和食盐水。下列关于实验室电解饱和食盐水的说法中正确的是(? )
A.可以选用石墨棒作为阴、阳极材料,但阳极材料也可以用铁棒
B.用湿润的淀粉KI试纸靠近阴极区域,试纸变蓝
C.电解过程中,在阳极区域溶液中滴加品红,品红褪色
D.实验结束后,将溶液搅拌,然后用pH试纸检验,溶液呈中性
2、填空题 (14分)高铁酸钠(Na2FeO4)是一种多功能、高效无毒的新型绿色水处理剂。
(1)Na2FeO4中铁元素的化合价是 价,Na2FeO4具有较强的 (填“氧化性”或“还原性”)。
(2)用Na2FeO4给水消毒、杀菌时得到的Fe3+可以净水,Fe3+净水原因是 (用离子方程式表示)。
(3)工业上可用FeCl3、NaOH 、NaClO三种物质在一定条件下反应制得Na2FeO4,完成下列化学方程式:2FeCl3 + 10NaOH + 3NaClO = 2 + 5 + 9 。
(4)工业上还可用电解浓NaOH溶液的方法制Na2FeO4 。
① 若电解所需的浓NaOH溶液为16 mol/L,则在实验室配制500 mL该浓度的溶液需NaOH g,配制过程所需玻璃仪器是 。
② 电解浓NaOH溶液制备Na2FeO4,其工作原理如下图所示:

阳极的电极反应式是 ;可循环使用的物质是 ,理由是 。
3、选择题 如图所示,X为铁、Y为石墨电极,a是电解质溶液,实验开始前,在U形管的两边同时滴入几滴酚酞试液,下列叙述错误的是
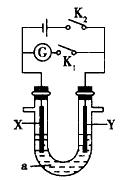
?[? ]
A.合上K1、断开K2,若a是稀硫酸,则Y上有 气泡冒出
B.合上K2、断开K1,若a是饱和食盐水,则Y 电极附近溶液慢慢变为红色
C.合上K2、断开K1,若a是硫酸铜溶液,则Y 电极上有红色物质析出
D.合上K2、断开K1,若a是氢氧化铁胶体,则X电极附近红褐色加深
4、填空题 现向含6 mol KI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量的关系如图所示。已知:
①BrO3-+6I-+6H+=3I2+Br-+3H2O;
②2BrO3-+I2=2IO3-+Br2。
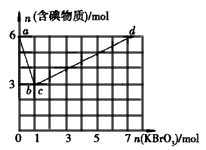
请回答下列问题。
(1)b点时,KI反应完全,则消耗的氧化剂与还原剂的物质的量之比为___,还原产物是___ 。
(2)b→c过程中只有一种元素的化合价发生了变化,写出该过程中发生反应的离子方程式__。
(3)有同学由反应②得出氧化性I2>Br2的结论,你认为是否正确,并说明理由___。
(4)含6 mol KI的硫酸溶液所能消耗n(KBrO3)的最大值为__。
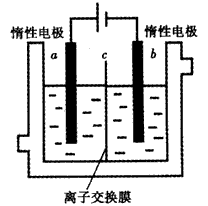
(5)现以电解法制备碘酸钾,实验装置如图所示。先将一定量的碘溶于 过量氢氧化钾溶液中,发生反应:3I2+6KOH=5KI+KIO3+3H2O, 将该溶液加入阳极区,另将氢氧化钾溶液加入阴极区,开始电解。阳极的电极反应式为___;阴极观察到的现象是___。
5、选择题 用石墨作电极,电解硫酸铜和氯化钠的混合溶液,在溶液中2n(Na+)≤n(SO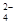 ),在任何情况下,阴、阳两极不可能同时发生的反应是? ( )
),在任何情况下,阴、阳两极不可能同时发生的反应是? ( )