微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在反应中CaH2+2H2O=Ca(OH)2+2H2↑,下列叙述正确的是( )
①H2是氧化产物?②H2是还原产物?③H2是氧化产物又是还原产物④CaH2中氢元素既被氧化又被还原?⑤生成1mol?H2时,电子转移1mol⑥H2O是氧化剂.
A.②④⑤
B.③⑤⑥
C.①④⑥
D.②⑤⑥
参考答案:因反应CaH2+2H2O=Ca(OH)2+2H2↑中,CaH2中H元素的化合价为-1价,H2O中H元素的化合价为+1价,H2中H元素的化合价为0,
则H2既是氧化产物又是还原产物,故①②错误,而③正确;
CaH2中H元素的化合价只升高,被氧化,故④错误;
由反应可知,生成2molH2时,转移的电子为2mol,则生成1molH2时,电子转移1mol,故⑤正确;
反应中H2O中H元素的化合价降低,则H2O是氧化剂,故⑥正确;
故选B.
本题解析:
本题难度:一般
2、简答题 A、B、C、D、E五种短周期元素的原子序数依次增大,且已知:①其原子半径的大小关系是:D>E>B>C>A;②A、D同主族,可形成离子化合物;③B、D、E三者的最高价氧化物对应的水化物两两之间均可反应生成可溶性盐和水,且所得盐中均含C元素;④B、E两元素原子的最外层电子数之和等于A、C、D三种元素原子的最外层电子数之和.请填写下列空白:
(1)常温下,浓度均为0.lmol/L的B、D的最高价氧化物对应的水化物溶液中,水电离出的c(H+)的相对大小关系为X______Y(填写“大于”“于”或“等于”),化合物BA5所属晶体类型为离子晶体,其电子式为______.
(2)在合成BA3的实际生产过程中,常采取______的方法,使气态BA3变成液态后从混合气体中分离出去,以促使化学平衡向生成BA3的方向移动.
(3)E单质与足量的D的最高价氧化物的水化物溶液反应的离子方程式为______;BC2与水反应被氧化与被还原的物质的量之比是______.
(4)已知在298K时,lg?B2A4气体燃烧生成B2和A2C气体,放出16.7kJ的热量.该燃烧反应的热化学方程式______.
(5)X、Y分别是B、C与A形成的10电子微粒,请你提供一个能验证X结合H+能力较Y强的离子方程式______.
参考答案:由题干条件可知,A、B、E是在三个不同周期的短周期主族元素,B、C在同一周期(第二周期),D、E在同一周期(第三周期),A为H元素,A、D同主族,可形成离子化合物,可形成NaH,D为Na元素,B、D、E三者的最高价氧化物对应的水化物两两之间均可反应生成可溶性盐和水,则一定有Al元素,因D为Na,则E为Al,可形成含氧酸盐,则所得盐中均含C元素,C应为O元素,B为N元素,则
(1)B、D的最高价氧化物对应的水化物分别为HNO3、NaOH,都为强电解质,浓度相同时,对水的电离的抑制程度相同,则水电离出的c(H+)的相对大小关系X等于Y,化合物NH5所属晶体类型为离子晶体,应为NH4H,为离子化合物,电子式为
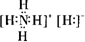
,
故答案为:等于;
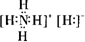
;
(2)使气态NH3变成液态后从混合气体中分离出去,应采用液化的方法,有利于平衡向正反应方向移动,
故答案为:冷却;
(3)Al与NaOH反应的离子方程式为2Al+2H2O+2OH-=2AlO2-+3H2↑,在反应3NO2+H2O=2HNO3+NO中,被氧化与被还原的物质的量之比2:1,
故答案为:2Al+2H2O+2OH-=2AlO2-+3H2↑;2:1;
(4)n(N2H4)=132mol,则1molN2H4气体燃烧放出的热量为32×16.7kJ=534.4kJ,
所以该燃烧反应的热化学方程式为N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=-534.4kJ/mol,
故答案为:N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=-534.4kJ/mol;
(5)X、Y分别是B、C与A形成的10电子微粒,则X为NH3,Y为H2O,NH3可与H3O+反应生成NH4+,
发生NH3+H3O+=NH4++H2O,说明NH3结合H+能力较H2O强,故答案为:NH3+H3O+=NH4++H2O.
本题解析:
本题难度:一般
3、选择题 下列反应属于氧化还原反应的是( )
A.CaO+H2O=Ca(OH)2
B.NaCl+AgNO3=NaNO3+AgCl↓
C.H?2CO3=H2O+CO2↑
D.H2+CuO=Cu+H2O
参考答案:A、CaO+H2O=Ca(OH)2,反应前后无元素化合价变化不是氧化还原反应,故A不符合;
B、NaCl+AgNO3=NaNO3+AgCl↓,反应前后无元素化合价变化不是氧化还原反应,故B不符合;
C、H?2CO3=H2O+CO2↑,反应前后无元素化合价变化不是氧化还原反应,故C不符合;
D、H2+CuO=Cu+H2O,反应前后无氢元素和铜元素化合价变化,是氧化还原反应,故D符合;
故选D.
本题解析:
本题难度:简单
4、选择题 下列反应中H2O表现还原性的是( )
A.2Na+2H2O=2NaOH+H2↑
B.2F2+2H2O=4HF+O2↑
C.CO2+H2O=H2CO3
D.C+H2O
CO+H2
参考答案:A.2Na+2H2O=2NaOH+H2↑中,钠中的钠元素化合价升高,水中氢元素化合价降低,所以钠作还原剂,水作氧化剂,故A错误;
B.2F2+2H2O=4HF+O2↑中,氟气中氟元素的化合价降低,水中氧元素的化合价升高,所以氟气是氧化剂,水是还原剂,故B正确;
C.CO2+H2O=H2CO3↑中,该反应中各元素的化合价都不变化,所以不是氧化还原反应,则水不是还原剂,故C错误;
D.C+H2O?△?.?CO+H2中,该反应中碳中的碳元素化合价升高,水中的氢元素化合价降低,所以碳是还原剂,水是氧化剂,故D错误;
故选B.
本题解析:
本题难度:一般
5、选择题 黑火药的爆炸反应为:2KNO3+S+3C=K2S+N2↑+3CO2↑,其中被还原的元素是( )
A.N
B.C
C.N和C
D.N和S
参考答案:D
本题解析:
本题难度:简单