微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 pH值相同的盐酸溶液和醋酸溶液分别和锌反应,若最后锌都已完全溶解,放出的氢气一样多,则下列判断正确的是(?)
A.整个反应阶段平均速率:醋酸>盐酸
B.反应所需时间:醋酸>盐酸
C.参加反应的锌的质量:盐酸<醋酸
D.开始反应速率:盐酸>醋酸
参考答案:A
本题解析:pH值相同的盐酸溶液和醋酸溶液,醋酸的浓度远远大于盐酸,最后锌完全反应,说明醋酸和盐酸足量。A、因为醋酸的浓度大,反应时电离平衡向右移动,所以整个反应阶段平均速率:醋酸>盐酸,正确;B、醋酸平均反应速率大,则反应所需时间:醋酸<盐酸,错误;C、因为最后锌都已完全溶解,放出的氢气一样多,所以参加反应的锌质量相等,错误;D、开始时,pH相同,H+浓度相同,则开始时反应速率相等,错误。
本题难度:一般
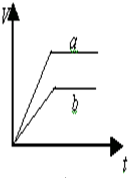
2、选择题 等质量的两份锌粉a和b,分别加入过量的稀硫酸中,a中同时加入少量CuSO4溶液,下列各图中表示其产生氢气总体积(V)与时间(t)的关系正确的是( )
A.

B.

C.
D.
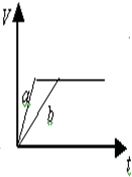
参考答案:锌和硫酸反应,加入硫酸铜,会置换出金属铜,形成锌、铜、稀硫酸原电池,加速金属锌和硫酸反应的速率,所以反应速率是:a>b,
速率越大,锌完全反应时所用的时间越短,所以a所用的时间小于b的时间;
产生氢气的量取决于金属锌的质量,而a中,金属锌一部分用于置换金属铜,导致和硫酸反应生成氢气的量减少,所以氢气的体积是:a<b.
故选A.
本题解析:
本题难度:简单
3、选择题 下列各组实验中,过氧化氢分解最快的是( )
| H2O2的浓度(质量分数) | 温度(℃) | 催化剂的使用
A
2
10
使用MnO2
B
4
10
不使用
C
6
30
使用MnO2
D
6
30
不使用
|
A.A
B.B
C.C
D.D
参考答案:浓度越大,温度越高,反应速率越快,使用催化剂加快反应.
故选C
本题解析:
本题难度:简单
4、选择题 反应2A(g) 2B(g)+C(g)△H>0达平衡时,要使v(正)降低,A的浓度增大,应采取的措施是(?)
2B(g)+C(g)△H>0达平衡时,要使v(正)降低,A的浓度增大,应采取的措施是(?)
A.加压
B.减压
C.减小C的浓度
D.降温
参考答案:D
本题解析:A、加压,是加快反应速率的,错误;B、减压可以使v(正)降低,且平衡正向移动,A的浓度减小,错误;C、减小C的浓度,平衡正向移动,A的浓度减小,错误;D、降温是向着放热方向移动的,正向是一个吸热的方向,因些降温可以降低正反应的速率,还呆以增大A的浓度,正确。
本题难度:一般
5、选择题 下列各组反应(表内物质均为反应物)刚开始时,放出H2的速率最大的是
[? ]
金属(粉末状) 物质的量 酸的浓度 酸的体积 反应温度
A. Mg 0.1mol 6mol/L硝酸 10mL 60℃
B. Mg 0.1mol 3mol/L盐酸 10mL 30℃
C. Fe 0.1mol 3mol/L盐酸 10mL 60℃
D. Mg ? 0.1mol 3mol/L盐酸 10mL 60℃
参考答案:D
本题解析:
本题难度:一般