微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈蓝色。下列说法中不正确的是

[? ]
A.X是正极,Y是负极
B.X是负极,Y是正极
C.a极和Pt都有气泡产生
D.U形管中溶液的碱性增强
参考答案:A
本题解析:
本题难度:一般
2、选择题 市场上经常见到的标记为Li-ion的电池称为“锂离子电池”。它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料。这种锂离子电池的电池反应式为:
Li+2Li0.35NiO2 2Li0.85NiO2。下列说法不正确的是
2Li0.85NiO2。下列说法不正确的是
[? ]
A.放电时,负极的电极反应式:Li-e-==Li+
B.充电时,Li0.85NiO2既发生氧化反应又发生还原反应
C.该电池不能用水溶液作为电解质
D.放电过程中Li+向负极移动
参考答案:D
本题解析:
本题难度:一般
3、选择题 用铂电极电解CuSO4溶液,当溶液中Cu2+浓度降至一定范围时,需加入适量的物质。如果要使加入物质后溶液的浓度和体积恢复到电解前的状况,所加入的物质是?
A.CuSO4
B.CuSO4・5H2O
C.CuO
D.Cu(OH)2
参考答案:C
本题解析:用惰性电极电解CuSO4溶液,反应
阴极:2Cu2++4e==2Cu
阳极:4OH--4e==O2↑+2H2O
总反应式:
2CuSO4+2H2O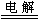 2Cu+2H2SO4+O2↑
2Cu+2H2SO4+O2↑
电解的结果,除了在阴极得到Cu,在阳极放出O2之外,溶液中H+浓度增大,产生了H2SO4。因此,要使溶液恢复到原来状况,除了要补充Cu2+,还得中和掉H+。由此可知,单纯加入CuSO4或CuSO4・5H2O是不行的,而加入CuO或Cu(OH)2则可达到上述目的。但需要溶液的浓度和体积不变,加入Cu(OH)2会多生成H2O出来,所以选CuO。
本题难度:一般
4、填空题 盐酸、硫酸和硝酸是中学阶段常见的“三大酸”.请就“三大酸”与金属铜反应的情况,回答下列问题:
(1)我们知道,稀盐酸与铜不反应,但向稀盐酸中加入H2O2后,则可使铜溶解.该反应的化学方程式为_____________________________.某同学未加入氧化剂,而是设计了一个实验装置,也能使铜很快溶于稀盐酸.请在下面的方框中画出该装置:

(2)在一定体积的18?mol/L的浓硫酸中加入过量的铜片,加热使之反应,被还原的硫酸是0.9?mol,则该硫酸的实际体积________(填“>”“=”或“<”)100?mL. 有同学提出:若使剩余的铜片继续溶解,可向其中加入硝酸盐,可行吗?________(填“可行”或“不可行”).
(3)将等质量的铜片分别与等体积、过量的浓硝酸和稀硝酸反应,所得到的溶液前者呈绿色,后者呈蓝色,某同学提出可能是Cu2+浓度不同引起的,你同意这种看法吗?________(填“同意”或“不同意”),原因是______________________________________.另一同学提出溶液呈“绿色”是溶液中Cu2+与NO2共存的结果,请你设计实验探究此说法正确与否,简述实验方案、实验现象及由此得出的结论:__________________________________________________________________________.
参考答案:(1)Cu+H2O2+2HCl===CuCl2+2H2O
作图:以铜为阳极,以盐酸为电解质溶液的电解池装置

(2)>;可行
(3)不同意;等质量的铜片与等体积、过量的浓硝酸、稀硝酸反应,溶液中Cu2+将一定量的NO2通入铜片与稀硝酸反应后的溶液中,若溶液呈绿色,则该同学的结论正确,反之,不正确(其他合理答案也对)
本题解析:
本题难度:一般
5、填空题 高锰酸钾可用于生活消毒,是中学化学常见的氧化剂。工业上,用软锰矿(主要成分是二氧化锰)制高锰酸钾的流程如下(部分条件和产物省略):

请回答下列问题:
(1)提高锰酸钾浸出率(浸出锰酸钾质量与固体总质量之比)的措施有 。
(2)写出二氧化锰和氢氧化钾熔融物中通入空气时发生的主要化学反应的方程式: 。
(3)从经济性考虑试剂X宜选择(填名称): 。上述流程中,设计步骤IV和V的目的是 。
(4)以惰性材料为电极,采用电解锰酸钾溶液的方法完成步骤III转化。
①阳极反应式为 。
②电解过程中,阴极附近电解质溶液的pH将 (填:增大、减小或不变)。
(5)测定高锰酸钾样品纯度:向高锰酸钾溶液中滴定硫酸锰溶液,产生黑色沉淀。当溶液由紫红色刚好褪色且半分钟不变色,表明达到滴定终点。写出离子方程式: 。
(6)已知:常温下, 。工业上,调节pH沉淀废水中Mn2+.当pH=10时,溶液中c(Mn2+)= 。
。工业上,调节pH沉淀废水中Mn2+.当pH=10时,溶液中c(Mn2+)= 。
参考答案:(9分)
(1)加热、搅拌等(1分)
(2)2MnO2+4KOH+O2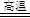 2K2MnO4+2H2O(1分)
2K2MnO4+2H2O(1分)
(3)石灰乳(或生石灰)(1分)
循环利用二氧化锰、氢氧化钾,提高原料利用率(1分)
(4)①MnO42--e-=MnO4-(1分)②增大(1分)
(5)2MnO4-+3Mn2++2H2O=5MnO2↓+4H+(2分)
(6)2.0×10-5mol/L(1分)
本题解析:(1)为提高提高锰酸钾浸出率,应采用加热、搅拌的方法,使反应尽可能多的生成锰酸钾;
(2)根据流程图,二氧化锰与氢氧化钾溶液、氧气在高温条件下发生反应生成锰酸钾和水,化学方程式为2MnO2+4KOH+O2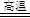 2K2MnO4+2H2O;
2K2MnO4+2H2O;
(3)碳酸钾与X反应又得氢氧化钾,所以X试剂应是与碳酸钾发生复分解反应的物质,结合碳酸根离子的性质判断X是石灰乳或生石灰;设计步骤IV和V的目的是使氢氧化钾、二氧化锰重新被利用,提高原料的利用率;
(4)锰酸钾生成高锰酸钾,Mn元素的化合价升高,所以锰酸钾发生氧化反应,所以电解锰酸钾溶液的阳极反应式为锰酸根离子失去电子生成高锰酸根离子,电极反应式为MnO42--e-=MnO4-;阴极是氢离子放电生成氢气,氢离子浓度减小,氢氧根离子浓度增大,则溶液的pH增大;
(5)向高锰酸钾溶液中滴定硫酸锰溶液,产生黑色沉淀,该黑色沉淀是二氧化锰,所以该滴定反应的离子方程式为2MnO4-+3Mn2++2H2O=5MnO2↓+4H+;
(6)Mn(OH)2的溶度积Ksp=c(Mn2+)c(OH-)2=2.0×10-13,当pH=10时,c(OH-)=1.0×10-4mol/L,所以c(Mn2+)=2.0×10-13/ c(OH-)2=2.0×10-5mol/L.
考点:考查对反应流程的分析,电极反应式的判断,离子方程式的书写,溶度积的计算
本题难度:一般