微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列叙述正确的是
[? ]
A.电解饱和食盐水制烧碱时,Fe作阳极,石墨作阴极
B.电解氯化铜时,阳极上产生的气体质量和阴极上析出的铜的质量相等
C.钢铁在空气中发生电化腐蚀时,铁作负极
D.原电池工作时,阳离子移向电池的负极
参考答案:C
本题解析:
本题难度:一般
2、简答题 氯碱工业是化学工业基础,目前我国大多采用立式隔膜电解槽电解食盐水.电解饱和食盐水的化学方程式:2NaCl+2H2O
NaOH+Cl2↑+H2↑,
(1)若要制得标准状况下的氯气89.6L,理论上需要质量分数为26%的食盐水多少kg?______
(2)若用(1)中所得氯气来制备密度为1.05g/cm3的盐酸2.8kg,求所得盐酸物质的量浓度是多少?(答案保留到小数点后一位)______.
参考答案:(1)设食盐水的质量是xKg,
2NaCl+2H2O通电.NaOH+Cl2↑+H2↑,
117g 22.4L
x×1000×26%g 89.6L
x=117g×89.6L(1000×26%)g×22.4L=1.8,
答:理论上需要质量分数为26%的食盐水1.8kg;
(2)溶液的体积=2800g1.05g/cm3=2666.7ml=2.67L,盐酸的物质的量浓度=89.6L22.4L/mol×22.67L=3mol/L;
答:所得盐酸物质的量浓度是3mol/L;
本题解析:
本题难度:一般
3、选择题 如图为一电化学综合实验装置。其中装置D为用加有酚酞的淀粉碘化钾溶液湿润的长条滤纸,a、b、c、d为Pt片。整套装置工作一段时间后,发现Pt片d的周围变为蓝色。下列有关说法错误的是
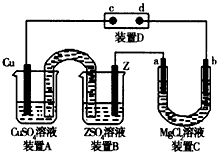
[? ]
A.Pt片c上发生的反应为2H++2e-=H2↑,c周围变为红色
B.b电极周围有白色沉淀生成
C.Z单质的金属活动性较Cu强
D.装置A、B之间倒置的U形管,是沟通两装置的离子通道
参考答案:C
本题解析:
本题难度:一般
4、填空题 (9分)近期“五水共治”越来越引起人们的重视。对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施。
(1)含乙酸钠和对氯酚( )的废水可以通过构成微生物电池除去,其原理如下图所示。
)的废水可以通过构成微生物电池除去,其原理如下图所示。
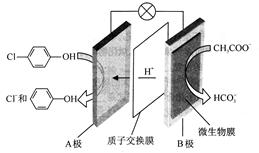
①B是电池的 极(填“正”或“负”);
②A极的电极反应式为 。
(2)电渗析法处理厨房垃圾发酵液,同时得到乳酸的原理如下图所示(图中“HA”表示乳酸分子,A-表示乳酸根离子)。

①阳极的电极反应式为 ;
②简述浓缩室中得到浓乳酸的原理 ;
③电解过程中,采取一定的措施可控制阳极室的pH约为6~8,此时进入浓缩室的OH-可忽略不计。400 mL10 g/L 乳酸溶液通电一段时间后,浓度上升为 145 g/L(溶液体积变化忽略不计),则阴极上产生的H2在标准状况下的体积约为 L(乳酸的摩尔质量为90g/ mol )。
参考答案:(1) ①负 (1分) 
(2)①4OH- - 4e- = 2H2O + O2↑ (2分)
②阳极OH-放电,c(H+)增大,H+从阳极通过阳离子交换膜进入浓缩室(1分);A-通过阴离子交换膜从阴极进入浓缩室,H++A― = HA,乳酸浓度增大(1分) ③ 6.72 (2分)
本题解析:(1)①根据装置图可知氢离子向A电极移动,这说明A电极是正极,则B电极是负极。
②A极是正极,得到电子发生还原反应,则电极反应式为 。
。
(2)①电解池中阳极失去电子发生氧化反应,阳极加入硫酸,则溶液中的氢氧根离子放电,电极反应式为4OH- - 4e- = 2H2O + O2↑。
②阳极OH-放电,导致溶液中c(H+)增大,H+从阳极通过阳离子交换膜进入浓缩室,A-通过阴离子交换膜从阴极进入浓缩室,二者结合生成HA,即H++A―=HA,从而导致乳酸浓度增大。
③反应后增加的乳酸质量是0.4L×(145g/L―10g/L)=54g,物质的量是54g÷90g/mol=0.6mol,因此结合氢离子的物质的量是0.6mol,根据电荷守恒可知生成的氢气是0.3mol,在标准状况下的体积是6.72L。
考点:考查电化学原理的应用
本题难度:困难
5、填空题 (12分)已知Cr(OH)3在碱性较强的溶液中将生成[Cr(OH)4]
参考答案:
本题解析:
本题难度:困难