微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知在1×105?Pa,298?K条件下,4g?氢气燃烧生成液态水放出572?kJ热量,下列表示氢气燃烧的热化学方程式的是
[? ]
A.H2O(g)?=?H2(g)+1/2O2(g)?△H=+286kJ/mol
B.2H2(g)+?O2(g)=2H2O(l)?△H=-572kJ/mol
C.H2(g)+?1/2O2(g)=?H2O(g)?△H=-286kJ/mol
D.H2(g)+1/2O2(g)=H2O(l)?△H=+286?kJ/mol
参考答案:B
本题解析:
本题难度:简单
2、选择题 实验表明,在一定条件下,乙烯和水的反应可表示为:C2H4(g) + H2O (g) = C2H5OH(g) ΔH=-45.8 kJ/mol 则下列说法中正确的是
[? ]
A.实验中,乙烯的用量不会影响该反应的反应焓变ΔH
B.0.5 mol H2O(l) 完全反应放出的热量为22.9 kJ
C.1 mol C2H5OH(g)具有的能量大于1 mol C2H4(g)和1 mol H2O(g)所具有的能量和
D.1 mol C2H4(g)和1 mol H2O(g)中化学键的总键能大于1 mol C2H5OH(g)中化学键的总键能
参考答案:A
本题解析:
本题难度:简单
3、填空题 应用化学反应原理知识解决下列问题
(1)某温度下纯水中c (H+) = 2.0×10-7 mol・L-1,则此纯水中的c (OH-) = 。
(2)将某CH3COOH溶液稀释10倍,则稀释后的溶液中c(H+) 原来的十分之一(填“大于”、“小于”或“等于”)。
(3)0.1 mol・L-1的下列溶液①HCl、②CH3COOH、③CH3COONa、④FeCl3、⑤NaOH,其中pH最大的是 (填序号);实验室配制的氯化铁溶液显弱酸性的原因: (用离子方程式表示)。
(4)一定条件下22g二氧化碳气体与足量氢气反应生成气态甲醇(CH3OH)和水蒸气时,放出247.5kJ热量,其反应的热化学方程式为 。
参考答案:(1)2.0×10-7 mol・L-1(1分) (2)大于 (2分)
(3)⑤ (2分) Fe3++3H2O Fe(OH)3+3H+ (3分)
Fe(OH)3+3H+ (3分)
(4)CO2(g)+3 H2(g)=CH3OH(g)+H2O(g ) △H=-495.0kJ・mol-1 (3分)
本题解析:(1)由于在任何的纯水中,水电离出的氢离子浓度总是等于水电离出的OH-浓度,因此某温度下纯水中c (H+)=2.0×10-7 mol・L-1,则此纯水中的c (OH-)=2.0×10-7 mol・L-1。
(2)醋酸是弱酸,存在电离平衡CH3COOH CH3COO-+H+。稀释促进电离,溶液中氢离子的物质的量增大,所以将某CH3COOH溶液稀释10倍,则稀释后的溶液中c(H+)大于原来的十分之一。
CH3COO-+H+。稀释促进电离,溶液中氢离子的物质的量增大,所以将某CH3COOH溶液稀释10倍,则稀释后的溶液中c(H+)大于原来的十分之一。
(3)HCl是强酸,酸性最强,pH最小。CH3COOH是弱酸,溶液显酸性,pH小于7。CH3COONa是强碱弱酸盐,CH3COO-水解,溶液显碱性,pH大于7。FeCl3是强酸弱碱盐,铁离子水解溶液显酸性,pH小于7。NaOH是强碱,溶液的碱性最强,pH最大,因此pH最大的是⑤;FeCl3是强酸弱碱盐,铁离子水解溶液显酸性,离子方程式为Fe3++3H2O Fe(OH)3+3H+。
Fe(OH)3+3H+。
(4)22g二氧化碳的物质的量=22g÷44g/mol=0.5mol,此时反应放出的热量是247.5kJ,则1molCO2参加反应放出的热量是247.5kJ×2=495.0kJ,因此该反应的热化学方程式为CO2(g)+3 H2(g)=CH3OH(g)+H2O(g ) △H=-495.0kJ・mol-1。
考点:考查水的电离、盐类水解、稀释对电离平衡的影响、溶液pH大小比较以及热化学方程式的书写
本题难度:一般
4、填空题 请按要求完成下列问题:
(1)已知葡萄糖的燃烧热是2804kJ/mol,请写出葡萄糖燃烧的热化学方程式:______,当它氧化生成1g?H2O(l)时放出的热量是:______;
(2)向1mol?L-1纯碱溶液中滴入酚酞溶液,观察到的现象是______,原因是(用离子方程式表示)______.
参考答案:(1)燃烧热是指1mol可燃物完全燃烧生成稳定的氧化物放出的热量,葡萄糖的燃烧热是2804kJ/mol,说明1mol葡萄糖完全燃烧生成二氧化碳气体和液态水放出2804kJ的热量,
则反应的热化学方程式为C6H12O6(g)+6O2(g)=6CO2(g)+6H2O(l);△H=-2804KJ/mol,
1g?H2O(l)的物质的量为118mol,则当它氧化生成1g?H2O(l)时放出的热量是118mol×16×2804KJ/mol=26kJ,
故答案为:C6H12O6(g)+6O2(g)=6CO2(g)+6H2O(l);△H=-2804KJ/mol;26kJ;
(2)纯碱为强碱弱酸盐,CO32-水解呈碱性,水解离子方程式为CO32-+H2O
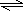
=HCO3-+OH-,加入酚酞溶液变红色,
故答案为:溶液变红;CO32-+H2O
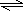
=HCO3-+OH-.
本题解析:
本题难度:一般
5、选择题 已知A、B两种气体在一定条件下可发生反应:2A+B=C+3D+4E.现将相对分子质量为M的A气体mg与适量的B充入一个密闭容器内,恰好完全反应,有少量液滴生成,在相同的温度下测得反应前后压强分别为6.06×106和1.01×107Pa,又测得反应共放热Q?kJ,下列说法正确的是( ? )
A.D为气体
B.C为液体
C.E为气体
D.该反应的热化学方程式2A(g)+B(g)=C(g)+3D(l)+4E(g);△H=-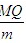 kJ/mol
kJ/mol
参考答案:C
本题解析:
本题难度:一般