|
高中化学知识点大全《热化学方程式》试题巩固(2017年最新版)(四)
2017-08-10 01:19:22
来源:91考试网
作者:www.91exam.org 【 大 中 小】
 (CO)=_____; (CO)=_____;
③实验II条件下反应的平衡常数K=_____________(保留小数点后二位);
④实验III中,若平衡时,CO的转化率大于水蒸气,则a,b必须满足的关系是______;
⑤若在900℃时,实验II反应达到平衡后,向此容器中再加入1molCO、0.5mol H2O、0.2mol CO2、0.5mol H2,则此时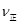 ___________ ___________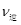 (填“>”或“<”),平衡向__________方向移动(填“正反应”、“逆反应”“不移动”) (填“>”或“<”),平衡向__________方向移动(填“正反应”、“逆反应”“不移动”)
参考答案:(1)-41kJ・mol-1(2分)(2)①A(1分) ②0.16mol・L-1・min-1 (2分)
③0.33(2分) ④a<b(1分) ⑤> 正反应(各1分)
本题解析:(1)②-①-③,整理可得:CO(g)+H2O(g) ="=" CO2(g)+H2(g)△H=-41kJ/mol;(2)①A.若容器中CO的含量保持不变,则其浓度不变,反应处于平衡状态,正确; B.容器中CO2浓度与CO浓度相等,反应可能处于平衡状态,也可能处于非平衡状态,因此不能作为判断反应处于平衡状态的标志,错误; C.无论反应是否达到平衡,都存在V(正)(CO)= V(正) (H2O) ,所以不能判断反应处于平衡状态,错误; D.由于容器的容积不变,气体的物质的量不变,所以无论反应进行到任何程度,容器中混合气体的平均相对分子质量都不变,因此不能判断反应处于平衡状态,错误;②实验I中,从反应开始到反应达到平衡时,CO的平均反应速率V(CO)=(1.6mol÷2L)÷5min=0.16mol/(L・min); ③实验II条件下反应的平衡常数K= ;④由于在其它条件不变时。增大反应物的浓度可以是其它反应物的转化率提高,而其本身的转化率降低,所以在实验III中,若平衡时,CO的转化率大于水蒸气,则a,b必须满足的关系是二者的物质的量的比小于方程式中的计量关系的比,即a<b;⑤若在900℃时,实验II反应达到平衡后,向此容器中再加入1molCO、0.5mol H2O、0.2mol CO2、0.5mol H2,则此时由于Q= ;④由于在其它条件不变时。增大反应物的浓度可以是其它反应物的转化率提高,而其本身的转化率降低,所以在实验III中,若平衡时,CO的转化率大于水蒸气,则a,b必须满足的关系是二者的物质的量的比小于方程式中的计量关系的比,即a<b;⑤若在900℃时,实验II反应达到平衡后,向此容器中再加入1molCO、0.5mol H2O、0.2mol CO2、0.5mol H2,则此时由于Q= ,所以 ,所以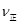 > >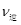 (填“”或“<”),平衡向向正反应方向移动。 (填“”或“<”),平衡向向正反应方向移动。
考点:考查热化学方程式的书写、可逆反应平衡状态的判断、化学反应速率、化学平衡产生的计算、物质转化率的大小比较和影响因素、化学反应进行的方向的判断的知识。
本题难度:困难
2、选择题 下列说法或表示方法正确的是
[? ]
A.等物质的量的硫蒸气和固体硫分别完全燃烧,前者放出热量多
B.1mol碳和2mol碳的燃烧热不同相同
C.在101kPa时,2g氢气完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=?2H2O(l)?△H=-285.8kJ/mol
D.在稀溶液中,H+(aq)?+?OH-(aq)?=?H2O?(l)?△H=-57.3kJ/mol,若将0.5?mol?浓硫酸与1mol?氢氧化钠溶液混合,放出的热量大于57.3kJ
参考答案:AD
本题解析:
本题难度:一般
3、填空题 新的《环境空气质量标准》将于2016年1月1日在我国全面实施。据此,环境空气质量指数(AQI)日报和实时报告包括了SO2、NO2、CO、O3、PM10、PM2.5等指标,为公众提供健康指引,引导当地居民合理安排出行和生活。
(1)汽车排出的尾气中含有CO和NO等气体,用化学方程式解释产生NO的原因________________________________________
(2)汽车排气管内安装的催化转化器,可使汽车尾气中的主要污染物转化为无毒的大气循环物质。已知:
N2(g)+O2(g)===2NO(g) ΔH=+180.5 kJ・mol-1
2C(s)+O2(g)===2CO(g) ΔH=-221.0 kJ・mol-1
C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ・mol-1
则反应2NO(g)+2CO(g)
参考答案:
本题解析:
本题难度:困难
4、选择题 X、Y、Z、W有如图所示的转化关系,且△H=△H1+△H2,则X、Y可能是( )
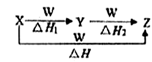
①C、CO ②S、SO2 ③AlCl3、Al(OH)3 ④Na2CO3、NaHCO3
⑤Fe、FeCl2
A.①②③④⑤ B.②④⑤ C.①③④ D.①②③
参考答案:C
本题解析:无机物之间的转化关系要熟练,已知X与W连续反应最终能生成Z,可分析如下:①C与少量O2反应生成CO,CO又可以与O2反应生成CO2,而C与过量O2反应生成CO2,所以符合题意;②S与少量O2反应生成SO2,SO2又可以与O2反应生成SO3,而S与过量O2反应还是生成SO2,不会得到SO3,所以不符合题意;③AlCl3与少量NaOH反应生成Al(OH)3,Al(OH)3又可以与NaOH反应生成NaAlO2,而AlCl3与过量NaOH反应生成NaAlO2,符合题意;④Na2CO3与少量HCl反应生成NaHCO3,NaHCO3又可以与HCl反应生成NaCl,而Na2CO3与过量HCl反应生成NaCl,符合题意;⑤Fe与HCl(或Cl2)反应生成FeCl2(FeCl3),但是FeCl2(FeCl3)不能与HCl(Cl2)再反应,所以不符合题意。
考点:无机物之间的相互转化,常见物质的化学反应要熟练
点评:只要熟记常见物质的性质和相关化学反应,此题可迎刃而解。
本题难度:一般
5、填空题 (12分)氮及其化合物在工农业生产、生活中有着重要作用。
(1)下图是N2(g)和H2(g)反应生成1mol NH3(g)过程中能量变化示意图,请写出N2和H2反应的热化学方程式 。

(2)已知:H-H、N≡N键能分别为435kJ・mol-1、943kJ・mol-1,则结合(1)图中数据,计算N-H的键能 kJ・mol-1。
(3)已知:N2(g)+2O2(g) N2O4(l);△H1=" -19.5" kJ・mol-1;
N2H4(l)+O2(g) N2(g)+2H2O(g) ;△H2=" -534.2" kJ・mol-1
肼(N2H4)与氧化剂N2O4反应生成N2和水蒸气。写出该反应的热化学方程式 。
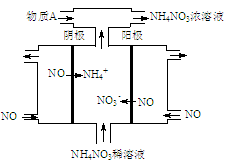
(4)工业上可电解NO制备NH4NO3,其工作原理如图所示,该阳极发生的电极反应式为 。为使电解产物全部转化为5mol NH4NO3,需补充的物质是 (填化学式),此时电子转移的物质的量为 mol。
参考答案:(1)N2(g) + 3H2(g) 2NH3(g) △H= -92kJ/mol 2NH3(g) △H= -92kJ/mol
(2)390 (3)2N2H4(l)+N2O4(l)= 3N2(g) + 4H2O(g) △H= -1048.9 kJ/mol
(4)NO-3e-+2H2O=NO3-+4H+ 氨气 15
本题解析:(1)根据图示,反应热为E1-E2=254-300=92kJ/mol,所以热化学方程式写成:N2(g) + 3H2(g) 2NH3(g) △H= -92kJ/mol(2)根据反应热=反应物的键能总和-生成物的键能总和计算,-92=943+3×435-6x, x=390kJ・mol-1。(3)将方程式标记为①和②,根据盖斯定律,②×2-①,计算反应热=-534.2×2+19.5=-1048.9 kJ/mol。(4)阳极反应是一氧化氮失去电子变成了硝酸根离子,即为NO-3e-+2H2O=NO3-+4H+,总反应为8 NO+2NH3+7H2O=5NH4NO3,所以为使电解产物全部转化为5mol NH4NO3,需补充的物质是氨气,此时电子转移的物质的量为15mol。 2NH3(g) △H= -92kJ/mol(2)根据反应热=反应物的键能总和-生成物的键能总和计算,-92=943+3×435-6x, x=390kJ・mol-1。(3)将方程式标记为①和②,根据盖斯定律,②×2-①,计算反应热=-534.2×2+19.5=-1048.9 kJ/mol。(4)阳极反应是一氧化氮失去电子变成了硝酸根离子,即为NO-3e-+2H2O=NO3-+4H+,总反应为8 NO+2NH3+7H2O=5NH4NO3,所以为使电解产物全部转化为5mol NH4NO3,需补充的物质是氨气,此时电子转移的物质的量为15mol。
考点:热化学方程式的书写,电解原理的应用。
本题难度:一般
|  (CO)=_____;
(CO)=_____;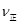 ___________
___________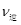 (填“>”或“<”),平衡向__________方向移动(填“正反应”、“逆反应”“不移动”)
(填“>”或“<”),平衡向__________方向移动(填“正反应”、“逆反应”“不移动”)