��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��1��ij�������ṹ��ͼ��ʾ�����ķ���ʽΪ______��һ�ȴ�����______�֣�
��2����CH3CH2��2C��CH3��2��ϵͳ����Ϊ______��
��3��ij��������̼��������Ϊ6��1����ʵ��ʽΪ______���ֲ�øû����������������ܶ�Ϊ14���û�����ķ���ʽΪ______��
��4��д��3P�����1��δ�ɶԵ��ӵ�Ԫ�ط��ţ�______��
�ο��𰸣���1��

�ķ���ʽΪC18H14�����ݵ�Ч�ⷨ����ͬһ̼ԭ���ϵ���ԭ�ӵ�Ч����ͬһ̼ԭ��������-CH3�ϵ���ԭ�ӵ�Ч���۴��ڶԳ�λ���ϵ�̼ԭ���ϵ���ԭ�ӵ�Ч����4����ԭ�Ӿ�������һ�ȴ���ʴ�Ϊ��C18H14��4��
��2����CH3CH2��2C��CH3��2��ϵͳ������ѡȡ�����̼ԭ�ӵ�Ϊ��̼���������������̼ԭ�ӣ�����ȡ���������һ�����ţ�д�����ƣ�3��3-�������飬
�ʴ�Ϊ��3��3-�������飻
��3��̼��������Ϊ6��1��̼��ԭ�Ӹ��������������Ϊ1��2��
�û����������������ܶ�Ϊ14����û�����ķ�������14��2=28����û�����Ļ�ѧʽΪCxHy��
12x��y=6��1
12x+y=28
��ã�x=2��y=4��
��˸û�����Ļ�ѧʽΪC2H4��
�ʴ�Ϊ��CH2��C2H4��
��4��p�ܼ���3�������3p�������1��δ�ɶԵ��ӣ���3p�ܼ�Ϊ3p5���������Ų�ʽΪ1s22s22p63s23p5����ΪCl���ʴ�Ϊ��Cl��
���������
�����Ѷȣ�һ��
2��ѡ���� �����й�ԭ�Ӻ�����ӵ�˵��������ǣ�������
A���ں��ж�����ӵ�ԭ������ӷֱ���������ͬ���������˶�
B���������Ǿ����ܵ��ȴ��ڲ����𣬵�һ��������������һ��
C��ÿ�����Ӳ���Ϊ�����ʱ����������8������
D����ԭ�Ӻ˽��ĵ��������ͣ���ԭ�Ӻ�Զ�ĵ���������
�ο��𰸣�C
���������
�����Ѷȣ�һ��
3��ѡ���� �����ܲ��У���f�ܼ����ǡ�
[? ]
A��K
B��L
C��M
D��N
�ο��𰸣�D
���������
�����Ѷȣ���
4������� ԭ��������С�������е����ֶ�����Ԫ��X��Y��Z��W������Ԫ�ص�ԭ������֮��Ϊ32�������ڱ���X��ԭ�Ӱ뾶��С��Ԫ�أ�Y��Z�������ڣ�Z��Wλ��ͬ���壮
��1��WԪ�������ڱ��е�λ��Ϊ______��д��YԪ��ԭ�ӵļ۵����Ų�ʽ��______��
��2����X��Z��Ԫ�ؿ������A��B���ֻ����A��һ�������¿��Էֽ��B��A�ķ�������______������ԡ������Ǽ��ԡ������ӣ�
��3��һ�������£�Y�ĵ���������X�ĵ��������ַ�Ӧ����6.8g?C���壨��֪n��X����n��Y��=3��1���ɷų�18.44kJ��������÷�Ӧ���Ȼ�ѧ����ʽΪ______��
��4����X��Y��Z��W����Ԫ����ɵ�һ�����ӻ�����D
����֪1mol?D��������NaOHŨ��Һ��Ӧ���ɱ�״����44.8L���壮д������������D��NaOH��Һ��Ӧ�����ӷ���ʽ______��
����֪D���������ᷴӦ����������ˮ��Ӧ��д��D����ˮ��Ӧ�����ӷ���ʽ______��
��5?��X�ĵ�����Z�ĵ�����KOH��Ũ��Һ�п����γ�ԭ��أ�����Խ���M�ͽ���NΪ���Ե缫���ڵ�ص�M��ͨ��X�ĵ������壬N��ͨ��Z�ĵ������壬��M���ĵ缫��ӦʽΪ______��
�ο��𰸣�ԭ��������С�������е����ֶ�����Ԫ��X��Y��Z��W������Ԫ�ص�ԭ������֮��Ϊ32�������ڱ���X��ԭ�Ӱ뾶��С��Ԫ�أ���XΪ��Ԫ�أ�Y��Z�������ڣ�Z��Wλ��ͬ���壬ԭ������Y��Z��W�������ߵ����λ��Ϊ
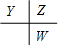
����Y��ԭ������Ϊa����Z��ԭ������Ϊa+1��W��ԭ������Ϊa+9������a+a+1+a+9=32-1�����a=7����XΪ��Ԫ�أ�YΪ��Ԫ�أ�ZΪ��Ԫ�أ�WΪ��Ԫ�أ�
��1��WΪ��Ԫ�أ�ԭ�Ӻ�����16�����ӣ���3�����Ӳ㣬����������Ϊ6��λ�����ڱ��е������ڵ�V��A�壻?YΪ��Ԫ�أ�ԭ�Ӻ�����7�����ӣ���������Ų�ʽΪ1S22S22P3����ԭ�Ӽ۵����Ų�ʽ?2S22P3��
�ʴ�Ϊ���������ڵ�V��A�壻?2S22P3��
��2��XΪ��Ԫ�أ�YΪ��Ԫ�أ���X��Z��Ԫ�ؿ������A��B���ֻ����A��һ�������¿��Էֽ��B����AΪN2H4��BΪNH3��N2H4�����е�ԭ���뵪ԭ��֮���γ�N-N������ÿ��Nԭ�ӻ��γ�2��N-H����Nԭ����1�Թ¶Ե��Ӷԣ�Nԭ�ӵ��ӻ������Ϊ4��Nԭ�Ӳ�ȡsp3�ӻ���������������-NH2�ֱ�λ�����ƴ���ҳ��ҳ���ڣ�������������ƣ����Ӳ��Գƣ�Ϊ���Է��ӣ�
�ʴ�Ϊ�����ԣ�
��3��XΪ��Ԫ�أ�YΪ��Ԫ�أ�һ�������£�Y�ĵ���������X�ĵ��������ַ�Ӧ����6.8g?C���壬�ɷų�18.44kJ������CΪNH3��6.8gNH3�����ʵ���Ϊ6.8g17g/mol=0.4mol����������2molNH3���ų�������Ϊ18.44kJ��2mol0.4mol=92.2kJ����÷�Ӧ���Ȼ�ѧ����ʽΪN2��g��+3H2��g��?

?2NH3?��g����H=-92.2?kJ/mol��
�ʴ�Ϊ��N2��g��+3H2��g��?

?2NH3?��g����H=-92.2?kJ/mol��
��4����X��Y��Z��W����Ԫ����ɵ�һ�����ӻ�����D����DΪ�����γɵ���λ��������γɵ���Σ�
��DΪ�����γɵ���λ��������γɵ���Σ�1mol?D��������NaOHŨ��Һ��Ӧ���ɱ�״����44.8L���壬������Ϊ���������ʵ���Ϊ2mol����DΪ����炙�������泥�����������D��NaOH��Һ��Ӧ�����ӷ���ʽΪNH4++OH-??��?.?H2O+NH3����
�ʴ�Ϊ��NH4++OH-??��?.?H2O+NH3����
��D���������ᷴӦ����������ˮ��Ӧ����Ϣٿ�֪DΪ������泥�Cl2��SO32-����ΪSO42-����������ԭΪCl-��
��Ӧ�����ӷ���ʽΪSO32-+Cl2+H2O�TSO42-+2Cl-+2H+��
�ʴ�Ϊ��SO32-+Cl2+H2O�TSO42-+2Cl-+2H+��
��5?��������������KOH��Ũ��Һ�п����γ�ԭ��أ�����Խ���M�ͽ���NΪ���Ե缫���ڵ�ص�M��ͨ��X�ĵ������壬N��ͨ��Z�ĵ������壬ԭ��ظ�������������Ӧ���������ڸ����ŵ磬������Ӧ��ԭ��Ӧ���������������ŵ磬����M��ͨ������N��ͨ���������������£������ŵ�����ˮ����M���ĵ缫��ӦʽΪ H2+2OH--2e-�T2?H2O��
�ʴ�Ϊ��H2+2OH--2e-�T2?H2O��
���������
�����Ѷȣ�һ��
5��ѡ���� ��ԭ�ӵĵ�����ͼ�е�С�ڵ��ʾ��������
[? ]
A��һ��С�ڵ��ʾһ������
B���ڵ�Ķ��ٱ�ʾ���Ӹ����Ķ���
C����ʾ�����˶��Ĺ켣
D�������ں���ռ���ֻ���Ķ���
�ο��𰸣�D
���������
�����Ѷȣ���