��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��������ЧӦ����Դ��ȱ�����⣬��ν��ʹ����е�CO2���������Կ������ã������˸�����ձ����ӡ�Ŀǰ��ҵ����һ�ַ�������CO2����ȼ�ϼ״���һ�������·�����Ӧ��CO2(g)��3H2(g)  CH3OH(g)��H2O(g)���÷�Ӧ�������仯��ͼ��ʾ��
CH3OH(g)��H2O(g)���÷�Ӧ�������仯��ͼ��ʾ��
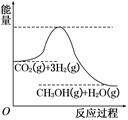
(1)������Ӧƽ�ⳣ��K�ı���ʽΪ?���¶Ƚ��ͣ�ƽ�ⳣ��K?(����������䡱��С��)��
(2)�����Ϊ2 L���ܱ������У�����1 mol CO2��3 mol H2�����CO2�����ʵ�����ʱ��仯���±���ʾ���ӷ�Ӧ��ʼ��5 minĩ��������Ũ�ȱ仯��ʾ��ƽ����Ӧ����v(H2)��?��
t/min
| 0
| 2
| 5
| 10
| 15
|
n(CO2)/mol
| 1
| 0.75
| 0.5
| 0.25
| 0.25
|
?
(3)����������ʹ������Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ�����?(��д�����ĸ)
a����ʱ�����CH3OH����
b���ʵ������¶�
c�������������ݻ����䣬�ٳ���1 mol CO2��3 mol? H2
d��ѡ���Ч����
�ο��𰸣�(1) 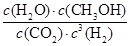 ?����
?����
(2)0.15 mol��L��1��min��1
(3)c
���������(1)�÷�Ӧ������ȷ�Ӧ�������ͣ��Ƿ��ȷ�Ӧ���¶Ƚ��ͣ�ƽ�������ƶ���Kֵ����
(2)v(H2)��3v(CO2)��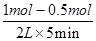 ��3
��3
��0.15 mol��L��1��min��1��
(3)��ʱ������״������ʹƽ�������ƶ�������Ӧ���ʼ�С�������¶Ȼ�ʹ��Ӧ��������ƽ�������ƶ���ѡ���Ч�Ĵ�����ӿ췴Ӧ���ʣ���ƽ�ⲻ�ƶ��������������ݻ����䣬�ٳ���1 mol CO2��3 mol H2����Ч����ԭƽ��Ļ���������ѹǿ����ѧ��Ӧ��������ƽ�������ƶ���
�����Ѷȣ�һ��
2��ѡ���� ij�¶���2L�ܱ������У�3��������ʼ״̬��ƽ��״̬ʱ�����ʵ�����n�������ʾ������˵����ȷ���ǣ�������
| ? | X | Y | W
����ʼ״̬��/mol
2
1
0
��ƽ��״̬��/mol
1
0.5
1.5
|
A�����¶��£��˷�Ӧ��ƽ�ⳣ������ʽ��K=
B�������¶ȣ���W�����������С����˷�Ӧ��H��0
C������ѹǿ�������淴Ӧ���ʾ�����ƽ��������Ӧ�����ƶ�
D�����¶��£�����������ͨ��3molW���ﵽƽ��ʱ��n��X��=2mol
�ο��𰸣����������ݿ�֪��Ӧ�Ļ�ѧ����ʽΪ2X��g��+Y��g��

3W��g������
A�����¶��£��˷�Ӧ��ƽ�ⳣ������ʽ��K=c3(W)c2(X)��c(Y)����A����
B�������¶ȣ���W�����������С��˵��ƽ�����淴Ӧ�����ƶ�����˷�Ӧ��H��0����B����
C����Ӧǰ�������������䣬��ѹǿ��ƽ���ƶ�û��Ӱ�죬��C����
D����Ӧǰ�������������䣬��ѹǿ��ƽ���ƶ�û��Ӱ�죬���¶��£�����������ͨ��3molW���ﵽƽ��ʱ��Ч�ڼ���4molX��2molY��ƽ��״̬��ͬ�������ʵĺ�����ͬ����ﵽƽ��ʱ��n��X��=2mol����D��ȷ��
��ѡD��
���������
�����Ѷȣ�һ��
3������� ��ҵ�����÷�Ӧ:CO(g)+H2O(g) 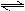 ?CO2(g)+H2(g)����H="Q" kJ��mol-1,�Ʊ�H2 .��֪�÷�Ӧ��ƽ�ⳣ��K���¶ȵĹ�ϵ��ͼ��ʾ��
?CO2(g)+H2(g)����H="Q" kJ��mol-1,�Ʊ�H2 .��֪�÷�Ӧ��ƽ�ⳣ��K���¶ȵĹ�ϵ��ͼ��ʾ��

����һ�ݻ��̶����� ��������,��850��ʱ����������Ӧ,����������ڸ����ʵ�Ũ��(mol��L�D1)��ʱ��ı仯��ϵ���±�:
��������,��850��ʱ����������Ӧ,����������ڸ����ʵ�Ũ��(mol��L�D1)��ʱ��ı仯��ϵ���±�:
t/min
| CO(g)
| H2O(g)
| CO2(g)
| H2(g)
|
0
| 0.200
| 0.300
| 0
| 0
|
2
| 0.138
| 0.238
| 0.062
| 0.062
|
3
| c1
| c2
| c3
| c4
|
4
| c1
| c2
| c3
| c4
|
?
��֪:850��ʱ�÷�Ӧ�Ļ�ѧƽ�ⳣ��K=1.0,��ش���������:
(1)���п����жϸ÷�Ӧ�ﵽ��ѧƽ��״̬����_______.
A.�� λʱ���ڼ���CO(g)��Ũ�ȵ�������CO2(g)��Ũ��
λʱ���ڼ���CO(g)��Ũ�ȵ�������CO2(g)��Ũ��
B.��Ӧ�����ڵ�ѹǿ�������仯
C.���������H2(g)��Ũ�Ȳ��ٷ����ı�
D.�������������ʵ���ˮ����������
(2)Q______0(���������=������).
(3)����850��ʱ��Ӧ�����г���H2O(g),Kֵ___ __(���������С�����䡱).
__(���������С�����䡱).
(4)��ƽ��ʱCO2�ķ�Ӧ����______,CO(g)��ת����Ϊ_______.
�ο��𰸣���1��C��2������3�����䣨4��0.04 mol/(L?min)?��? 60
�����������
�����Ѷȣ�һ��
4��ѡ���� ij�¶��£�N2O4��g�� 2 NO2��g������H��0�����ܱ������дﵽƽ�⣬����˵������ȷ����?
2 NO2��g������H��0�����ܱ������дﵽƽ�⣬����˵������ȷ����?
A����ѹʱ����С���������ʹ�����淴Ӧ��������ƽ�����淴Ӧ�����ƶ�
B������������䣬��������NO2����ʹ����Ӧ���ʼ�С���淴Ӧ��������ƽ�����淴Ӧ����
C������������䣬��������N2O4���ٴﵽƽ��ʱ����ɫ����
D������������䣬�����¶ȣ��ٴ�ƽ��ʱ��ɫ����
�ο��𰸣�B
���������
�𰸣�B
B�б���������䣬��������NO2����ʹ����Ӧ���������淴Ӧ����Ҳ����ƽ�����淴Ӧ����
A����ѹ��ƽ���������С���淽���ƶ�
C?�൱����С�������ϵNO2Ũ�������ٴﵽƽ��ʱ����ɫ����
D�������¶ȣ�ƽ�������ȷ����ƶ��������������ƶ����ٴ�ƽ��ʱ��ɫ����
�����Ѷȣ���
5�������� ��һ�������£���һ����PCl5(g)ͨ���ܱ������У�������ӦPCl5(g)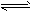 PCl3(g)��Cl2(g)�����ﵽƽ��ʱ��������������H2���ܶ�Ϊ74.5����PCl3(g)��ƽ������������ռ��������ǣ�����������̡�
PCl3(g)��Cl2(g)�����ﵽƽ��ʱ��������������H2���ܶ�Ϊ74.5����PCl3(g)��ƽ������������ռ��������ǣ�����������̡�
�ο��𰸣��⣺����ʼʱͨ��PCl5(g)�����ʵ���Ϊ1 mol���ﵽƽ��ʱ����PCl5(g)�����ʵ���Ϊx���� 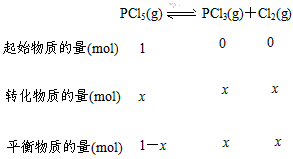 ƽ��ʱ�����ʵ���Ϊ(1mol��x)��x��x��1 mol��x���������ƽ���������ƽ��Ħ������
ƽ��ʱ�����ʵ���Ϊ(1mol��x)��x��x��1 mol��x���������ƽ���������ƽ��Ħ������
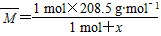 ��74.5��2 g��mol-1��
��74.5��2 g��mol-1��
���x��0.40 mol��
��PCl3(g)��ƽ������������ռ�������Ϊ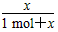 ��100%��
��100%��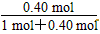 ��100%��28.6%
��100%��28.6%
���������
�����Ѷȣ�һ��