|
|
|
�߿���ѧ֪ʶ����ɡ���ɫ��ѧ����Ƶ����ǿ����ϰ��2017�����°棩(ʮ)
2017-08-10 01:36:01
��Դ:91������
����:www.91exam.org �� �� �� ��
|
��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� I��Ŀǰ���ҹ����á��Ӵ����������ᣬ�豸��ͼ��ʾ��

��1��ͼ���豸A��������_____________?���豸����Ҫ��Ӧ�Ļ�ѧ����ʽΪ?��
��2���йؽӴ��������������˵���У�����ȷ����______________��
A����������ĽӴ������ڽӴ����з���

B����������Ũ��Ϊ98.3%Ũ����������������
C�����պ���48%�Ļ�����ʱ����FeS2��ʧ��2%����S��ʧ2%
D��Bװ���з�Ӧ������֮һΪ�ϸ��¶���Ϊ�����SO2��ת����
| E�����Ṥҵ���ڽӴ��Ұ�װ�Ƚ�������Ϊ������SO3ת��ΪH2SO4ʱ�ų�������
��3�����й����߿������Ʊ�SO2�����õ绯ѧԭ����������ķ�����װ����ͼ��Ϊ���ȶ����������������Ũ��Ӧά�ֲ��䣬��ͨ���SO2��ˮ��������Ϊ?��
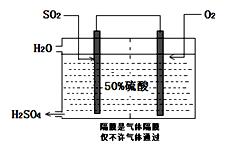
II. ������һ����Ҫ�Ļ���ԭ�ϡ�Ŀǰ�Ƽҵ��Ҫ�� ��������͡������Ƽ�����ֹ��ա��밴Ҫ��ش����⣺
��1�����������������CaCl2�������д���ù����в���CaCl2�Ļ�ѧ����ʽ��?��
��2��д���������Ƽ���йط�Ӧ�Ļ�ѧ����ʽ��?��
?��
��3��CO2���Ƽҵ����Ҫԭ�ϣ��������Ƽ����CO2����Դ��?��
�� �������CO2��Դ��?�� �������CO2��Դ��?��
�ο��𰸣���1������¯ ��1�֣���4FeS2 +11O2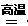 ?2Fe2O3 + 8SO2��2�֣� ?2Fe2O3 + 8SO2��2�֣�
��2��D E��2�֡����ֱ�ͬǰ��?��3��16�s29 ��2�֣�
��1��2NH4Cl + Ca(OH)2 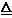 ?CaCl2 + 2NH3��+ 2H2O ��2�֣� ?CaCl2 + 2NH3��+ 2H2O ��2�֣�
��2��NH3 + H2O + CO2 + NaCl�����ͣ� �� NaHCO3��+ NH4Cl��2�֣�
2NaHCO3 ?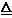 Na2CO3 + CO2��+ H2O?��2��) Na2CO3 + CO2��+ H2O?��2��)
��3���ϳɰ�����1�֣� ������ʯ��ʯ��1�֣�
�����������
�����Ѷȣ�һ��
2������� ��14�֣���ͭ��CuFeS2������ȡͭ���仯�������Ҫԭ��֮һ���������Ʊ������Ļ����
(1)?ұ��ͭ�ķ�ӦΪ
8CuFeS2 + 21O2 8Cu + 4FeO + 2Fe2O3 + 16SO2
��CuFeS2��Fe�Ļ��ϼ�Ϊ+2����Ӧ�б���ԭ��Ԫ����_________����Ԫ�ط��ţ���
(2)?����ұ�����̲�������SO2�����д��������к�������__________������ţ���
a.?�߿��ŷ�? b.�����Ʊ�����
c.?�ô�����Һ������Na2SO4? d.��Ũ��������
(3)?��������أ�K2S2O8������ǿ�����ԣ��ɽ�I?����ΪI2��S2O82? + 2I? �� 2SO42? + I2��ͨ���ı䷴Ӧ;����Fe3+��Fe2+���ɴ�������Ӧ���������ӷ���ʽ��ʾFe3+��������Ӧ���Ĺ��̣�__________��__________��
(4)?���û�ͭ��ұ��ͭ������¯������Fe2O3��FeO��SiO2��Al2O3�����Ʊ�Fe2O3������Ϊ��
����ϡ�����ȡ¯�������ˣ�����Һ���������ټ������NaOH��Һ�����ˣ�������ϴ�ӡ�������յ�Fe2O3��
a.?��ȥAl3+ �����ӷ���ʽ��____________________________��
b.?ѡ���ṩ���Լ������ʵ����֤¯���к���FeO��
�ṩ���Լ���ϡ����?ϡ����? KSCN��Һ? KMnO4��Һ? NaOH��Һ?��ˮ
��ѡ�Լ�Ϊ__________��֤��¯���к���FeO��ʵ������Ϊ____________________��
�ο��𰸣�(1)? Cu��O? 2��? (2)? b��c? 2��
(3)?��2Fe3+ + 2I? �� I2 + 2Fe2+?2��?��2Fe2+ + S2O82? �� 2Fe3+ + 2SO42?2��
(4) a.? Al3+ + 4OH? �� AlO2? + 2H2O?2��
b.?ϡ���ᡢKMnO4��Һ?2��
��ϡ�����ȡ¯����������Һ������KMnO4��Һ��Ӧ������Һ��ɫ��֤������?2��
�����������1�����ݷ���ʽ��֪�����������������õ����ӣ���˱���ԭ��Ԫ������Ԫ�ء�CuFeS2��ͭԪ�صĻ��ϼ��ǣ�2�ۣ������������е���ͭ���ɣ����Ա���ԭ��Ԫ�ػ���ͭ��
��2��SO2��һ������������������Ʊ����ᣬb��ȷ��SO2����һ�ִ�����Ⱦ��������ⶪ����a����ȷ��c��ȷ��Ũ�����ϡ��SO2��d����ȷ����ѡbc��
��3���������ܰѵ������������ɵ��ʵ⣬����һ�������£���S2O82?���ܰ����������������������ӣ�����ʽΪ2Fe3+ + 2I? �� I2 + 2Fe2+��2Fe2+ + S2O82? �� 2Fe3+ + 2SO42?��
��4��������������������������������������������У����Է���ʽΪAl3+ + 4OH?�� AlO2? + 2H2O��
����Ϊ�����������л�ԭ�ԣ������Ը��������Һ�־��������ԣ�����������ʹ���Ը��������Һ��ɫ���ݴ˿��Լ��飬����ѡ����Լ���ϡ���ᡢKMnO4��Һ��ʵ����������ϡ�����ȡ¯����������Һ������KMnO4��Һ��Ӧ������Һ��ɫ��֤�����ڡ�
�����Ѷȣ�һ��
3��ѡ���� ��ʶ��Ӧ�����Ի�ѧ��Ӧ��Ӱ�죬��ѧ�û�������֪ʶ������Ҫ���塣����˵������ȷ����? (����)��
A��SO2�ϳ�SO3��Ȼ���ڷ��ȷ�Ӧ������ҵ�Ϻϳ�SO3ʱ�������
B���ϳɰ���ҵ���ø��¸�ѹ��ʹ�ô���������Щ���������ϻ�ѧƽ��ԭ��
C���ϳɴ���Ĺ����У�Ӧ������ʳ��ˮ��ͨ��NH3����ͨ������CO2
D��ͨ����ѹ���µķ����ɻ���Ʊ�NH3��ԭ����N2
�ο��𰸣�B
����������ϳɰ���Ӧ�Ƿ��ȷ�Ӧ���ӻ�ѧƽ��ĽǶȷ��������¸������ںϳɰ���B���ȷ��
�����Ѷȣ�һ��
4������� ��1�����й��ڹ�ҵ����˵����ȷ����?��������ţ�
A���ں����Ƽҵ�У����Ȼ�����Һ����ͨ������̼����ͨ����
B�������Ṥҵ���ϳɰ���ҵ�����Ṥҵ�У��Բ���ѭ���������ԭ��������
C�����ȼҵ�����۱����ӽ���Ĥ���������Һ�������
D����ҵ�ϲ��õ�������Ȼ����ķ�����ȡ������
|
E��ʯ���ѻ����ڻ�ѧ�仯����ҪĿ����Ϊ�˻�ö�����������̬��
��2���ҹ��涨����ˮ�������涨��������±���Ҫ��
pH
| Ca2+?��Mg2+��Ũ��
| ϸ������
|
6.5��8.5
| �� 0.004 5 mol��L-1?
| ��100����mL-1?
|
?
������ԭˮ����������ˮ�Ĺ�������ʾ��ͼ��

��ԭˮ�к�Ca2+?��Mg2+?��HCO3-��Cl-�ȣ�����ʯ������Ca(OH)2�������������ɸ��ֽⷴӦ��д�����е����ӷ���ʽ��ֻҪ��д����������
?��
?��
��FeSO4��7H2O�dz��õ����ۼ�������ˮ����������
?������ͨ�������̼��Ŀ����
?��
?��
������A��������
?������������
?������Ϊ����A�Ĵ���Ʒ�����ţ���
a��ClO2 ?b��Ũ��ˮ? c��K2FeO4? d��SO2? e.Ư��
�ο��𰸣���15�֣���1��BC��2�֣���2����HCO3��+OH-=CO32��+H2O,? Mg2+ +2OH-=Mg(OH)2��
Ca2+ + HCO3��+OH-=CaCO3��+H2O ����ѡ�������������д��Ҳ�ԣ�ÿ��2��)
�ڽ�״Fe(OH)3?��2�֣��� ��ȥCa2+?��?����pH?��ÿ��2�֣�
��ɱ������?��1�֣� ��? a c e?��2�֣�
�����������1��A����Ϊ�����ܽ�ȷdz�����ͨ������ͨ������̼�������������̼�����գ����������ɴ����A����ȷ��
B����ѧ��Ӧ�����ѭ�����ÿ������ԭ�������ʣ���B��ȷ��
C����ⱥ��ʳ��ˮʱ���������ϲ��������������������ƣ��������ϲ��������������������ӽ���Ĥ�����ɷ�ֹ�����Ҳ�����C12���������ң�����ѡ��C��ȷ��
D���Ȼ����ǹ��ۻ��������ʱ���ܵ��磬���Թ�ҵ�ϲ��õ�������������ķ�����ȡ��������D����ȷ��
E��ʯ���ѻ����ڻ�ѧ�仯����ҪĿ����Ϊ��������͵IJ�����������E����ȷ����ѡBC��
��2��������������ǿ��ܺ��Ȼ�þ��Ӧ�����Ȼ��ƺ�������þ��������ѧ��Ӧ�����ӷ���ʽ��Mg2+ +2OH-=Mg(OH)2������������Ҳ�ܺ�HCO3����Ӧ����CO32������������̼��Ƴ�������Ӧ�����ӷ���ʽ��HCO3��+OH-=CO32��+H2O��Ca2+ + HCO3��+OH-=CaCO3��+H2O��
���������Ӿ��л�ԭ�ԣ��ױ��������������ӣ�������ˮ�����������������壬����FeSO4��7H2O��ˮ���������ɽ�״Fe(OH)3������CO2�������������Ӧ���������ƹ���������ͨ��CO2��Ŀ���dz�ȥ������Ca2+�͵�����Һ��pH��
������A��������ɱ�����������о���ǿ�����Ե�������ClO2 ��K2FeO4��Ư�ۣ����Կ��Դ���A����������ѡ��ace��
�����Ѷȣ�һ��
5��ѡ���� ��ɫ����������Ҳ�����ǵ������������ʵ����ϡ���ɫ������˼�����
[? ]
A����������ˮ����ˮ 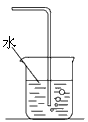
B��ͭ��Ũ���ᷴӦ 
C��ʵ�����Ʊ����ռ��Ȼ������� 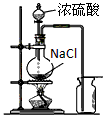
D��һ����̼��ԭ����ͭ 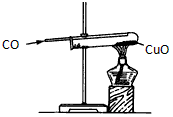
�ο��𰸣�B
���������
�����Ѷȣ�һ��

 �������CO2��Դ��?��
�������CO2��Դ��?��



