微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (14分)硫酸工业中2SO2(g)+O2(g)催化剂△2SO3(g);ΔH<0(放热反应)有关实验数据如下:
  压强 压强
SO2的
转化率
温度
| 1×105 Pa
| 5×105 Pa
| 10×105 Pa
| 50×105 Pa
| 100×105 Pa
|
450 ℃
| 97.5%
| 98.9%
| 99.2%
| 99.6%
| 99.7%
|
550 ℃
| 85.6%
| 92.9%
| 94.9%
| 97.7%
| 98.3%
|
(1)在生产中常用过量 的空气是为了________。
的空气是为了________。
(2)高温对该反应有何影响?________,实际生产中采用400~500 ℃的温度除了考虑速率因素外,还考虑到________。
(3)增大压强对上述反应有何影响?____,但工业上又常采用常压进行反应,其原因是______________。
(4)常用浓H2SO4而不用水吸收SO3是由于___ ___,尾气中SO2必须回收,主要是为了________。
参考答案:(14分) (1)使平衡正向移动,提高SO2的转化率
(2)高温使反应速率加快,缩短了达到平衡所需的时间,但是对SO2的转化不利 。
催化剂在该温度下活性最强,催化效果最佳。
(3)加快反应速率,且使平衡正向移动,有利于SO2转化和SO3的生成。
常压时SO2的转化率已经很高,无采用高压的必要,况且,采用高压还受动力、设备 等条件的限制,提高了成本。
等条件的限制,提高了成本。
(4)用水吸收SO3易形成酸雾,吸收效果差,而用浓H2SO4吸收则不易形成酸雾,吸收效果好。
防止空气污染。
本题解析:略
本题难度:简单
2、填空题 (l)火法炼锌是将闪锌矿(主要成分是ZnS)通过浮选焙烧使它转化为氧化锌,再把氧化锌和焦?炭混合,在鼓风炉中加热到1100~1300℃,使锌蒸馏出来。
①写出火法炼锌的主要反应:
焙烧反应:?。
鼓风炉中可能发生的反应:?(任写一个)
②从保护环境和充分利用原料角度看如何处理和利用产生的烟气?
?
(2)工业上冶炼铝就是电解氧化铝
①冶炼铝的电解槽中的阴极和阳极材料均用石油炼制和煤的干馏产品?(填物质名称)
②氧化铝的熔点很高,在铝的冶炼中要加入冰晶石(Na3AlF),其作用是____?。
③工业上冶炼铝时用的原料是Al2O3,而不是AlCl3,其原因是?。
(3)工业上“联合制碱法”中主要反应的化学方程式是?。其中的CO2来源于?。
(4)磁酸钙是制玻璃的原料之一,工业上制玻璃是在玻璃熔炉中进行,其中反应之一为:
 ,若在上述条件下,把l000ag CaCO3和60ag SiO2混合,则生成的CO2在标准状况下的体积为?(用含a的代数式表示)。
,若在上述条件下,把l000ag CaCO3和60ag SiO2混合,则生成的CO2在标准状况下的体积为?(用含a的代数式表示)。
参考答案:(1)① 2ZnS+3O2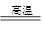 2ZnO+2SO2;2C+O2
2ZnO+2SO2;2C+O2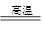 2CO或ZnO+CO
2CO或ZnO+CO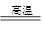 Zn+CO2或2ZnO+C
Zn+CO2或2ZnO+C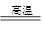 2Zn+CO2
2Zn+CO2
②用氨水吸收烟气中的SO2生成(NH4)2SO3或NH4HSO3,再让(NH4)2SO3或NH4HSO3与硫酸反应产生SO2,收集SO2用于生产硫酸。
(2)①石墨(或碳)②降低Al2O3熔化后温度,节约能量;③Al2O3熔化后能导电,AlCl3是共价化合物,熔化后不导电。
(3)NH3+CO2+H2O+NaCl(饱和)=NaHCO3↓+NH4Cl;2NaHCO3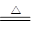 Na2CO3+CO2↑+H2O;合成氨厂。
Na2CO3+CO2↑+H2O;合成氨厂。
(4)22.4a
本题解析:(1)①根据题意“将闪锌矿(主要成分是ZnS)通过浮选焙烧使它转化为氧化锌”反应的化学方程式为2ZnS+3O2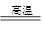 2ZnO+2SO2;根据题意“再把氧化锌和焦?炭混合,在鼓风炉中加热到1100~1300℃,使锌蒸馏出来”可能发生的反应就有:2C+O2
2ZnO+2SO2;根据题意“再把氧化锌和焦?炭混合,在鼓风炉中加热到1100~1300℃,使锌蒸馏出来”可能发生的反应就有:2C+O2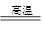 2CO或ZnO+CO
2CO或ZnO+CO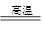 Zn+CO2或2ZnO+C
Zn+CO2或2ZnO+C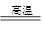 2Zn+CO2
2Zn+CO2
②分析题意,必须“从保护环境和充分利用原料角度”,而且
“如何处理和利用产生的烟气”,故用氨水吸收烟气中的SO2生成(NH4)2SO3或NH4HSO3,再让(NH4)2SO3或NH4HSO3与硫酸反应产生SO2,收集SO2用于生产硫酸。
(2)①电极材料是石墨碳棒;②电解氧化铝用冰晶石作为助熔剂,其目的是降低Al2O3熔化后温度,节约能量。③从本质上来分析,Al2O3是离子化合物,熔融时发生电离,而AlCl3是共价化合物,熔化后不导电。
(3)NH3+CO2+H2O+NaCl(饱和)=NaHCO3↓+NH4Cl;2NaHCO3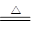 Na2CO3+CO2↑+H2O;合成氨厂。
Na2CO3+CO2↑+H2O;合成氨厂。
(4)CaCO3+SiO2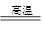 CaSiO3+CO2,据方程式可知CaCO3过量,应用SiO2计算生成CO2的量。
CaSiO3+CO2,据方程式可知CaCO3过量,应用SiO2计算生成CO2的量。
本题难度:一般
3、选择题 以乙烯为原料生产环氧乙烷的方法很多。经典的方法是氯代乙醇法,它包括两步反应:
① CH2=CH2+Cl2+H2O ClCH2CH2OH+HCl
ClCH2CH2OH+HCl
② ClCH2CH2OH+HCl+Ca(OH)2
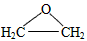 +CaCl2+H2O
+CaCl2+H2O
现代石油化工采用银作催化剂,可以实现一步完成,反应式为: 2CH2=CH2+O2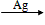
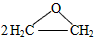
与经典方法相比,现代方法的突出优点是
[? ]
A.所使用的原料没有爆炸的危险
B.符合绿色化学(green chemistry)中的最理想的“原子经剂”(atom economy)
C.对设备的要求较低
D.充分利用了加成反应的原理
参考答案:B
本题解析:
本题难度:简单
4、填空题 随着世界粮食需求量的增加,农业对化学肥料的需求越来越大。氮肥是需求最大的一种化肥。氮肥的生产和合理施用在农业生产中起着重大作用。合成氨及化肥生产流程示意图如下:
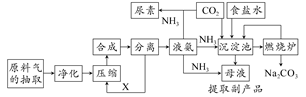
(1)目前,工业上用铁触媒作催化剂,在20~50 MPa、450℃左右用氮、氢混合气体在________中进行合成氨。则沿X方向回去的物质是________。
(2)目前生产尿素是以氨气与CO2为原料,发生反应的化学方程式是________、________。
尿素适用于各种土壤,在土壤中尿素发生水解,其水解的化学方程式是________。
(3)沉淀池中发生反应的化学方程式是________________。
(4)上述生产中的副产品氯化铵长期使用会造成土壤酸化、变硬甚至板结。对土壤的酸碱性进行测定与改良是保护________、提高土壤肥力的有效途径。测定土壤的pH的方法是________。
参考答案:(1)合成塔;H2、N2
(2)2NH3+CO2 NH2COONH4;NH2COONH4
NH2COONH4;NH2COONH4 CO(NH2)2+H2O;CO(NH2)2+H2O=2NH3↑+CO2↑
CO(NH2)2+H2O;CO(NH2)2+H2O=2NH3↑+CO2↑
(3)NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓
(4)土壤资源;取土样于试管中,加5 mL蒸馏水振荡,静置后,取上层清液,用精密pH试纸或pH计测上层清液的pH
本题解析:(1)目前,工业上用铁触媒作催化剂,在20~50 MPa、450°C左右用氮、氢混合气体在合成塔中进行合成氨,沿X方向回去的物质是H2、N2,以循环利用。(2)目前,生产尿素是以氨气与CO2为原料,发生反应的化学方程式是2NH3+CO2 NH2COONH4、NH2COONH4
NH2COONH4、NH2COONH4 CO(NH2)2+H2O。在土壤中尿素发生水解,其水解的化学方程式是CO(NH2)2+H2O=2NH3↑+CO2↑。(3)沉淀池中发生反应的化学方程式是NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓。(4)对土壤的酸碱性进行测定与改良是保护土壤资源、提高土壤肥力的有效途径。测定土壤的pH的方法是:取土样于试管中,加5 mL蒸馏水振荡,静置后,取上层清液,用精密pH试纸或pH计测上层清液的pH。
CO(NH2)2+H2O。在土壤中尿素发生水解,其水解的化学方程式是CO(NH2)2+H2O=2NH3↑+CO2↑。(3)沉淀池中发生反应的化学方程式是NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓。(4)对土壤的酸碱性进行测定与改良是保护土壤资源、提高土壤肥力的有效途径。测定土壤的pH的方法是:取土样于试管中,加5 mL蒸馏水振荡,静置后,取上层清液,用精密pH试纸或pH计测上层清液的pH。
本题难度:一般
5、选择题 “绿色化学”是当今社会提出的一个新概念。在“绿色化学”工艺中,理想状态是反应中原子全部转化为欲制得产物,即原子利用率100%。以下反应最符合绿色化学的是
[? ]
A.CH2=CH2与HCl反应制取CH3CH2Cl
B.CH4与Cl2反应制取CCl4
C.苯与液溴反应制取溴苯
D.乙醇与金属钠反应制取乙醇钠
参考答案:A
本题解析:
本题难度:简单