微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 常温下将0.010molCH3COONa和0.004molHCl溶于水,配制成0.5L混合溶液,判断:
(1)溶液中有两种微粒的物质的量之和一定等于0.010mol,它们是__________和__________;
(2)溶液中n(CH3COO-) + n(OH-) - n(H+) = _____________mol。
参考答案:(1)CH3COO-和CH3COOH
(2)0.006
本题解析:
本题难度:一般
2、填空题 Ⅰ.如图为向25mL0.1mol?L-NaOH溶液中逐滴加入0.2mol?L-醋酸溶液过程中溶液pH的变化曲线,请回答:
(1)有人认为B点时NaOH与CH3COOH恰好完全反应,这种看法是否正确?______(填“是”或“否”).若不正确,则二者恰好完全反应的点是在AB区间还是在BD区间内?______区间.(若正确,此问不答)
(2)在AB区间内,c(OH-)>c(H-),则c(OH-)与c(CH3COO-)的大小关系是______.
A.c(OH-)一定大于c(CH3COO-)?B.c(OH-)一定小于c(CH3COO-)
C.c(OH-)一定等于c(CH3COO-)?D.c(OH-)可能大于、小于或等于c(CH3COO-)
(3)在D点时,溶液中c(CH3COO-)+c(CH3COOH)______2c(Na+).(填“大于”,“小于”或“等于”)
Ⅱ.已知硫酸钡的Ksp为1.0×10-10,碳酸钡的Ksp为2.58×10-9,工业上却可以将硫酸钡转化为碳酸钡,请问至少需要______?mol?L-的碳酸钠溶液浸泡才能实现转化.实现此转化的离子方程式为______.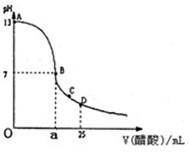
参考答案:Ⅰ、(1)溶液混合后发生的反应为:NaOH+CH3COOH=CH3COONa+H20,当醋酸和氢氧化钠的物质的量之比为1:1时,反应生成的CH3COONa为强碱弱酸盐,溶液显碱性,pH>7,介于AB之间,故答案为:否、AB;
(2)在AB区间内,c(OH-)>c(H-),说明溶液显碱性,当氢氧化钠溶液和醋酸恰好反应是时,显碱性,此时生成的溶液可能为醋酸钠,c(OH-)小于c(CH3COO-);当氢氧化钠溶液和醋酸反应后剩余氢氧化钠溶液,溶液仍然显碱性,此时若剩余的氢氧化钠量很大,则c(OH-)大于c(CH3COO-),也有可能剩余的氢氧化钠和醋酸钠中醋酸根水解之后剩余的醋酸根的浓度相等,故答案为:D;
(3)在D点时,反应后醋酸剩余,溶液的组成为等浓度的醋酸和醋酸钠的混合物,根据物料守恒,此时:c(CH3COO-)+c(CH3COOH)=2c(Na+),故答案为:等于;
Ⅱ、要将硫酸钡转化为碳酸钡,此时在硫酸钡水溶液中,根据硫酸钡的溶度积Ksp=[Ba2+][SO32-]=1.0×10-10,且[Ba2+]=[SO32-],则[Ba2+]=
本题解析:
本题难度:一般
3、填空题 已知在25℃时,0.1mol/L醋酸溶液的pH约为3,向其中加入醋酸钠晶体,等晶体溶解后发现溶液的pH增大。对上述现象有两种不同的解释:
甲同学认为醋酸钠水解溶液呈碱性,增大了c(OH-),因而溶液的pH增大。
乙同学认为醋酸钠溶于水电离出大量的醋酸根离子,抑制了醋酸的电离,使c(H+)减小,因此溶液的pH增大。
(1)上述两种解释中______________(填“甲”或“乙”)正确。
(2)为了验证上述哪种解释正确,继续做如下实验:向0.1mol/L醋酸溶液中加入少量下列物质中的______________(填写编号),然后测定溶液的pH。
A.固体CH3COOK
B.固体CH3COONH4
C.气体NH3
D.固体NaHCO3
(3)若_____________(填“甲”或“乙”)的解释正确,溶液的pH应____________(填“增大”、“减小”或“不变”)(已知25℃时,CH3COONH4溶液呈中性)。
(4)常温下将0.010molCH3COONa和0.004molHCl溶于水,配置成0.5L混合溶液,判断:
①溶液中共有____________种粒子;
②溶液中有两种粒子的物质的量之和一定等于0.010mol,它们是______________和___________;
③溶液中n(CH3COO-)+n(OH-)-n(H+)=____mol。
参考答案:(1)乙
(2)B
(3)乙;增大
(4)①7;②CH3COOH;CH3COO-;③0.006
本题解析:
本题难度:一般
4、选择题 下列溶液中,微粒的物质的量浓度关系正确的是
[? ]
A.1.0mol・L-1的Na2CO3溶液:c(OH-)= c(HCO3-) +c(H+)+2c(H2CO3)
B.1.0mol・L-1的NH4Cl溶液:c(NH4+)= c(Cl-)
C.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+) > c(CH3COO-)> c(H+)> c(OH-)
D.向硝酸钠溶液中滴加稀盐酸,得到pH=1的混合溶液:c(Na+) = c(NO3-)
参考答案:AD
本题解析:
本题难度:一般
5、选择题 下列说法正确的是( )
A.在KI溶液中加入氯化银,一段时间后沉淀变成黄色,说明同温度下K(AgI)<K(AgCl)
B.0.1mol?L-1的NaHCO3溶液:c(H+)+c(H2CO3)=2c(CO2-3)+c(OH-)
C.中和pH与体积都相同的盐酸和醋酸,消耗NaOH的物质的量之比是1:1
D.NaHCO3溶液与NaAlO2溶液混合产生白色沉淀,说明酸性:HCO3-<Al(OH)3
参考答案:A
本题解析:
本题难度:一般