��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��һ�������£������ܱ������н��еķ�Ӧ2SO2��g�� �� O2��g�� 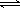 ?2SO3��g��������˵������˵���÷�Ӧ�Ѿ��ﵽ��ѧƽ��״̬����
?2SO3��g��������˵������˵���÷�Ӧ�Ѿ��ﵽ��ѧƽ��״̬����
A��SO2��O2��SO3ͬʱ����
B��SO2��O2��SO3�����ʵ���Ũ�����
C�������淴Ӧ���ʶ�������
D��SO2��O2��SO3�����ʵ���Ũ�Ȳ��ٸı�
�ο��𰸣�D
�����������һ�������£������淴Ӧ������Ӧ���ʺ��淴Ӧ�������ʱ������Ϊ0������Ӧ��ϵ�и������ʵ�Ũ�Ȼ������ٷ����仯��״̬����Ϊ��ѧƽ��״̬������ѡ��C����ȷ��D��ȷ��A�ǿ��淴Ӧ���ص㣬���ʵ�Ũ�Ȳ��ٷ����仯��������֮�䵫Ũ�Ȳ�һ����ȣ�BҲ����ȷ����ѡD��
�����Ѷȣ���
2��ѡ���� ���ݻ��̶����ܱ������г���һ������X��Y�������壬һ�������·������淴Ӧ3X(g)+Y(g)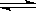 2Z(g)�����ﵽƽ�⡣��֪����Ӧ�Ƿ��ȷ�Ӧ�����X��ת����Ϊ37. 5%��Y��ת����Ϊ25%�������й�������ȷ����
2Z(g)�����ﵽƽ�⡣��֪����Ӧ�Ƿ��ȷ�Ӧ�����X��ת����Ϊ37. 5%��Y��ת����Ϊ25%�������й�������ȷ����
A����X�ķ�Ӧ����Ϊ0.2 mol��L��1��s��1����Z�ķ�Ӧ����Ϊ0.3 mol��L��1��s��1
B�����������г��뺤����ѹǿ����Y��ת�������
C�������¶ȣ�����Ӧ���ʼ�С��ƽ�����淴Ӧ�����ƶ�
D����ʼ���������е�X��Y���ʵ���֮��Ϊ2��1
�ο��𰸣�D
���������A������Ӧ����֮��=��ѧ������֮�ȣ�B��������Ϊ�����壬���뺤����ƽ�ⲻ�ƶ���Y��ת���ʲ��䣻C���������¶Ȼ�ѧ��Ӧ��������D��ȷ��
�����Ѷȣ�һ��
3��ѡ���� I2��KI��Һ�д�������ƽ�⣺I2(aq)��I��(aq) I3��(aq)�� ijI2��KI�����Һ�У� c(I3��)���¶�T�Ĺ�ϵ����ͼ��ʾ���������κ�һ�㶼��ʾƽ��״̬����
I3��(aq)�� ijI2��KI�����Һ�У� c(I3��)���¶�T�Ĺ�ϵ����ͼ��ʾ���������κ�һ�㶼��ʾƽ��״̬����
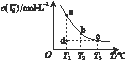
����˵����ȷ����
A����Ӧ I2(aq)��I��(aq) I3��(aq)��H��0
I3��(aq)��H��0
B�����¶�ΪT1��T2����Ӧ��ƽ�ⳣ���ֱ�ΪK1��K2����K2��K1
C����T1ʱ����Ӧ���е�״̬dʱ��һ���Ц��� ������
D��״̬a��״̬b��ȣ�״̬bʱI2��ת���ʸ���
�ο��𰸣�C
���������A����ͼ�����ߵı仯���ƿ�֪�����¶�����ʱ��I3-�����ʵ���Ũ�ȼ�С��˵���÷�Ӧ������ӦΪ���ȷ�Ӧ����ӦI2��aq��+I-��aq�� I3-��aq���ġ�H��0����A����ȷ��B�и÷�Ӧ������ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�����淴Ӧ�����ƶ����¶�Խ�ߣ�ƽ�ⳣ��ԽС�����¶�ΪT1��T2����Ӧ��ƽ�ⳣ���ֱ�ΪK1��K2����K1��K2����B����ȷ��C������Ӧ���е�״̬dʱ����Ӧδ�ﵽƽ��״̬������Ӧ������ƽ�⣬��Ӧ�����ɵ�I3-�����ƶ�����v����v�棬��C��ȷ��D��״̬a��״̬b��ȣ�b״̬�൱����a�Ļ����������¶ȣ�ƽ�����淴Ӧ�����ƶ�����״̬aʱI2��ת���ʸ��ߣ���D����ѡC��
I3-��aq���ġ�H��0����A����ȷ��B�и÷�Ӧ������ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�����淴Ӧ�����ƶ����¶�Խ�ߣ�ƽ�ⳣ��ԽС�����¶�ΪT1��T2����Ӧ��ƽ�ⳣ���ֱ�ΪK1��K2����K1��K2����B����ȷ��C������Ӧ���е�״̬dʱ����Ӧδ�ﵽƽ��״̬������Ӧ������ƽ�⣬��Ӧ�����ɵ�I3-�����ƶ�����v����v�棬��C��ȷ��D��״̬a��״̬b��ȣ�b״̬�൱����a�Ļ����������¶ȣ�ƽ�����淴Ӧ�����ƶ�����״̬aʱI2��ת���ʸ��ߣ���D����ѡC��
�������������е��Ѷȵ����⣬Ҳ�Ǹ߿��еij������ͣ����������ǿ�����ض�ѧ�������������ͽ��ⷽ����ָ����ѵ��������Ĺؼ�����ȷ���������Ȼ��Ӱ��ƽ��״̬�ģ�Ȼ��������������ü��ɡ�
�����Ѷȣ���
4��ѡ���� �� 4 mol A ����� 2 mol B ������ 2 L ���ܱ������л�ϲ���һ�������·������·�Ӧ
2A��g��+B��g��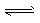 2C��g�������� 2 s���룩���� C ��Ũ��Ϊ 0.6 mol��L-1 ���������м���˵����������ȷ����
2C��g�������� 2 s���룩���� C ��Ũ��Ϊ 0.6 mol��L-1 ���������м���˵����������ȷ����
[? ]
A�������� A ��ʾ��Ӧ��ƽ������Ϊ 0.6 mol��L-1��s-1
B�������� B ��ʾ��Ӧ��ƽ������Ϊ 0.3 mol��L-1��s-1
C��2 s ĩ���� A ��ת����Ϊ70��
D��2 s ĩ���� B ��Ũ��Ϊ 0.7 mol��L-1
�ο��𰸣�D
���������
�����Ѷȣ�һ��
5������� ͼһ��ú������ҵ����һ���֣���������ѧ֪ʶ���ش��������⣺
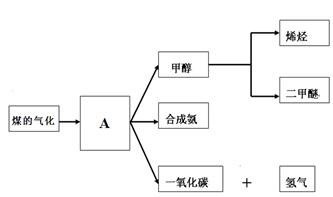
ͼһ
��1��ͼһ������A���׳���_______________
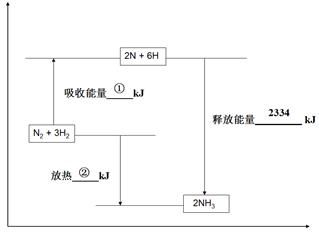
��2���ϳɰ���ҵ��ú������ҵ���зdz���Ҫ��һ������֪��һ�����ݣ��ƻ�1mol�����еĻ�ѧ����Ҫ����946 kJ�������ƻ�0.5mol�����е�H-H����Ҫ����218kJ���������γɰ�������1 mol N-H���ܹ��ͷ�389kJ������ͼ����ʾ�ϳɰ���ҵ�����������ı仯���뽫ͼ�Т١��ڵ������仯����ֵ�������±ߵĺ����ϡ�
ͼ��
��?kJ ����?kJ
��3��ú������ҵ����Ҫ��Ʒ֮һ�״�����һ�����͵���������ȼ�ϣ�������ҵ�һ��ͨ��CO��H2�����Ʊ��״�,�÷�Ӧ�Ļ�ѧ����ʽΪ��CO (g) + 2H2(g) CH3OH(g)
CH3OH(g)
��������������˵��������Ӧ�Ѵ�ƽ�����_______��
A. �����������ƽ��Ħ���������ֲ���
B.? 2v(H2)�� = v(CH3OH)��
C. �����������ѹǿ���ֲ���
D. ��λʱ��������n molCO��ͬʱ����2n mol H2
�����ݻ��̶��ĺ����ܱ������г���CO��H2����������Ӧ����Ӧ�ڵ�4 minʱ��ﵽ���ȣ���ʱ������ѹǿ�뷴Ӧǰ֮��Ϊ3�U5�����������ʵĸ������ʵ���Ũ�����±���
ʱ��/Ũ��
| c(CO)(mol/L)
| C(H2 )(mol/L)
| c(CH3OH)(mol/L)
|
��ʼ
| 0.200
| 0.300
| 0.000
|
��4 min
| a
| b
| c
|
��b=__________________
��4���״�������ȼ�ϵ�أ�DMFC)��һ�ָ�Ч�ܡ�����Ⱦ�綯�����ij��ص�أ��乤��ԭ������ͼ��ʾ����ȼ�ϵ�صĵ�ط�ӦʽΪ2CH3OH (g) + 3O2(g) = 2CO2(g) + 4H2O(l)�����ĵ缫��ӦʽΪ______________________����������pHֵ_______________(��д����������С�����ߡ����䡱)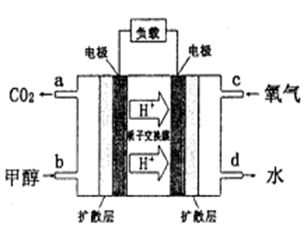
�ο��𰸣���1��ˮú�� ��2�� ��?2254?��?80 ?��3�� A��C? 0.100 91exam .org?
��4��CH3OH-6e- +H2O=CO2+6H+?����
�����������2�������յ�����=946+218��6= 2254KJ���ڷų�������=2254-2334=80KJ
��3���ٸ÷�Ӧǰ�����������������ȣ��ʵ�ƽ�����Ħ��������ѹǿ����ʱ����Ӧ�ﵽ��ƽ��״̬��v(H2)�� = 2v(CH3OH)��Ҳ�ܱ�ʾ��Ӧ�ﵽƽ��״̬����Dѡ���ʾ�淴Ӧ�����ܱ�ʾ��Ӧ�ﵽƽ��״̬�����跴Ӧ�����У�CO��ת��Ũ��Ϊx��H2Ϊ2x���״�Ϊx����CO��ƽ��Ũ��Ϊ��0.2-x����H2��ƽ��Ũ��Ϊ��0.3-2x�����״���ƽ��Ũ��Ϊx,��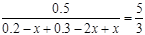 ����ã�x=0.100����4����������������Ӧ������������ԭ��Ӧ�������ĵ缫��Ӧʽ��O2+4e-+4H+=2H2O����������pHֵ����
����ã�x=0.100����4����������������Ӧ������������ԭ��Ӧ�������ĵ缫��Ӧʽ��O2+4e-+4H+=2H2O����������pHֵ����
���������������ǹ�ҵ����Ҫ��ҵ���������߿����ȵ㣬�����ڱ���������Ӧע��֪ʶ��������ã��ﵽ��һ������Ч�����ѶȽϴ�
�����Ѷȣ�����