微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (10分)2SO2(g) + O2(g) = 2SO3 (g)反应过程的能量变化如图所示。已知1mol SO2 (g)氧化为1mol SO3(g)的 ΔH= ―99kJ・mol-1。请回答下列问题:
ΔH= ―99kJ・mol-1。请回答下列问题:
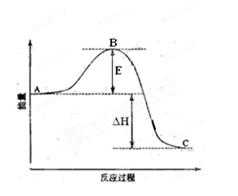
 (1)图中A、C分别表示?,E的大小对该反应的反应热
(1)图中A、C分别表示?,E的大小对该反应的反应热
?(填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点?(填“升高”或“降低”),△H?(填“变大”、“变小”或“不变”),
 (2)图中△H=?KJ・mol-1;
(2)图中△H=?KJ・mol-1;
参考答案:(1)A表示反应物总能量、C表示生成物总能量;无;降低;?不变;(2)―198
本题解析:略
本题难度:一般
2、选择题 在一定条件下密闭容器中发生: 4NH3(g) + 5O2(g) 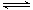 4NO (g)+ 6H2O(g)
4NO (g)+ 6H2O(g)
反应过程中能量变化如图所示;下列说法正确的是
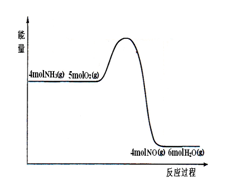
A.由图可知,该反应的正反应是吸热反应
B.升高温度可以提高NH3的转化率
C.反应体系中加入催化剂可增加反应热
D.将平衡混合物通入水中一定有硝酸铵生成
参考答案:D
本题解析:由图示可知,反应物总能量大于生成物总能量,为放热反应,升温时,平衡逆向移动,可降低氨气的转化率,排除AB
催化剂只能改变反应速率,不影响平衡的移动,不会改变反应热,排除C
平衡混合物中NO可被氧气氧化为NO2,NO2溶于水有硝酸生成,硝酸与氨气可得到硝酸铵
答案为D
本题难度:一般
3、选择题 下列说法中不正确的是(?)
A.吸热反应不一定需要加热条件
B.放热反应只有化学键的形成,没有化学键的断开
C.化学反应除了生成新物质外,还伴随着能量的变化
D.稀酸和稀碱发生中和反应生成1mol水所释放的热量称为中和热
参考答案:B
本题解析:略
本题难度:简单
4、填空题 (9分)如图所示,在一个小烧杯里加入研细的20g Ba(OH)2・8H2O晶体。将此小烧杯放在事先滴有3~4滴水的玻璃片上,然后向小烧杯中加入10g NH4CL晶体,并用玻璃棒快速搅拌。
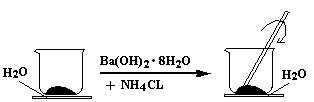
(1)实验中要用玻璃棒搅拌的原因是?。
(2)写出该反应的化学方程式?。
该反应?(填“是”或“不是”)氧化还原反应。
(3)该实验的现象有?。
(4)该反应为?(填“吸”或“放”)热反应,这是由于反应物的总能量?(填“大于”或“小于”)生成物的总能量。
参考答案:(1)该反应是固体之间的反应,搅拌可使混合物充分接触并发生反应
(2)Ba(OH)2・8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O?不是
(3)玻璃片上因结冰而与小烧杯粘在一起,同时有刺激性气味的气体产生
(4)吸?小于
本题解析:(1)因为反应物都是固体,即这是固体间的反应,所以通过玻璃棒的搅拌可使混合物充分接触并发生反应。
(2)在反应中元素的化合价并没有发生变化,所以不是氧化还原反应。
(3)因为反应是吸热反应,所以会导致温度降低,因而还会结冰,同时有氨气释放出来,所以还会闻到有刺激性气味的气体产生。
(4)根据谢谢可知反应是吸热的,这说明反应物的总能量小于生成物的总能量。
本题难度:简单
5、实验题 (8分)用一定浓度的稀盐酸与稀NaOH溶液在左下图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热。已知强酸与强碱的中和热为57.3KJ/mol,水的比热容为4.2J/(g・℃),有关热量与比热容的计算公式:Q=m×c×△t(Q为热量,m为物质的质量,c为比热容,△t物质温度的变化值)
回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是:??
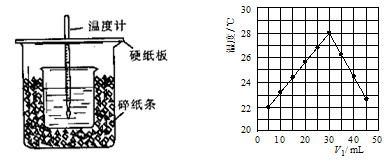
(2)将V1 mL 1.0 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50 mL)。
 ?
?
下列叙述正确的是?
A.做该实验时环境温度为22 ℃
B.该实验表明化学能可以转化为热能
C.NaOH溶液的浓度约是1.00 mol/L
D.该实验表明有水生成的反应都是放热反应