微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某位同学配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是
[? ]
A.有少量NaOH溶液残留在烧杯里
B.向容量瓶中加水未到刻度线
C.所用NaOH已经潮解
D.带游码的天平称2.4gNaOH时误用了“左码右物”方法
参考答案:B
本题解析:
本题难度:简单
2、选择题 下列说法正确的是
A.一定温度下,1L0.5mol・L-1NH4Cl溶液与1L0.25mol・L-1NH4Cl溶液中NH4+ 物质的量之比为2:1
B.100g硫酸溶液的物质的量浓度为18.4mol/L,用水稀释到物质的量浓度为9.8mol/L,需要水100g.
C.标准状况下,22.4LCH3Cl和CHCl3的混合物中所含有的碳原子个数一定为NA
D.在2Na2O2+2CO2=2Na2CO3+O2反应中,每生成16g氧气,则转移NA个电子
参考答案:D
本题解析:略
本题难度:简单
3、选择题 环氧乙烷(
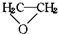
)、丙酮、丁醛、葡萄糖的混合物,碳元素的质量分数为66%,则氧元素的质量分数为( )
A.33%
B.27%
C.30%
D.23%?
参考答案:因环氧乙烷(
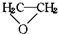
)、丙酮、丁醛、葡萄糖的混合物中,存在定组成CH2,
碳元素的质量分数为66%,
则氢元素的质量分数为66%×212=11%,
混合物中共有C、H、O三种元素,
则氧元素的质量分数为1-66%-11%=23%,
故选D.
本题解析:
本题难度:简单
4、计算题 (共7分)今有盐酸、硫酸混合液100 mL,向其中加入足量氯化钡溶液,反应完
全后,过滤,将沉淀洗涤、烘干,称得沉淀的质量为9.32g。向滤液中加入500 mL 0.2
mol/L的氢氧化钠溶液呈中性。求混合液中盐酸、硫酸的物质的量浓度各为:
(1)硫酸的物质的量浓度为____________
(2)盐酸的物质的量浓度为____________
参考答案:H2SO4:0.4 mol/L (3分) HCl:0.2 mol/L (4分)
本题解析:考查物质的量的有关计算。
(1)生成沉淀的方程式是H2SO4+BaCl2=2HCl+BaSO4↓
硫酸钡的质量是9.32g
则硫酸钡的物质的量是9.32g÷233g/mol=0.04mol
所以硫酸的物质的量也是0.04mol
根据c=n/V可知
硫酸的浓度是0.04mol÷0.1L=0.4mol/L
(2)消耗氢氧化钠的物质的量是0.5L× 0.2 mol/L=0.1mol
硫酸中氢离子的物质的量是0.08mol
所以盐酸的物质的量是0.1mol-0.08mol=0.02mol
因此盐酸的浓度是0.02mol÷0.1L=0.2mol/L
本题难度:一般
5、选择题 32g Cu的物质的量是
A.3.01×1023个
B.0.5mol
C.11.2L
D.1 mol