微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列有关元素周期表的叙述错误的是(?)
A.原子半径最小的是氢
B.所含元素种类最多的族是第VIII族
C.金属元素的种类多于非金属元素
D.第n周期第n主族的元素不一定为金属
参考答案:B
本题解析:略
本题难度:简单
2、选择题 2011年3月,日本福岛核电站由于地震损毁而造成放射性物质泄漏,在我国多地检测出极微量的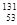 I,关于
I,关于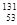 I的下列说法中正确的是(?)
I的下列说法中正确的是(?)
A.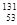 I是放射性核素,应该多吃加碘食盐来预防其对人体的损害
I是放射性核素,应该多吃加碘食盐来预防其对人体的损害
B.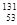 I与
I与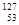 I属于碘元素的两种不同核素,互称同素异形体
I属于碘元素的两种不同核素,互称同素异形体
C.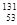 I与
I与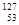 I属于同种元素,所以性质完全相同
I属于同种元素,所以性质完全相同
D.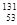 I核内中子数比核外电子数多25个
I核内中子数比核外电子数多25个
参考答案:D
本题解析:在表示原子的组成时元素符号的左下角表示质子数,左上角表示质量数,因此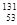 I的质子数是53,质量数是131,则中子数是131-53=78,所以中子数比核外电子数多78-53=25,选项D是正确的。同素异形体是指同种元素组成的不同单质,B错误。
I的质子数是53,质量数是131,则中子数是131-53=78,所以中子数比核外电子数多78-53=25,选项D是正确的。同素异形体是指同种元素组成的不同单质,B错误。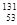 I与
I与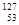 I的质量数不同,属于不同的核素,C不正确。食盐加碘是原来预防甲状腺肿大的,A不正确。答案是D。
I的质量数不同,属于不同的核素,C不正确。食盐加碘是原来预防甲状腺肿大的,A不正确。答案是D。
本题难度:一般
3、选择题 元素性质呈周期性变化决定因素是
A.元素半径大小呈周期性变化
B.元素相对质量依次递增
C.元素核外电子排布呈周期性变化
D.元素最高正化合价呈周期性变化
参考答案:C
本题解析:结构决定性质,即原子的核外电子排布尤其是最外层电子排布决定了元素的性质,所以
元素性质呈周期性变化的决定因素是元素原子核外电子排布呈周期性变化的必然结果,C正确。
本题难度:一般
4、选择题 下表为元素周期表的一部分,有关说法正确的是
族
周期
| IA
| ?
| 0
|
1
| ①
| ⅡA
| ⅢA
| ⅣA
| ⅤA
| ⅥA
| ⅦA
| ?
|
2
| ?
| ?
| ?
| ②
| ③
| ④
| ?
| ?
|
3
| ⑤
| ?
| ⑥
| ⑦
| ?
| ?
| ⑧
| ?
|
?
A.④、⑤、⑥、⑦、①的原子半径依次减小
B.⑤、⑥、⑧的最高价氧化物对应的水化物不能相互反应
C.⑦、②、③、④的氢化物的稳定性依次增强
D.②、③的气态氢化物均能与它们的最高价氧化物对应的水化物反应
参考答案:C
本题解析:A项中④的原子半径比⑦小,错误;B项中⑥的最高价氧化物对应的水化物为两性,所以相互间反应;②的气态氢化物为甲烷与其最高价氧化物对应的水化物不反应,所以D项错误。
本题难度:一般
5、填空题




(1)Ge的原子核外电子排布式为
(2)C、Si、Sa三种元素的单质中,能够形成金属晶体的是
(3)按要求指出下列氧化物的空间构型、成键方式或性质
①CO2分子的空间构型及碳氧之间的成键方式?;
②SO2晶体的空间构型及硅氧之间的成键方式?;
③已知SnO2是离子晶体,写出其主要物理性质?(写出2条即可)
(4)CO可以和很多金属形成配合物,如Ni(CO)2,Ni与CO之间的键型为
(5)碳氧键的红外伸缩振动频率与键的强度成正比,已知Ni(CO)4中碳氧键的伸缩振动频率为2060cm-3,CO分子中碳氧键的伸缩振动频率为2143cm-2,则Ni(CO)中碳氧键的强度比CO分子中碳氧键的强度?(填字母)
A.强?
B.弱?
C.相等?
D.无法判断
参考答案:(1)1s22s22p63s23p63d104s24p2
(2)Sn
(3)①直线型?共价键(或α键与π键)②Si=O通过共价键形成四面体结构,四面体之间通过共价键形成空间网状结构共价键(或α键)③熔融时能导电、较高的熔点
(4)配位键
(5)B
本题解析:考查学生对原子结构和原子核外电子排布的了解,对常见物质空间构型和化学键与物质性质的了解,以及对原子晶体、金属晶体、简单配合物的结构的了解和对离子键形成的理解,考查学生的归纳推理能力、信息迁移能力及其综合应用能力。
本题难度:简单