微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列关于物质性质变化的比较,正确的是
A.非金属性强弱: I>Br>Cl
B.原子半径大小:Na>P> S
C.碱性强弱:KOH>NaOH>LiOH
D.金属性强弱: Na>Mg>Al
2、填空题 如图为四、五、六、七主族元素简单氢化物沸点随周期变化图像,(代表氢化A、B、C、D物中另外一种元素)分析图像并回答
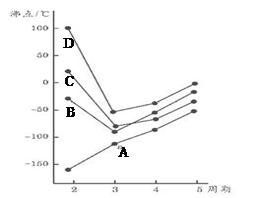
(1)写出B3-的空间构型?
(2)B元素另外一种氢化物可做火箭的燃料,其电子式为:__________________,中心原子杂化方式为_______________
(3)A元素氧化物晶体类型为____________________,研究发现其氧化物晶胞中,A的位置与金刚石晶胞中碳原子位置相似,试分析晶胞中占有氧原子个数应为___________个。
(4)A、B、C、D第一电离能由小到大的顺序是____________________(用元素符号表示)
3、实验题 (11分)为探究Na、M g、Al的金属活动性顺序,某课外小组同学进行了如下实验:
g、Al的金属活动性顺序,某课外小组同学进行了如下实验:
 他们记录的实验现象有:
他们记录的实验现象有:
实验
现象
| ①剧烈反应,迅速生成大量的气体。
②浮在水面上,熔成小球,不断游动,小球渐小最终消失,溶液变红。
③反应不剧烈,产生无色气体。
④有气体产生,溶液变成红色。
|
请帮助该小组同学补充下列实验报告中的内容。
(1)在下表中填写与实验相对应的实验现象序号:
(2)写出钠与水 反应的化学方程式___________________________________。
反应的化学方程式___________________________________。
(3)实验结论是______________________________________。
(4)用原子结构理论对上述实验结论进行解释:同周期元素从左至右,原子的电子层数相同,核电荷数逐渐增多,原子半径逐渐_________,原子核对电子的引力逐渐增强,失电子能力逐渐_________,因此_________逐渐减弱。
4、选择题 下列有关物质性质的比较,正确的是
A.热稳定性:HF<HCl<HBr
B.微粒半径: O2->Mg2+>Cl-
C.第一电离能:Si>Al>Mg
D.电负性:Si>Al>Mg
5、选择题 铊盐与氰化钾被列为A级危险品,铊(Tl)与铝同主族,Tl3+与Ag在酸性介质中发生反应:Tl3+ +2Ag===Tl+ +2Ag+且已知Ag+ +Fe2+===Ag+Fe3+,则下列推断正确的是( ?)
A.Tl+最外层有3个电子
B.氧化性:Tl3+>Ag+>Fe3+
C.Tl(OH)3与Al(OH)3相似,也是两性氢氧化物
D.铊位于第五周期ⅢA族