微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在下图装置中,若通电一段时间后乙装置左侧电极质量增加,则下列说法错误的是(? )

A.乙中左侧电极反应式:Cu2++2e-=Cu
B.电解过程中装置丙的pH无变化
C.向甲中通人适量的HCl气体,可使溶液恢复到电解前的状态
D.当甲装置中产生标准状况下4.48 L气体时,Cu电极上质量增加43.2 g
参考答案:D
本题解析:A、乙装置的左侧电极质量增加,则左侧为阴极,由此可确定X极为负极,Y为正极,乙装置中铜离子放电,对;B、装置内阴极析出银单质,阳极上的银失去电子变成银离子,理论上溶液的物质的量浓度不变,pH保持不变,对;C、装置甲中开始的反应为:2KCl+2H2O2KOH+H2↑+Cl2↑,故要使溶液恢复可通入适最HCl气体即可,对;D、由装置甲发生的反应可得两电极产生的气体体积相等,所以产生氢气为2.24 L,转移电子0.2 mol,则铜电极上生成Ag0.2 mol,质量为21.6 g,错。
本题难度:一般
2、选择题 如图a、b都是惰性电极,通电一段时间后,b极附近溶液呈蓝色。下列说法中不正确的是?

[? ]
A.U形管中溶液碱性增强?
B.c上析出红色物质
C.a极和Pt都有气泡产生?
D.x是正极,y是负极
参考答案:D
本题解析:
本题难度:一般
3、选择题 用惰性电极电解饱和Na2SO4溶液,若保持温度不变,则一段时间后( )
A.溶液pH变大
B.c(Na+)与c(SO42-)的比值变大
C.溶液浓度变大,有晶体析出
D.溶液浓度不变,有晶体析出
参考答案:A.硫酸钠是强酸强碱盐,其水溶液呈中性,用惰性电极电解饱和硫酸钠溶液,实质上是电解水,温度不变,所以溶液的pH不变,故A错误;
B.该电解过程中,实际上是电解水,溶质的量不变,所以溶液由饱和溶液变为过饱和溶液,有硫酸钠晶体析出,且硫酸钠是强酸强碱盐,钠离子、硫酸根离子不水解,所以c(Na+)与c(SO42-)的比值不变,故B错误;
C.该电解过程中,实际上是电解水,溶质的量不变,所以溶液由饱和溶液变为过饱和溶液,有硫酸钠晶体析出,温度不变,溶液浓度不变,故C错误;
D.该电解过程中,实际上是电解水,溶质的量不变,所以溶液由饱和溶液变为过饱和溶液,有硫酸钠晶体析出,温度不变,溶液浓度不变,故D正确;
故选D.
本题解析:
本题难度:简单
4、填空题 (12分)如下图,通电5 min后,电极5质量增加2.16 g,回答:

(1)电源:a是________极,b是________极;A池电极反应,电极1:__________;
电极2:____________________________________________________________。
C池电极反应,电极5:________________________________________________;
电极6:______________________________________________________________。
(2)如果B池中共收集到224 mL气体(标准状况),且溶液体积为200 mL(设电解过程中溶液体积不变),则通电前溶液中Cu2+的物质的量浓度为________。
参考答案:(1)负 正 2H++2e-===H2↑ 2Cl--2e-===Cl2↑ 2Ag++2e-===2Ag Cu-2e-===Cu2+
(2)0.025 mol/L
本题解析:(1)通电5 min后,电极5质量增加2.16 g,这说明电极5是阴极,所以电极是阳极。则b是电源的正极,a是电源的负极。因此电极1是阴极,氢离子放电生成氢气,电极反应式是2H++2e-===H2↑。电极2是阳极,溶液中的氯离子放电生成氯气,电极反应式是2Cl--2e-===Cl2↑。C装置中电极5是阴极,溶液中的银离子放电,电极反应式是2Ag++2e-===2Ag。电极6是阳极,但电极是铜电极,所以铜失去电子,电极反应式是Cu-2e-===Cu2+。
(2)电极5生成银的质量是2.16g,物质的量是0.02mol,转移0.02mol电子。B池中共收集到224 mL气体(标准状况),则气体的物质的量是0.01mol。如果气体全部是氧气,则转移电子是0.04mol。显然电子的得失不守恒,所以生成的气体中还含有氢气。根据电子的得失守恒可知,阳极生成氧气的物质的量是0.02mol÷4=0.005mol,所以阴极生成的氢气是0.01mol-0.005mol=0.005mol。则阴极析出的铜的物质的量是(0.02mol-0.005mol×2)÷2=0.005mol,因此电解硫酸铜溶液的物质的量浓度是0.005mol÷0.2L="0.025" mol/L。
点评:该题的难点在(2)问,需要利用电子守恒,通过讨论得出阴极还有氢气生成,最后再通过电子的守恒计算即可,属于中等难度的试题。
本题难度:一般
5、填空题 (16分)某粗铜含铁、银、金和铂等杂质,通过电解精炼铜后,为充分利用电解后的阳极泥和电解液,设计如下工艺流程:
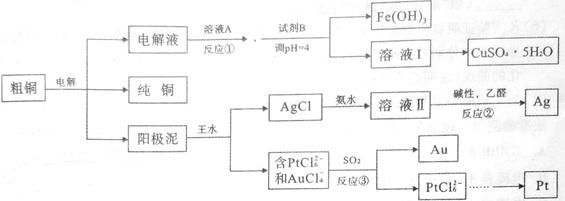
回答下列问题:
(1)电解时,以粗铜作______极,______________为电解液,写出阴极的电极反应式______________。
(2)电解后溶液中含有的主要金属阳离子为________________;溶液A是一种绿色氧化剂,则反应①的离子方程式为___________________________________________。
(3)加入的试剂B最好选用___________(填序号)
A.Cu
B.CuO
C.NaOH
D.氨水