微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 如图为持续电解含有一定量CaCl2水溶液(含酚酞)的装置(以铂为电极),A为电流表。电解一段时间t1后,将CO2连续通入电解液中。
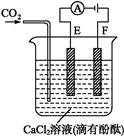
(1)电解时,F极发生 反应,电极反应为 ,E极发生 反应,电极反应为 ,电解总反应为 。
(2)电解池中产生的现象:
① 。
② 。
③ 。
参考答案: (1)氧化 2Cl--2e- Cl2↑ 还原 2H++2e-
Cl2↑ 还原 2H++2e- H2↑ 2Cl-+2H2O
H2↑ 2Cl-+2H2O 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
(2)①通电后E极处溶液呈红色 ②通电时,E极、F极均有气体生成 ③通入CO2时,溶液中先出现白色沉淀,继续通入CO2沉淀又消失
本题解析:溶液中含有:Ca2+、H+、Cl-、OH-,通电时,Ca2+、H+移向阴极,H+放电能力比Ca2+强,在E极上发生反应:2H++2e- H2↑,H2O电离出的H+放电,OH-富集在阴极(E极),则使阴极区溶液变红;Cl-、OH-移向阳极,Cl-在阳极放电,2Cl-
H2↑,H2O电离出的H+放电,OH-富集在阴极(E极),则使阴极区溶液变红;Cl-、OH-移向阳极,Cl-在阳极放电,2Cl- Cl2↑+2e-,总反应方程式:2Cl-+2H2O
Cl2↑+2e-,总反应方程式:2Cl-+2H2O Cl2↑+H2↑+2OH-;电解一段时间t1后,溶液中OH-浓度增大,相当于Ca(OH)2、CaCl2的混合溶液,通入CO2:Ca2++2OH-+CO2
Cl2↑+H2↑+2OH-;电解一段时间t1后,溶液中OH-浓度增大,相当于Ca(OH)2、CaCl2的混合溶液,通入CO2:Ca2++2OH-+CO2 CaCO3↓+H2O,继续通入CO2:CaCO3+CO2+H2O
CaCO3↓+H2O,继续通入CO2:CaCO3+CO2+H2O Ca(HCO3)2。
Ca(HCO3)2。
考点:电解原理
本题难度:一般
2、填空题 下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极。接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加。据此回答问题
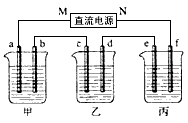
(1)电源的N端为______极;
(2)写出电解前后各溶液的pH变化情况(增大、减小或不变):
甲溶液______;乙溶液______;丙溶液______;
(3)电极b上生成的气体在标准状态下的体积是______;电极c的质量变化是______g。
参考答案:(1)正
(2)增大;减小;不变
(3)2.8L;16
本题解析:
本题难度:一般
3、选择题 下列各组中,每种电解质溶液在惰性电极条件下电解时只生成氢气和氧气的是( )
A.HCl、CuCl2、Ba(OH)2
B.NaOH、CuSO4、H2SO4
C.NaOH、H2SO4、Ba(OH)2
D.NaBr、H2SO4、Ba(OH)2
参考答案:A.电解HCl生成氢气和氯气,电解CuCl2生成Cu和氯气,电解Ba(OH)2生成氢气和氧气,故A不选;
B.电解NaOH生成氢气和氧气,电解CuSO4生成Cu、氧气、硫酸,电解H2SO4生成氢气和氧气,故B不选;
C.电解NaOH、H2SO4、Ba(OH)2,均只生成氢气和氧气,故C选;
D.电解NaBr生成溴、氢气、NaOH,电解H2SO4生成氢气和氧气,电解Ba(OH)2生成氢气和氧气,故D不选;
故选C.
本题解析:
本题难度:一般
4、填空题 雾霾含有大量的污染物SO2、NO。工业上变“废”为宝,吸收工业尾气SO2和NO,可获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素):

(1)装置Ⅰ中的主要离子方程式为 。
(2)含硫各微粒(H2SO3、HSO3-和SO32-)存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数X(i)与溶液pH 的关系如图所示。

①若是0.1molNaOH反应后的溶液,测得溶液的pH=8时,溶液中个离子由大到小的顺序是 。
②向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因: 。
(3)写出装置Ⅱ中,酸性条件下的离子方程式 。
(4)装置Ⅲ还可以使Ce4+再生,其原理如下图所示。
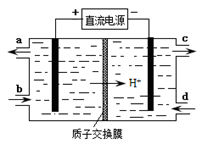
①生成Ce4+从电解槽的 (填字母序号)口流出。
②写出与阴极的反应式 。
(5)已知进入装置Ⅳ的溶液中,NO2-的浓度为a g・L-1,要使1 m3该溶液中的NO2-完全转化为NH4NO3,需至少向装置Ⅳ中通入标准状况下的O2 L。(用含a代数式表示,计算结果保留整数)
参考答案:(每空2分)
(1)SO2 + OH-="==" HSO3-
(2)①c(Na+>c(SO32-)>c(HSO3-)>c(OH-)>c(H+)
②HSO3- 在溶液中存在电离平衡:HSO3- SO32-+H+,加入CaCl2溶液后,Ca2++SO32-="==" CaSO3↓使电离平衡右移,c(H+)增大。
SO32-+H+,加入CaCl2溶液后,Ca2++SO32-="==" CaSO3↓使电离平衡右移,c(H+)增大。
(3)NO+2H2O+3Ce4+===3Ce3++NO3-+4H+、NO+H2O+Ce4+===Ce3++NO2-+2H+
(4)①a ②2HSO3-+4H++ 4e-="==" S2O32-+3H2O
(5)243a(242a、244a、5600a /23都给分)
本题解析:(1)装置Ⅰ中的将SO2变成了HSO3-,离子方程式是SO2 + OH-="==" HSO3-。
(2)①若是0.1molNaOH反应后的溶液,测得溶液的pH=8时,图像中的c(SO32-)>c(HSO3-),而c(OH-)=10-6mol/L,远小于c(OH-),故溶液中离子浓度为:c(Na+>c(SO32-)>c(HSO3-)>c(OH-)>c(H+)。②HSO3- 在溶液中存在电离平衡:HSO3- SO32-+H+,加入CaCl2溶液后,Ca2++SO32-="==" CaSO3↓使电离平衡右移,c(H+)增大。
SO32-+H+,加入CaCl2溶液后,Ca2++SO32-="==" CaSO3↓使电离平衡右移,c(H+)增大。
(3)在酸性条件下装置Ⅱ中,Ce4+将NO氧化为NO3-或NO2-,本身还原为Ce3+,有两个反应,即NO+2H2O+3Ce4+===3Ce3++NO3-+4H+、NO+H2O+Ce4+===Ce3++NO2-+2H+。
(4)装置Ⅲ使Ce3+→Ce4+,反应过程失去电子,在阳极发生,接电源正极,故生成Ce4+从电解槽的a口出来;阴极HSO3-得到电子生成S2O32,即2HSO3-+4H++ 4e-="==" S2O32-+3H2O。
(5)装置Ⅳ中的与O2和NO2-参加的反应:2NH3+2H++O2+2NO2-===2NH4NO3,n(O2)=n(NO2-)= ×1000L×a g・L-1/46g・mol-1,V(O2)=22.4L・mol-1 n(O2)= 243a。
考点:离子方程、电极反应式的书写及简单化学计算。
本题难度:困难
5、选择题 用铂电极电解下列溶液,阴极和阳极上的主要产物为分别为H2和O2的是( )
A.稀NaOH溶液
B.HCl溶液
C.CuSO4溶液
D.酸性AgNO3溶液
参考答案:A、电解氢氧化钠的实质是电解水,阴极和阳极上的主要产物为分别为H2和O2,故A正确;
B、电解HCl的实质是电解物质本身,在阴极和阳极上的主要产物为分别为H2和Cl2,故B错误;
C、电解硫酸铜属于“生酸放氧型”,在阴极和阳极上的主要产物为分别为Cu和O2,故C错误;
D、电解硝酸银属于“生酸放氧型”,在阴极和阳极上的主要产物为分别为Ag和O2,故D错误.
故选A.
本题解析:
本题难度:一般