��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1�������� (6��)��4 mol SO2��2 mol O2������2L�������л�ϣ���һ�������·������·�Ӧ��2SO2(g)��O2 (g) 2SO3 (g)������2s����SO3��Ũ��Ϊ0.6 mol/ L���Լ��㣺
2SO3 (g)������2s����SO3��Ũ��Ϊ0.6 mol/ L���Լ��㣺
��1:v(O2)��
С��2:SO2��ת���ʣ�
С��3:2sʱ��O2Ũ�ȡ�
�ο��𰸣�
��1:0.15mol/��L��s����
��1:30%��
��1:0.7mol/L
���������������淴Ӧ��Ӧ�ü��㡣�ڿ��淴Ӧ�ļ�����������������ʽ�����ֱ��г���ʼ����ת������ƽ�⣨��ijʱ�̣�����Ȼ�����������ʽ���㼴�ɡ�
��ӦʽΪ? 2SO2(g)��O2 (g) 2SO3 (g)
2SO3 (g)
��ʼ����mol��? 4? 2? 0
ת������mol��? 1.2? 0.6? 1.2
2s��mol��? 2.8? 1.4? 1.2
��1����������ʾ�ķ�Ӧ����Ϊ
��2��SO2��ת����Ϊ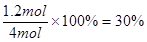
��3��2sʱ��O2Ũ��Ϊ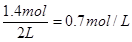
�����Ѷȣ�һ��
2������� �ںϳɰ���Ӧ�У���úϳ�����ڴ�N2��H2��NH3���������Ϊ6��18��1�����ڴ�N2��H2��NH3���������Ϊ9��27��8����H2��ת����Ϊ______��
�ο��𰸣�25%
�������������ڴ�N2��H2��NH3���������Ϊ6L��18L��1L������ת�������Ϊx����
N2?��? 3H2?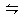 ?2NH3
?2NH3
��ʼ���ʵ����/L��? 6? 18? 1?
ת�����ʵ����/L��? x? 3x? 2x?
ƽ�����ʵ����/L��? 6��x? 18��3x? 1��2x?
�����⣬�ɵã�?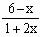 ��
��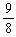
��ã�x��1.5L
��A��ת����Ϊ������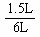 ��100%��25%
��100%��25%
�����Ѷȣ���
3������� ��8�֣������裨Si3N4����һ�������մɲ��ϣ�������ʯӢ�뽹̿�ڸ��µĵ������У�ͨ�����·�Ӧ�Ƶã�
��SiO2����C����N2 ��Si3N4����CO
��Si3N4����CO
��1����ƽ������Ӧ�Ļ�ѧ����ʽ������ѧ���������ڷ����ڣ���
��2���÷�Ӧ���������������������������仹ԭ��������������������
��3����֪������ӦΪ���ȷ�Ӧ�����䷴Ӧ�ȡ�H���������㣨����ڡ�����С�ڡ����ڡ����������¶ȣ���ƽ�ⳣ��ֵ���������������������С�����䡱����
��4����ʹѹǿ����������ƽ����������������Ӧ�����ƶ�����������桱����
��5������֪CO��������Ϊv(CO)��18mol/(L.min)����N2����������Ϊv(N2)��������������mol/(L.min)��
�ο��𰸣���1��3��6��2��1��6��2�֣�
��2��N2��Si3N4?��3��С��?��С?��4����?��5��6��ÿ��1�֣�
�����������1����Ӧ��̼Ԫ�صĻ��ϼ۴�0�����ߵ���2�ۣ�ʧȥ2�����ӣ���Ԫ�صĻ��ϼ۴�0�۽��͵���3�ۣ��õ�3�����ӡ����Ը��ݵ��ӵĵ�ʧ�غ��֪����ԭ���������������ʵ���֮����3�U1��������ƽ��Ļ�ѧ�������ֱ�������3��6��2��1��6��
��2�����ݣ�1����֪���������������仹ԭ������Si3N4��
��3�����ȷ�Ӧ�ġ�HС��0�������¶�ƽ�������ȵ��淴Ӧ�����ƶ������ƽ�ⳣ����С��
��4��������ƽ��ķ���ʽ��֪������Ӧ���������ģ���������ѹǿ��ƽ�����淴Ӧ�����ƶ���
��5�����ݷ�Ӧ����֮������Ӧ�Ļ�ѧ������֮�ȿ�֪������������������18mol/(L.min)��3��6mol/(L.min)��
�����Ѷȣ�һ��
4��ѡ���� �����ͬ�ļס���������������ͬ�¶��¼׳���1gSO2 ��g����1g O2��g��,�ҳ���2g SO2��g����2g O2��g������Ӧ2SO2��g��+O2(g) 2SO3(g)��ƽ�����SO2��ת����Ϊm������SO2��ת����Ϊn���� m��n�Ĺ�ϵΪ
2SO3(g)��ƽ�����SO2��ת����Ϊm������SO2��ת����Ϊn���� m��n�Ĺ�ϵΪ
A��m =" n"
B��m > n
C��m < n
D����ȷ��
�ο��𰸣�C
�����������
�����Ѷȣ�һ��
5��ѡ���� ��һ���¶��£�������ijһ��Ӧ��M��N�����ʵ����淴Ӧʱ��ı仯������ͼ�����б����в���ȷ����
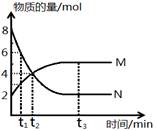
A����Ӧ�Ļ�ѧ����ʽΪ��2M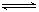 N
N
B��t3ʱ�����淴Ӧ�������
C��t2ʱ��N���������ʴ���N����������
D��t1ʱ��N��Ũ����MŨ�ȵ�2��
�ο��𰸣�A
�����������Ӧ�Ļ�ѧ����ʽΪ��M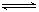 2N��t2 N���������ʴ���N���������ʣ�t3ʱƽ�⣬���淴Ӧ������ȡ�t1ʱ��N��Ũ��Ϊ6mol��L��MŨ��3mol��L��2����
2N��t2 N���������ʴ���N���������ʣ�t3ʱƽ�⣬���淴Ӧ������ȡ�t1ʱ��N��Ũ��Ϊ6mol��L��MŨ��3mol��L��2����
�����Ѷȣ�һ��