|
高考化学知识点总结《反应速率与平衡的有关计算》答题技巧(2017年最新版)(六)
2017-08-10 02:26:42
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 甲醇被称为2l世纪的新型燃料,工业上通过下列反应Ⅰ和Ⅱ,用CH4和H2O为原料来制备甲醇:
CH4(g)+H2O(g) CO(g)+3H2(g)……Ⅰ? CO(g)+2H2(g) CO(g)+3H2(g)……Ⅰ? CO(g)+2H2(g) CH3OH(g) ……Ⅱ。 CH3OH(g) ……Ⅱ。
(1)将1.0 mol CH4和2.0 mol H2O(g)通入容积为100L反应室,在一定条件下发生反应I,CH4的平衡转化率与温度、压强的关系如图。
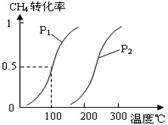
①已知100℃时达到平衡所需的时间为5min,则用H2表示的平均反应速率为?。
②图中的P1?P2(填“<”、“>”或“=”),100℃时平衡常数的值为??。
(2)在压强为0.1 MPa条件下, 将a mol CO与 3a?mol H2的混合气体在催化剂作用下,自发反应Ⅱ,生成甲醇。
③该反应的△H?0;若容器容积不变,下列措施可增加甲醇产率的是?。
A.升高温度
B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大
D.再充入1mol CO和3mol H2
| ④为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
实验编号
| T(℃)
| n(CO)/n(H2)
| P(Mpa)
| i
| 150
| 1/3
| 0.1
| ii
| ?
| ?
| 5
| iii
| 350
| ?
| 5
|
?
a.请在上表空格中填入剩余的实验条件数据。
b.根据反应Ⅱ的特点,在给出的坐标图中,补画出在5MPa条件下CO的转化率随温度变化的趋势曲线示意图,并标明压强。

参考答案:(共16分)
(1)(7分)①0.003mol/(L・min)(2分)?②<(2分)? 2.25×10-4(3分) ?
(2)(9分)③<(2分) BD(2分)?
④a.(见下表,3分)?
实验编号
T(℃)
n(CO)/n(H2)
P(Mpa)
i
?
?
?
ii
150
1/3
?
iii
?
1/3
?
?
b.(见下图,2分)
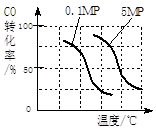
本题解析:(1)①起始时c(CH4)=1.0mol/100L=0.01mol/L,读图可知平衡时CH4转化率为0.5,则CH4的变化浓度为0.01mol/L×0.5=0.005mol/L,根据化学反应速率计算公式可知,v(CH4)= 0.005mol/L÷5min=0.001mol/(L?min),根据系数之比等于速率之比可知,v(H2)="3" v(CH4)= 0.003mol/(L?min);②I是气态物质体积增大的反应,因此增大压强平衡左移,CH4转化率减小,减小压强平衡右移,CH4转化率增大,即压强越小,CH4转化率越大,读图可知,200℃、P1时CH4转化率大于200℃、P2时CH4转化率,说明P1< P2;在P1、100℃时,
CH4(g)+H2O(g) CO(g)+3H2(g) CO(g)+3H2(g)
起始浓度/ mol・L-1? 0.01? 0.02? 0? 0
变化浓度/ mol・L-1? 0.005? 0.005? 0.005? 0.015
平衡浓度/ mol・L-1? 0.005? 0.015? 0.005? 0.015
K="[" c(CO)?c3(H2)]/[ c(CH4)?c(H2O)]= [0.005×0.0153]/[ 0.005×0.015]=2.25×10ˉ4
(2)③II是气态物质体积减小的反应,不符合熵增原理,则正反应符合焓判据,△H<0;正反应是放热反应,升高温度平衡左移,甲醇产率减小,故A错误;减小生成物浓度,平衡右移,甲醇产率增大,故B正确;充入惰性气体,虽然增大压强,但是容器容积不变,各组分浓度不变,平衡不移动,甲醇产率不变,故C错误;再充入投料比相同的CO和H2,就是增大压强,使平衡右移,甲醇产率增大,故D正确;④a、根据控制变量探究的原则,实验i和ii的压强不同,则温度和投料比一定相同;实验ii和iii的温度不同,则投料比和压强一定相同;由此确定实验ii的温度为150℃,投料比为1/3,实验iii的投料比为1/3;b、画图要点:相同温度下,增大压强平衡右移,CO转化率增大,则0.1MPa时CO转化率随温度变化曲线向右适当平移,就变为5MPa时CO转化率随温度变化曲线。
本题难度:一般
2、填空题 (8分)在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表: CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
t℃
| 700
| 800
| 830
| 1000
| 1200
| K
| 0.6
| 0.9
| 1.0
| 1.7
| 2.6
|
回答下列问题:
(1)该反应的化学平衡常数表达式为K=?。
(2)该反应为?反应(选填吸热、放热)。
(3)能判断该反应是否达到化学平衡状态的依据是?。
a.容器中压强不变? b.混合气体中c(CO)不变
c.υ正(H2)=υ逆(H2O)? d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)・c(H2)=c(CO)・c(H2O),试判断此时的温度为?℃。
参考答案:(1 )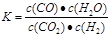 (2)吸热?(3) bc?(4)830 (2)吸热?(3) bc?(4)830
本题解析:(1)平衡常数是指在一定条件下的可逆反应中,当反应达到化学平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,所以根据方程式可知,平衡常数的表达式为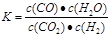
(2)根据数据可知,随温度的升高平衡常数逐渐增大,即升高温度,平衡向正反应方向移动,所以反应是吸热反应。
(3)在一定条件下,当可逆反应中正反应速率和逆反应速率相等时(但不为0),各种物质的浓度或含量均不再发生变化的状态,是化学平衡状态。所以b正确。反应前后体积不变,所以压强始终是不变的,a不正确。C中反应速率的方向是相反的,且满足速率之比是相应的化学计量数之比,c正确。d中反应速率的方向相同,所以不能说明。答案选bc。
(4)当c(CO2)・c(H2)=c(CO)・c(H2O)时K=1,所以温度是830℃。
本题难度:简单
3、选择题 某一反应物的浓度是2mol・ L-1,经过4min后,它的浓度变成1. 68 mol・ L-1,则在这4min内它的平均反应速率为
A.0.2 mol・ L-1
B.0.1 mol・ L-1
C.0.04 mol・ L-1
D.0.08 mol・ L-1
参考答案:D
本题解析:试题分析:反应速率通常用单位时间内浓度的变化量来表示,则该反应的反应速率是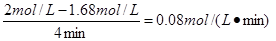 ,答案选D。 ,答案选D。
考点:考查反应速率的有关计算
点评:该题是基础性试题的考查,也是高考中的常见题型和考点。该题的关键是明确反应速率的含义以及表达式,然后结合题意灵活运用即可,有利于培养学生规范的答题能力。
本题难度:一般
4、填空题 有人研究了340 K时N2O5的分解反应:2N2O5=4NO2+O2,所得实验数据(各种物质在不同时刻的浓度)见下表。

(1)图象能够非常直观地描述物理量的变化趋势。请你在下图中分别作出c(N2O5)-t图象及c(O2)-t图象,描述反应物、生成物的浓度与反应时间的关系。
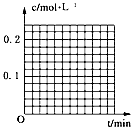
(2)数据处理是化学实验过程中非常重要的一个环节。请按下式计算化学反应速率,并将计算结果填入表中。 

(3)根据计算结果寻找用各物质表示的化学反应速率之间的关系。
参考答案: (1) (2)
(3)用各物质表示的化学反应速率之比等于化学方程式中各物质的化学计量数之比。
本题解析:
本题难度:一般
5、选择题 对于处于平衡状态的可逆反应:A(g)+2B(g) 2C(g)(正向放热)下列叙述正确的是(?) 2C(g)(正向放热)下列叙述正确的是(?)
A.增大压强,正反应速率增大,逆反应速度减小,平衡正向移动
B.升高温度,逆反应速率增大,正反应速度减小,平衡逆向移动
C.使用催化剂,平衡不移动,但可缩短达到平衡所需时间
D.扩大容器的容积,平衡逆向移动,A、B的浓度增大
参考答案:C
本题解析:略
本题难度:一般
| 