微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列反应属于吸热反应的是
A.高锰酸钾分解
B.盐酸和氢氧化钠溶液混合
C.锌放入稀硫酸中
D.碳不完全燃烧生成一氧化碳
参考答案:A
本题解析:A是放热反应,其余选项都是放热反应,答案选A。
点评:该题是基础性试题的考查,也是高考中的常见考点。试题基础性强,难度不大,侧重对学生基础知识的训练和检验。该题的关键是熟练记住常见的放热反应和吸热反应,即一般金属和水或酸反应,酸碱中和反应,一切燃烧,大多数化合反应和置换反应,缓慢氧化反应如生锈等是放热反应。大多数分解反应,铵盐和碱反应,碳、氢气或CO作还原剂的反应等是吸热反应。
本题难度:一般
2、填空题 (14分)
Ⅰ.氯碱工业中常用离子交换膜法电解制碱(如图1所示)。

(1)写出图1中阴极的电极反应式?。
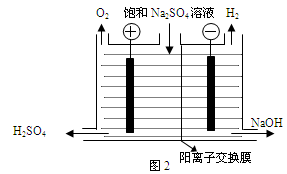
(2)已知阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过。工业上若用图2装置电解饱和Na2SO4溶液来生产纯净的NaOH和H2SO4,则该装置最主要的缺陷是?。
Ⅱ.辉钼矿(MoS2)是一种重要的矿物。图3是辉钼矿多层焙烧炉的示意图,其中1,2,3,…是炉层编号。580,600,610,…是各炉层的温度(℃)。图4给出了各炉层固体物料的物质的量百分含量。?
已知:MoS2焙烧生成1molMoO3的反应热△H1=-1011KJ/mol;MoO2氧化生成1molMoO3的反应热△H2=-154KJ/mol。试回答:

(1)验证辉钼矿焙烧生成的气体是SO2而不是SO3的方法是?。
(2)辉钼矿焙烧生成的气体能使硫酸酸化的KMnO4溶液褪色,用化学方程式表示褪色的原因?。
(3)第6炉层存在的固体物质分别是MoS2、MoO3、MoO2,则它们的物质的量之比为?。
(4)图4表明,中间炉层(4~6)可能存在一种“固体+固体→固体+…”的反应,请写出该反应的热化学反应方程式?。
参考答案:(除标注外,每空2分,共14 分)?
Ⅰ?(1)2H2O + 2e―= H2↑ + 2OH―?或2H+ + 2e―= H2↑
(2)?缺阴离子交换膜 (3分,合理答案均计分)
Ⅱ?(1)收集少量气体,将气体通入品红溶液中,观察到品红溶液褪色,加热又恢复原色?(合理答案均计分)
(2) 5SO2 + 2H2O + 2KMnO4 = K2SO4 + 2MnSO4 + 2H2SO4?
(3) 1:1:3
(4) MoS2(s) + 6MoO3(s) = 7MoO2(s) + 2SO2(g)?△H=+67KJ/mol (3分)
本题解析:I、(1)阴极是水中的氢离子放电生成氢气,电极反应式为2H2O + 2e―= H2↑ + 2OH―?
(2)该装置中缺少阴离子交换膜,不能阻止氢离子的定向移动,则阳极得不到硫酸产品;
II、(1)二氧化硫的检验使用品红溶液,收集少量气体,将气体通入品红溶液中,观察到品红溶液褪色,加热又恢复原色?;
(2)焙烧生成的气体能使硫酸酸化的KMnO4溶液褪色,实际是二氧化硫与酸性高锰酸钾溶液的氧化还原反应,化学方程式为 5SO2 + 2H2O + 2KMnO4 = K2SO4 + 2MnSO4 + 2H2SO4?
(3)根据图4可知MoS2、MoO3、MoO2的物质的量之比近似等于1:1:3;
(4)图4表明,中间炉层(4~6)中可能存在一种“固体+固体→固体+…”的反应,依据图象变化减小的是反应物,增大的是生成物,反应的化学方程式为:MoS2+6MoO3=7MoO2+2SO2;根据MoS2焙烧生成1molMoO3的反应热△H1=-1011KJ/mol;MoO2氧化生成1molMoO3的反应热△H2=-154KJ/mol及盖斯定律计算出MoS2+6MoO3=7MoO2+2SO2的反应热为+67KJ/mol ,所以该反应的热化学方程式为MoS2(s) + 6MoO3(s) = 7MoO2(s) + 2SO2(g)?△H=+67KJ/mol
本题难度:一般
3、选择题 下列对化学反应的认识错误的是? ( )。
A.会引起化学键的变化
B.会产生新的物质
C.必然引起物质状态的变化
D.必然伴随着能量的变化
参考答案:C
本题解析:化学反应的本质是化学键的断裂和形成,表现为有新物质生成,并伴随着能量的变化,而化学变化中的反应物和生成物的状态在反应前后可能相同,也可能不相同,故正确答案为C。
本题难度:简单
4、选择题 下列关于化学反应的说法中不正确的是
A.能量变化是化学反应的基本特征之一
B.能量变化可以体现为热能、光能、电能等
C.化学反应中能量变化的大小与反应物的多少无关
D.化学反应中的能量变化主要原因是化学键的断裂和形成
参考答案:C
本题解析:略
本题难度:简单
5、选择题 工业生产水煤气的反应为:C(s)+H2O(g)→CO(g)+H2(g)-131.4kJ下列判断正确的是( )
A.反应物能量总和大于生成物能量总和
B.CO(g)+H2(g)→C(s)+H2O(l)+131.4?kJ
C.水煤气反应中生成1?mol?H2(g)吸收131.4?kJ热量
D.水煤气反应中生成1体积CO(g)吸收131.4?kJ热量
参考答案:A、该反应是吸热反应,故反应物的总能量小于生成物的总能量,故A错误;
B、反应中是液态水,根据题干热化学方程式判断CO(g)+H2(g)=C(s)+H2O(l)△H<-131.4 kJ/mol,故B错误;
C、由题干反应可知生成1mol氢气吸收的热量为131.4?KJ,故C正确;
D、由题干反应可知生成1mol氢气吸收的热量为131.4?KJ,1体积氢气物质的量不是1mol,故D错误;
故选C.
本题解析:
本题难度:一般