微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 氨在工农业生产中应用广泛。在压强为30MPa时,合成氨平衡混合气体中NH3的体积分数如下:
温度/°C
| 200
| 300
| 400
| 500
| 600
|
氨含量/%
| 89.9
| 71.0
| 47.0
| 26.4
| 13.8
|
请回答:
(1)根据表中数据,结合化学平衡移动原理,说明合成氨反应是放热反应的原因是?。
(2)根据-4,合成氨的热化学方程式是?。

(3)在一定温度下,将2molN2和6molH2通入到体积为1L的密闭容器中,发生反应
N2+3H2? 2NH3,2min达到平衡状态时,H2转化率是50%,则用H2表示该反应的平均速率v(H2)=?;该温度下的平衡常数K=?(用分数表示);俗使K增大,可以采取的措施是?。
2NH3,2min达到平衡状态时,H2转化率是50%,则用H2表示该反应的平均速率v(H2)=?;该温度下的平衡常数K=?(用分数表示);俗使K增大,可以采取的措施是?。
(4)从化学平衡移动的角度分析,提高H2转化率可以采取的措施是?(选填序号字母)
a.及时分离出NH3?b.升高温度
c.增大压强? d.使用催化剂
参考答案:
本题解析:略
本题难度:一般
2、选择题 下列说法中正确的是
A.凡是放热反应都是自发的,吸热反应都是非自发的
B.在反应A(g)+3B(g)=2C(g)+2D(g)的速率测定实验中,分别?测得反应速率如下:v(A)= 0.15mol・L―1・s―1 ,v(C)= 0.3 mol・L―1・s―1 ,则用C来表示反应进行的速率更快。
C.如图所示,在一U型管中装入含有紫色石蕊试液的Na2SO4溶液,通直流电,一段时间后U型管内会形成一个倒立的三色“彩虹”,从左到右颜色的次序是.红、紫、蓝

D.反应HCl ( aq ) + NaOH ( aq ) =" NaCl" ( aq ) + H2O ( l ) △H < 0,在理论上能用于设计原电池?
参考答案:C
本题解析:略
本题难度:简单
3、填空题 (1) 纳米级Cu2O由于具有优良的催化性能而受到关注。已知:
2Cu(s)+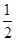 O2(g) ="==" Cu2O(s)? ΔH=-169kJ・mol-1,
O2(g) ="==" Cu2O(s)? ΔH=-169kJ・mol-1,
C(s)+ 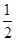 O2(g) ="==" CO(g) ?ΔH=-110.5kJ・mol-1,
O2(g) ="==" CO(g) ?ΔH=-110.5kJ・mol-1,
2Cu(s)+ O2(g)===2?CuO(s)?ΔH=-314kJ・mol-1
则工业上用炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式为
?。
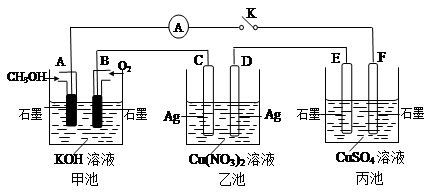
(2)某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。
请回答下列问题:
(1)甲池为?(填“原电池”、“电解池”或 “电镀池”),A电极的电极反应式为?。
(2)丙池中F电极为??(填“正极”、“负极”、“阴极”或“阳极”),该池的总反应方程式为?。
(3)当池中C极质量减轻10.8 g时,甲池中B电极理论上消耗O2的体积为?mL(标准状况)。
(4)一段时间后,断开电键K,下列物质能使乙池恢复到反应前浓度的是?(填选项字母)。
A.Cu
B.CuO
C.Cu(OH)2
D.Cu2(OH)2CO3
参考答案:(1)C(s) + 2CuO (s)= Cu2O(s) + CO(g) 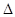 H =+34.5kJ・mol.-1(3分)
H =+34.5kJ・mol.-1(3分)
(2)①原电池 (1分)? CH3OH + 8OH--6e- = CO32-+ 6H2O(2分)
②阴极(1分)? 2CuSO4+ 2H2O 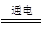 ?2H2SO4 + 2Cu + O2↑(2分)
?2H2SO4 + 2Cu + O2↑(2分)
③560(2分)
④A(2分)
本题解析:(1)工业上用炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式为
C(s) + 2CuO (s)= Cu2O(s) + CO(g) 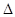 H =a,
H =a,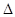 H 的计算如下,C(s)+
H 的计算如下,C(s)+ 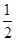 O2(g) ="==" CO(g) 减去2Cu(s)+ O2(g)===2?CuO(s) 再加上2Cu(s)+
O2(g) ="==" CO(g) 减去2Cu(s)+ O2(g)===2?CuO(s) 再加上2Cu(s)+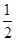 O2(g) ="==" Cu2O(s) 可以得到C(s) + 2CuO (s)= Cu2O(s) + CO(g) ,所以
O2(g) ="==" Cu2O(s) 可以得到C(s) + 2CuO (s)= Cu2O(s) + CO(g) ,所以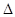 H =-110.5+314-169=+34.5kJ・mol.-1,所以工业上用炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式为
H =-110.5+314-169=+34.5kJ・mol.-1,所以工业上用炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式为
C(s) + 2CuO (s)= Cu2O(s) + CO(g) 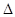 H =+34.5kJ・mol.-1;
H =+34.5kJ・mol.-1;
(1)由图可以知道,甲池为原电池,A电极为负极,该电极反应式为CH3OH + 8OH--6e- = CO32-+ 6H2O;(2)丙池中F电极与电池的负极连接,所以F电极为阴极,丙电池为电解池,该电池的总的反应式为2CuSO4+ 2H2O 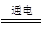 ?2H2SO4 + 2Cu + O2↑;(3)C极中,Ag溶解,所以当池中C极质量减轻10.8 g时,即通过的电子数为10.8/108=0.1mol,所以B电极理论上消耗O2的体积=0.1/4×22.4×1000=560mL;(4)一段时间后,断开电键K,乙池在电解的过程中引入了银离子,有一部分铜离子在电极上析出,所以加入Cu可以恢复到原来的浓度,故本题的答案选择A。
?2H2SO4 + 2Cu + O2↑;(3)C极中,Ag溶解,所以当池中C极质量减轻10.8 g时,即通过的电子数为10.8/108=0.1mol,所以B电极理论上消耗O2的体积=0.1/4×22.4×1000=560mL;(4)一段时间后,断开电键K,乙池在电解的过程中引入了银离子,有一部分铜离子在电极上析出,所以加入Cu可以恢复到原来的浓度,故本题的答案选择A。
点评:本题考查了热化学方程式的书写、原电池、电解池,这些考点是高考考查的重点和难点,本题有一定的综合性,难度适中。
本题难度:一般
4、选择题 下列有关能量转换的说法正确的是
[? ]
A.煤燃烧是热能转化为化学能的过程
B.化石燃料和植物燃料燃烧时放出的热量均来源于太阳能
C.动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程
D.植物通过光合作用将CO2转化为葡萄糖是太阳能转变成热能的过程
参考答案:B
本题解析:
本题难度:简单
5、选择题 下列关于化学反应与能量的说法正确的是( )
A.中和反应是吸热反应
B.燃烧属于放热反应
C.Ba(OH)2?8H2O晶体与NH4Cl晶体反应属于放热反应
D.反应物总能量与生成物总能量一定相等
参考答案:A、酸碱发生中和反应时向外界释放能量,所以中和反应都是放热反应,故A错误;
B、物质燃烧时向外界释放能量属于放热反应,故B正确;
C、Ba(OH)2?8H2O晶体与NH4Cl晶体反应时要吸收能量,所以属于吸热反应,故C错误;
D、化学反应中有物质变化一定伴随有能量变化,反应物总能量与生成物总能量一定不相等,故D错误;
故选B.
本题解析:
本题难度:简单