微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (17分)(1)浓硫酸与木炭粉在加热条件下反应的化学方程式是:?。
(2)试用下图所列各装置设计一个实验,来验证上述反应所产生的各种产物。
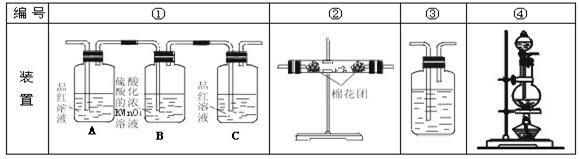 →这些装置的连接顺序(按产物气流从左至右的方向)是(填装置的编号):?→?→?→?。→??
→这些装置的连接顺序(按产物气流从左至右的方向)是(填装置的编号):?→?→?→?。→??
(3)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色。A瓶溶液的作用是?,B瓶溶液的作用是?,C瓶溶液的作用是?。
(4)装置②中所加固体药品是?,可验证的产物是?,确定装置②在整套装置中位置的理由是?。
(5)装置③中所盛溶液是?,可验证的产物是?。
参考答案:(1)2H2SO4(浓)+C=====CO2↑+2H2O↑+2SO2↑(3分)(2)④→②→①→③(2分)(3)验证产物气流中有SO2?将产物气流中SO2全部氧化吸收?确认产物气流中SO2已被B瓶溶液全部吸收(每空2分*3=6分)
(4)无水硫酸铜(或变色硅胶)(1分)?水蒸气(1分)?由于产物气流通过①、③时会带出水蒸气,所以②必须在①、③之前(2分)(5)澄清石灰水(或其他合理答案)(1分)? CO2(二氧化碳)(1分)
本题解析:(2)实验目的:验证浓硫酸与木炭粉在反应的产物中有CO2、SO2、H2O
通常:CO2用澄清石灰水检验(因两者反应会生成CaCO3白色沉淀),SO2用品红溶液检验(因SO2有漂白性,能使品红褪色),H2O用无水CuSO4白色粉末检验(因两者反应会生成蓝色晶体:CuSO4・5H2O);
三者的检验顺序:应先检验H2O(因检验CO2、SO2时都要用到水溶液,会带入水蒸气,则干扰产物中水的检验),再检验SO2(因SO2也能澄清石灰水变浑浊,故在检验CO2前排除SO2),最后检验CO2;
由上述分析,得:装置的连接顺序为④→②→①→③
④为浓硫酸与木炭粉的反应装置,
②中盛放有无水CuSO4白色粉末,作用:检验产物水,现象:变蓝
①:A中品红溶液的作用:检验SO2,现象:褪色
B中酸性KMnO4的作用:利用氧化还原反应除去SO2,
C中品红溶液的作用:检验SO2是否除尽,以排除对CO2检验的干扰,现象:不退色
③中盛放澄清石灰水,作用:检验CO2,现象:出现白色浑浊
本题难度:一般
2、填空题 (7分)现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-、SO42-、和NO3-的相互分离。相应的实验过程可用下图表示:
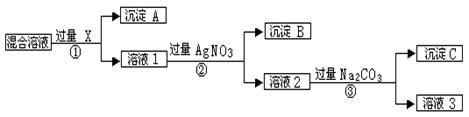
请回答下列问题:
⑴写出实验流程中下列物质的化学式
试剂X :??沉淀A:??沉淀B:?
⑵上述实验流程中加入过量的Na2CO3的目的是?。
⑶按此实验方案得到的溶液3中肯定含有?(填化学式)杂质。
参考答案:(7分)⑴BaCl2 [或Ba(NO3)2]? BaSO4? AgCl? (每个1分)
⑵除去过量的Ba2+、Ag+(2分)⑶Na2CO3 (2分)
本题解析:(1)根据步骤②可知,B是氯化银,所以步骤①中的试剂是氯化钡,则A是硫酸
钡。
(2)溶液2中含有Ag+和Ba2+,所以碳酸钠的作用是除去溶液中的Ag+和Ba2+。
(3)碳酸钠是过量的,所以溶液3中一定含有碳酸钠。
本题难度:一般
3、填空题 鉴别蛋白质溶液和食盐溶液的试剂是_______________;分离提纯蛋白质的方法是_________________。
参考答案:浓HNO3;盐析
本题解析:
本题难度:一般
4、选择题 为提纯下列物质(括号内为杂质)选用的试剂和分离方法都正确的是
?
| 物质
| 试剂
| 分离方法
|
①
| 硝酸钾(氯化钠)
| 蒸馏水
| 降温结晶
|
②
| 二氧化碳(氯化氢)
| 饱和碳酸钠溶液
| 洗气
|
③
| 乙醇(水)
| 金属钠
| 蒸馏
|
④
| NaCl溶液(Na2S)
| AgCl
| 过滤
|
A.①③?B.①④?C.只有②?D.③④
参考答案:B
本题解析:①硝酸钾混有氯化钠,氯化钠溶解度随温度变化不大,硝酸钾溶解度随温度升高增大,利用冷却热饱和溶液的方法得到硝酸钾晶体;故①正确;②二氧化碳和碳酸钠溶液也发生反应,应该用饱和碳酸氢钠溶液除去CO2中的氯化氢气体,故②错误;③乙醇和水都和钠发生反应,不能除去水,应该利用新制生石灰借助于蒸馏除去乙醇中的水,故③错误;④加入氯化银是难溶物,但硫化银更难溶,可以和硫化钠反应实现沉淀转化Na2S+2AgCl=Ag2S+2NaCl,乙醇可以实现除杂,故④正确,答案选B。
本题难度:一般
5、选择题 下列有关物质检验或鉴别的说法正确的是 ①检验某未知溶液中是否含有SO42-,通常是先向试液中滴加适量稀盐酸,然后再滴加BaCl2溶液;②鉴别氯化钠溶液和氯化钾溶液时,常用玻棒分别蘸取试液放在火焰上灼烧,直接观察火焰的颜色;③向某溶液中加入稀氢氧化钠溶液,若末嗅到氨的气味,则说明该溶液中无铵盐;④某白色固体与强酸溶液接触产生大量无色气体,则该固体一定是碳酸钙;⑤鉴别胶体与溶液最好的方法是观察有无“丁达尔现象”。
A.①②
B.②③
C.①⑤
D.④⑤
参考答案:C
本题解析:①⑤正确;②鉴别氯化钠溶液和氯化钾溶液时,不能直接观察火焰的颜色,要用蓝色的钴玻璃观察;③检验铵根离子,要用浓氢氧化钠溶液;④某白色固体与强酸溶液接触产生大量无色气体,则该固体不一定是碳酸钙,也可能是碳酸钡、碳酸钠、碳酸氢钠等。
点评:属于简单题。
本题难度:一般