��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����ʱ��M(OH)2(S)  M2+(aq)+2OH-(aq) ?Ksp=a��c(M2+)="b" mol��L-1ʱ����Һ��pH���ڣ�?��
M2+(aq)+2OH-(aq) ?Ksp=a��c(M2+)="b" mol��L-1ʱ����Һ��pH���ڣ�?��
A��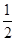 lg(
lg(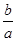 )
)
B��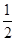 lg(
lg( )
)
C��14+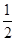 lg(
lg( )
)
D��14+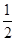 lg(
lg(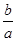 )
)
�ο��𰸣�C
�������������Ksp="a=" c(M2+)��c(OH-)2��c(M2+)="b" mol��L-1�����c(OH-)2=( )�������Ǽ��Ի����������c(OH-)������ˮ�����ӻ��������c(H+)���������Һ��pH=14+
)�������Ǽ��Ի����������c(OH-)������ˮ�����ӻ��������c(H+)���������Һ��pH=14+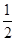 lg(
lg( )��
)��
�����㶨λ��ˮ�����ӻ���KSP��pH����
�����Ѷȣ���
2��ѡ���� ��Ca(OH)2��������ˮ�У�һ��ʱ���ﵽƽ�⣺Ca(OH)2(s)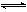 Ca2++2OH��
Ca2++2OH��
��������Һ�м���������ʯ�Һ����¶ȱ��ֲ��䣬����˵����ȷ���ǣ�?��?
A����Һ��Ca2+��Ŀ����
B����Һ��Ca2+��Ŀ����
C��c(Ca2+)����
D��c(Ca2+)����
�ο��𰸣�D
�����������Ca(OH)2��������ˮ�У��ﵽ�����ܽ�ƽ�����Һ���DZ�����Һ���ټ�����ʯ�ң���Ӧ����ˮ����ԭ��Һ������һ�����������ƹ��壬Ca2+��Ŀ���٣�����Һ���DZ�����Һ��������Ũ�Ȳ��䡣��ѡD
�����Ѷȣ�һ��
3��ѡ���� ����˵����ȷ����
A������ȼ��ʱ��ȫ���Ļ�ѧ��ת��Ϊ����
B������ʯ��ˮ�м���һ������ʯ�ң�������Һ��pH����
C����AgCl����Һ�м���KI��Һ����ɫ����ת��Ϊ��ɫ������˵���ܽ��AgCl<AgI
D����AgCl����Һ�еμ�Ũ��ˮ�������ܽ⣬˵��AgCl���ܽ�ƽ�������ƶ�
�ο��𰸣�D
�����������
�����Ѷȣ�һ��
4������� �������ԭ�����ش����и�С�⣺
����֪NaHSO4��ˮ�еĵ��뷽��ʽΪNaHSO4��Na++ H++ SO42- ��
��1����NaHSO4��Һ��c��H+��_________c��OH-��+ c��SO42-�����������������������ͬ��������������������������Һ��ȡ���ᱵ������Һ��SO42-��ȫ��������Ӧ����Һ��pH___________7��2����20mLpH=2��NaHSO4��Һ��μ��뵽20mL 0.1 mol��L-1Na2CO3��Һ�У���Һ�з�����Ӧ�����ӷ���ʽΪ��_________________����˷�Ӧ�����Һ�еμ� 0.001 mol��L-1BaCl2��Һ�����������ij�����_____________��[KSP��BaSO4��=1.1��10-10mol2��L-2 ��KSP��BaCO3��=5.1��10-9mol2��L-2]
����֪����25ʱ H2O H++OH-? KW=10-14��CH3COOH
H++OH-? KW=10-14��CH3COOH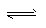 H++CH3COO- ?Ka=1.8��10-5
H++CH3COO- ?Ka=1.8��10-5
��3��������ˮ���ƽ�ⳣ��Kh�ı���ʽΪ___________ ���������¶�ʱ��Kh��___________���������С�������䡱����
��4��0��5mol��L-1��������ҺpHΪm����ˮ��ij̶ȣ���ˮ��Ĵ�������ԭ�д����Ƶı�ֵ��Ϊa��1mol��L-1��������ҺpHΪn��ˮ��ij̶�Ϊb����m��n�Ĺ�ϵΪ__________��a��b�Ĺ�ϵΪ________������ڡ���С�ڡ������ڡ�����
��5��0��9mol��L-1��������Һ�У�OH-��= mol��L-1 ��ij��Һ�к�Mg2+��Cd2+��Zn2+�������ӵ�Ũ�Ⱦ�Ϊ0.01mol��L-1�������м����������ƣ�ʹ��Ũ��Ϊ0.9mol��L-1���������ֽ���������___________�����ɳ�����ԭ����______________����KSP��Mg��OH��2��=1.8��10-11��KSP��Zn��OH��2��=1.2��10-17�� KSP��Cd��OH��2��=2.5��10-14��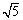 =2.2��
=2.2��
�ο��𰸣���1���� ������ ��
��2��CO32-+H+ === HCO3-?�� BaSO4
��3��Kh=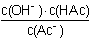 ������
������
��4��С�ڣ�����
��5����OH-��=2.2��10-5mol��L-1?Cd2+��Zn2+��
��OH-��=2.2��10-5mol��L-1����
��M2+�ݣ�OH-��2=5��10-12��mol��L-1��
3.5��10-12��KSP��Mg��OH��2��=1.8��10-11
5��10-12����KSP��Zn��OH��2��=1.2��10-17
5��10-12����KSP��Cd��OH��2��=2.5��10-14
���������
�����Ѷȣ�����
5������� ������ʴ�Ըߣ��ڸ��к����ﵽ12%��Ϊ����֣���ҵ��ұ��������Ҫ������ͼ��ʾ��
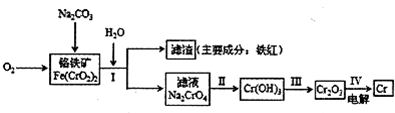
�Իش���������
��1�����粽���ķ�Ӧ����ʽΪ��
8Na2CrO4+6Na2S+23H2O��8Cr��OH��3��ʮ3Na2S2O3ʮ22NaOH
�÷�Ӧ����������______���ѧʽ��������?lmolCr��OH��3ʱת�Ƶ��ӵ����ʵ���Ϊ______mol��
��2������IV�е��Cr2O3��������ӦʽΪ______����ʱCr2O3?��״̬Ϊ______��
��3�������£�������������ϡ���ᡢϡ���ᣬ��������Ũ���ᣮ�䲻����Ũ�����ԭ�������______��
��4�����磺2CrO42-+2H+
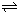
Cr2O72-+H2O
��25��C��KSP��Ag2Cr2O4��=1.12��10-12��KSP��Ag2Cr2O7��=2��10-7����Na2Cr2O7��Һ�м���AgNO3��Һ������ֻ����һ��ש��ɫ�������ó����Ļ�ѧʽ��______��
�ڽ�wg����Na2CrO4��������ˮ���lL��Һ������Һ���й����ӵ�Ũ�ȣ�mol?L-1����pH�Ĺ�ϵ���±���
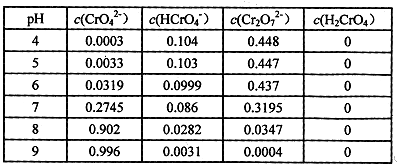
���ϱ���֪��
��Ҫʹ��Һ��CrO42-�����ﵽ���Ӧ������Һ��pH______���ã�������=��������ݱ�ʾ����
�� w g����Na2CrO4�����ʵ���n=______������ѧ����ʽ��ʾ����
�ο��𰸣���1��Cr���ϼ۴�+6��+3�����ϼ۽���3����Na2CrO4��������������?lmolCr��OH��3ʱת�Ƶ��ӵ����ʵ���Ϊ 3mol��
�ʴ�Ϊ��Na2CrO4 ?3��
��2������״̬ʱ��Cr2O3?�������룺Cr2O3�T2Cr3++3O2-�����Cr2O3��������ӦʽΪ��2O2--4e-�TO2����
�ʴ�Ϊ��2O2--4e-�TO2�� Һ̬��������̬����
��3��������������ϡ���ᡢϡ���ᣬ��������Ũ���ᣬ˵������Ũ�������������ܵı���Ĥ��
�ʴ�Ϊ������������������Ĥ�������ۻ�����
��4������KSP��Ag2Cr2O4��=1.12��10-12��KSP��Ag2Cr2O7��=2��10-7�������ܽ�ƽ�����ܽ��С�����С�ķ���ת����������Na2Cr2O7��Һ�м���AgNO3��Һ������ֻ����һ��ש��ɫ�������ó���Ϊ��Ag2CrO4��
�ʴ�Ϊ��Ag2CrO4��?
?�ڹ۲�������ݿ�֪��PH����c��CrO42-������PH=9ʱ��c��CrO42-��=0.996����Ҫʹ��Һ��CrO42-�����ﵽ���Ӧ������Һ��pH��9��
��Ԫ�ش�����ʽ�У�CrO42-��Cr2O72-��HCrO4-�����������غ�w g����Na2CrO4�����ʵ���Ϊ��n�Tn��CrO42-��+c��Cr2O72-��+n��HCrO4-����
�ʴ�Ϊ����9��n��CrO42-��+c��Cr2O72-��+n��HCrO4-����
���������
�����Ѷȣ�һ��