微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 下图所示为血红蛋白和肌红蛋白的活性部分--血红素的结构式。
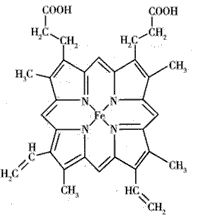
请回答下列问题:
(1)血红素中含有C、H、O、N、Fe五种元素,C、N、O三种元素的第一电离能由小到大的顺序是___ 写出基态Fe原子的核外电子排布式___。
(2)血红素中N原子的杂化方式为___,在下面的方框内用“→”标出Fe2+的配位键。

(3)铁有δ、γ、α三种同素异形体,γ晶体晶胞中所含有的铁原子数为___,δ、α两种晶胞中铁原子的配位数之比为____。

2、填空题 按要求填写表格。

3、简答题 超细铜粉主要应用于导电材料、催化剂等领域中.超细铜粉的某制备方法如下:

试回答下列问题:
(1)下列关于[Cu(NH3)4]SO4的说法中,正确的有______.(填字母序号)
A.[Cu(NH3)4]SO4中所含的化学键有离子键、极性键和配位键
B.[Cu(NH3)4]SO4含有NH3分子,其水溶液中也含有NH3分子
C.[Cu(NH3)4]SO4的组成元素中第一电离能最大的是氧元素
D.[Cu(NH3)4]SO4的外界离子的空间构型为正四面体
(2)NH4CuSO3中的金属阳离子的核外电子排布式为:______.
(3)SO
离子中S硫原子的杂化方式为______,与其互为等电子体的一种分子的分子式是______.
(4)NH3易液化的原因是______.
(5)如图是铜的某种氧化物的晶胞结构示意图,由此可确定该氧化物的化学式为______.
(6)NH4CuSO3与硫酸微热时除得到超细铜粉外,还可看到溶液变蓝,同时有使品红褪色的气体.则该反应的离子方程式为______.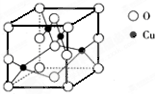
4、填空题 (三选一)【物质结构与性质】
三氟化氮是一种无色、无味、无毒且不可燃的气体,在半导体加工、太阳能电池制造和液晶显示器制造中得到广泛应用。NF3是一种三角锥型分子,键角102°,沸点-129℃;可在铜的催化作用下由F2和过量NH3反应得到。
(1)写出制备NF3的化学反应方程式:__________。
(2)NF3的沸点比NH3的沸点(-33℃)低得多的主要原因是_______________
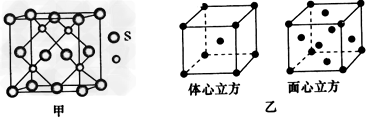
(3)与铜属于同一周期的过渡元素,且各电子层均无未成对电子,该元素的基态原子核外电子排布式为____________;若该元素的硫化物具有如图甲所示的晶胞结构,则该晶胞中S2-的配位数为__________。若该金属单质的晶体在不同温度下有两种不同的堆积方式,其晶胞结构分别如图乙所示,则两晶胞中实际含有的原子个数之比为____________。
(4)根据下列五种元素的第一至第四电离能数据(单位:kJ/mol),回答下面各题
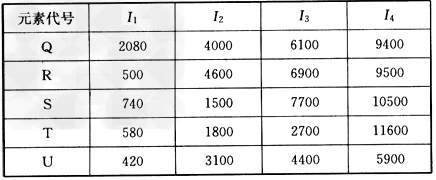
①在周期表中,最可能处于同一族的是______和_______。
②T元素最可能是_____区元素。若T为第二周期元素,E是第三周期元素中原子半径最小的元素,则T、E形成化合物的空间构型为_______,其中心原子的杂化方式为______。
5、填空题 水是自然界中普遍存在的一种物质,根据下列信息回答问题:
(1)氧原子基态时价层电子的电子排布图为_____________。
(2)已知2H2O?=?H3O+?+?OH-,H3O+的立体构型是___________________,中心原子的杂化类型是__________________。
(3)s轨道与s轨道重叠形成的共价键可用符号表示为:δs-s,p轨道与p轨道以“头碰头”方式重叠形成的共价键可用符号δp-p,则H2O分子含有的共价键用符号表示为_________。
(4)试比较同主族元素的氢化物H2O、H2S和H2Se的稳定性和沸点高低,并说明理由。稳定性_____________理由______________。沸点________________理由:______________。