��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��֪2Fe2+��Br2��2Fe3+��2Br������100mL��FeBr2��Һ��ͨ���״���µ�Cl2 3.36L����ַ�Ӧ������Һ��Cl����Br�������ʵ���Ũ����ȣ���ԭFeBr2��Һ�����ʵ���Ũ��Ϊ
A��2 mol/L
B��1 mol/L
C��0.4 mol/L��
D��0.2 mol/L
�ο��𰸣�A
�����������ԭ��Fe2+��Br-������ͨ�������ȷ�����Ӧ2Fe2++Cl2�T2Fe3++2Cl-��Fe2+��Ӧ��ϣ�ʣ��������ٷ�Ӧ��Ӧ2Br-+Cl2�TBr2+2Cl-����Һ�к���Br-��˵��������ȫ��Ӧ��Cl2�����ʵ���Ϊ3.36L��22.4L/mol=0.15mol����Br-û�з�Ӧ����c��FeBr2��=0.5n��Br-��=0.15mol��0.15molFe2+ֻ������0.075mol��Cl2�����в���Br-�μӷ�Ӧ��
��FeBr2�����ʵ���Ϊx����n��Fe2+��="x" mol��n��Br-��="2x" mol��δ��Ӧ��n��Br-��="0.3" mol���μӷ�Ӧ��n��Br-��=��2x-0.3��mol�����ݵ���ת���غ���x��1+[2x-0.3]��1=0.15mol��2�����x="0.2" mol������ԭFeBr2��Һ�����ʵ���Ũ��Ϊ0.2mol��0.1L=2mol/L��
��ѡA��
���������鷴Ӧ����ʽ�ļ��㣬�Ѷ��еȣ������ԭ��Fe2+��Br-��ͨ���Cl2��������Fe2+����Fe2+ȫ���������������Br-���ж�Br-�Ƿ���ȫ��Ӧ���ǽ���Ĺؼ���
�����Ѷȣ���
2��ѡ���� ��ȡm gþ���Ͻ���һ��Ũ�ȵ�ϡ������ǡ����ȫ�ܽ�(����Ļ�ԭ����ֻ��NO)����Ӧ��Ļ����Һ�еμ�b mol��L��1 NaOH��Һ�����μӵ�V mLʱ���õ���������ǡ��Ϊ���ֵn g���������йظ�ʵ���˵������ȷ����(����)��
�ٳ�����OH��������Ϊ(n��m)g
��ǡ���ܽ����Һ�е�NO3�������ʵ���Ϊ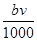 ?mol
?mol
�۷�Ӧ������ת�Ƶĵ�����Ϊ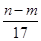 ?mol
?mol
�ܱ�״��������NO�����Ϊ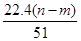 L
L
����Ͻ�Ӧ����������ʵ���Ϊ(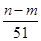 ��
��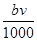 )mol
)mol
A��5��
B��4��
C��3��
D��2��
�ο��𰸣�A
��������������漰�ķ�Ӧ��Al��4HNO3(ϡ)=Al(NO3)3��NO����2H2O��3Mg��8HNO3(ϡ)=3Mg(NO3)2��2NO����4H2O��Al(NO3)3��3NaOH=Al(OH)3����3NaNO3��Mg(NO3)2��2NaOH=Mg(OH)2����2NaNO3�����Ͻ�ǡ���ܽ�ʱ����Һ�е�NO3����Na�������ʵ�����ȣ�n(NO3��)��n(NaOH)��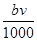 ?mol���ʢ���ȷ�������������ʱ�����ɵ�n g����Ϊ����������������þ�����������غ㶨�ɣ�����þ����Ԫ�ص���������m g�����Գ�����������������Ϊ(n��m)g����Ӧ������ת�Ƶĵ������ʵ���n(e��)��n(OH��)��
?mol���ʢ���ȷ�������������ʱ�����ɵ�n g����Ϊ����������������þ�����������غ㶨�ɣ�����þ����Ԫ�ص���������m g�����Գ�����������������Ϊ(n��m)g����Ӧ������ת�Ƶĵ������ʵ���n(e��)��n(OH��)��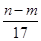 mol���ʢ٣�����ȷ�����ݵ��ӵ�ʧ�غ�֪����״����V(NO)��
mol���ʢ٣�����ȷ�����ݵ��ӵ�ʧ�غ�֪����״����V(NO)��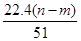 ?L���ʢ���ȷ���μӷ�Ӧ���������������ã����������õ�����(����������)�����ʵ������������Ƶ����ʵ�������
?L���ʢ���ȷ���μӷ�Ӧ���������������ã����������õ�����(����������)�����ʵ������������Ƶ����ʵ�������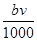 ?mol��������������������ʵ�������NO�����ʵ�������
?mol��������������������ʵ�������NO�����ʵ�������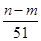 ?mol�����ԣ���Ͻ�Ӧ����������ʵ���Ϊ(
?mol�����ԣ���Ͻ�Ӧ����������ʵ���Ϊ(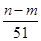 ��
��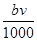 )mol���ʢ���ȷ��
)mol���ʢ���ȷ��
�����Ѷȣ�һ��
3��ѡ���� �ø�������(Na2FeO4)��ˮ�����dz�������ˮ�������¼�������֪��Ӧ��Fe2O3��3Na2O2=2Na2FeO4��Na2O������˵����ȷ����
A��Na2O2�������������ǻ�ԭ��
B��Na2FeO4���������������ǻ�ԭ����
C��3 mol Na2O2������Ӧ����12 mol����ת��
D����Na2FeO4��FeΪ��4�ۣ�����ǿ�����ԣ�������ɱ��
�ο��𰸣�B
�������������Ŀ�еķ�Ӧ����ʽ��������֪��Na2O2������������Ԫ���ɣ�1�۽��͵���2�ۣ�A������Ԫ����Fe2O3�еģ�3�����ߵ�Na2FeO4�еģ�6�ۣ�Na2FeO4���������������ǻ�ԭ���B��ȷ��D����C��3 mol Na2O2������Ӧ����6 mol����ת�ơ���ѡB��
�����Ѷȣ�һ��
4������� ��֪��ϡ�����У�KBrO3��KI�ܷ������·�Ӧ����δ��ƽ����
BrO3-+H++I-��I03-+Br2+H20?I03-+H++Br-��Br2+I2+H20
��1���ԱȽ�������������BrO3-��Br2��I03-��I2�����Ե�ǿ����______��______��______��______��
��2����ƽ���з�Ӧ�����ӷ���ʽ��
______BrO3-+______H++______I-��______I2+______Br-+______H20
��Ӧ�е���������______����������Ԫ����______��
��3����ϡ�����У���KI��KBrO3�����ʵ���֮��6��1.1��Ӧ�����ɵIJ�����H20��______��______��
______?���û�ѧʽ�����ӷ��ű�ʾ����
�ο��𰸣���1���ڷ�ӦBrO3-+H++I-��I03-+Br2+H20�У������ԣ�BrO3-��I03-���ڷ�ӦI03-+H++Br-��Br2+I2+H20�У�
�����ԣ�I03-��Br2���������ԣ�Br2��I2���������ԣ�BrO3-��I03-��Br2��I2���ʴ�Ϊ��BrO3-��I03-��Br2��I2��
��2����Ӧ��BrO3-���ϼ���+5�۽�Ϊ-1�ۣ�I-���ϼ���-1������Ϊ0�ۣ������ڷ�Ӧ�е�ʧ������Ŀ��ȣ����ж��ߵļ�������ֵΪ1��6���������ӷ���ʽ����غ㣬����ƽ�ⷽ��ʽΪ6I-+BrO3-+6H+=3I2+Br-+3H20������������ΪBrO3-����ԭ��ΪI-���ʴ�Ϊ��1��6��6��3��1��3��BrO3-��I-��
��3��I�ļ�̬��-1��0��+5��+7��Br�ļ�̬Ҳ��-1��0��+5��+7��KI��KBrO3�����ʵ���֮��6��1.1��Ӧ��I-��������+5����+7�ۣ���ô���ղμӷ�Ӧ��KI��KBrO3�����ʵ���֮��6��1.1���Ǿ��Բ����ܵģ�����I-ֻ�ܱ�������0�ۣ���I2��6molI-��������I2ʧȥ6mol���ӣ�Br���ֻ���ܱ���ԭ��0�ۣ�����-1�ۣ���Ϊ0�ۣ���1.1molKBrO3�õ���5.5mol����Ϊ-1�ۣ���1.1molKBrO3�õ���6.6mol��6mol������5.5��6.6֮�䣬˵��KBrO3����ԭΪ���ּ�̬��0��-1����ΪBr2��Br-���ʴ�Ϊ��I2��Br2��Br-����
���������
�����Ѷȣ�һ��
5��ѡ���� a mol FeS��b mol FeOͶ�뵽VLc mol��Lϡ�����г�ַ�Ӧ������NO���壬���ó�����Һ�ɷֿɿ�����Fe(NO3)3��H2SO4�Ļ��Һ����Ӧ��δ����ԭ���������Ϊ
�٣�a��b����63g?�ڣ�a��b����189g?�ۣ�a��b��mol?��(cV��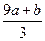 )mol
)mol
A���٢�
B���ڢ�
C���ڢ�
D���٢�
�ο��𰸣�B
�����������
�����Ѷȣ�һ��