微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 某研究小组设计如下工艺路线提纯工业碳酸钠。已知工业碳酸钠(纯度约为98%)中含有Ca2+、Mg2+、Fe3+、Cl-、和SO42―等杂质。
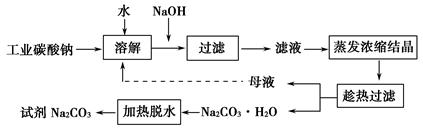
Ⅰ.碳酸钠的饱和溶液在不同温度下析出的溶质如下图所示:
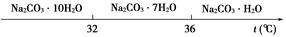
Ⅱ.有关物质的溶度积如下:
物质
| CaCO3
| MgCO3
| Ca(OH)2
| Mg(OH)2
| Fe(OH)3
|
Ksp
| 4.96×10-9
| 6.82×10-6
| 4.68×10-6
| 5.61×10-12
| 2.64×10-39
|
?
根据所给信息,回答下列问题:
(1)加入NaOH溶液时发生的离子方程式为___________________________。
向含有Mg2+、Fe3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8时,c(Mg2+)∶c(Fe3+)=__________________________________________
(2)“趁热过滤”时的温度应控制在____________________________________
(3)有人从“绿色化学”的角度设想将“母液”沿流程中虚线所示进行循环使用。请你分析实际工业生产中是否可行__________________,并说明理由_______________________________________
参考答案:(1)Fe3++3OH-=Fe(OH)3↓、MgCO3+2OH-=Mg(OH)2+CO32―、Mg2++2OH-=Mg(OH)2↓(三个答出两个即可)  ×1021或2.125×1021
×1021或2.125×1021
(2)高于36 ℃
(3)不可行 若“母液”循环使用,则溶液c(Cl-)和c(SO42―)增大,最后所得产物Na2CO3中混有杂质
本题解析:(1)工业碳酸钠中含有的Mg2+、Fe3+都可以与OH-反应。当溶液pH=8时,
c(OH-)=10-6 mol・L-1,
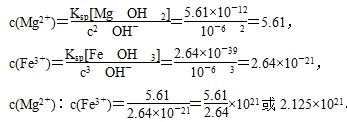
(2)“趁热过滤”得到的物质是Na2CO3・H2O,温度应控制在高于36 ℃。
(3)“母液”中含有Cl-和SO42―,若循环使用,则溶液c(Cl-)和c(SO42―)增大,最后所得产物Na2CO3混有杂质。
本题难度:一般
2、实验题 某同学欲探究食品添加剂铵明矾NH4Al(SO4)2・12H2O高温分解的情况。
(1)预测产物:下列关于气体产物的预测不合理的是?。
A.NH3、N2、SO2、H2O? B.NH3、SO3、H2O
C.NH3、SO2、H2O? D.NH3、N2、SO3、SO2、H2O
(2)定性检验:取一定量铵明矾,设计下列实验探究产物。
①按图示组装仪器后,首先检查整套装置的气密性,操作是?。
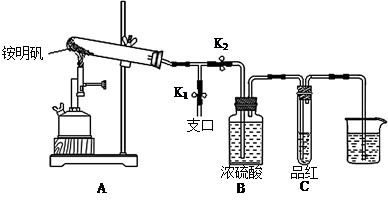
②夹住止水夹K1,打开止水夹K2,用酒精喷灯充分灼烧。实验过程中,装置A和导管中未见红棕色气体;试管C中的品红溶液褪色;在支口处可检验到NH3,方法是?;在装置A与B之间的T型导管中出现白色固体,该白色固体可能是?(任填一种物质的化学式)。
③分析得出装置A试管中残留的白色固体是两性氧化物,写出它溶于NaOH溶液的离子方程式?。
④为了防止倒吸,实验结束时必须先?(填字母序号),然后熄灭酒精喷灯。
A.取出烧杯中的导管? B.打开止水夹K1? C.关闭止水夹K2
(3)分析和结论:实验证明气体产物是(1)D中的5种气体。相同条件下测得生成N2和SO2的体积比是定值,V(N2):V(SO2)=?。
参考答案:(1)C(2分)
(2)①关闭支口开关K1并打开K2(1分),将最后的导管通入水中,微热大试管(1分),若看到从导管中出现气泡(1分),且停止加热后在导管中上升一段水柱,(1分)则证明气密性好。(共4分)
②打开K1,用蘸有浓盐酸的玻璃棒靠近支口,若出现白烟(或者不加试剂看到白烟也给分)(2分)(用润湿的紫色石蕊试纸检验不得分);(NH4)2SO4或者(NH4)2SO3或者SO3(酸式盐及以上物质的混合物也给分)(2分)
③Al2O3 +2OH-=2AlO2-+H2O或Al2O3 +3H2O +2OH-=2Al(OH)4-(2分,配平错误得0分)
④B或C,或BC(2分)
(3)1:3(2分)
本题解析:(1)A、生成N2,N元素化合价升高,生成SO2,S元素化合价降低,符合氧化还原反应原理,预测合理;B、生成NH3、SO3、H2O,为非氧化还原反应,预测合理;C、生成SO2,S元素化合价降低,无元素化合价升高,不符合氧化还原反应原理,预测不合理;D、既有元素化合价升高,也有元素化合价降低,预测合理。
(2)①利用加热气体膨胀的原理检验装置的气密性,首先要关闭支口开关K1并打开K2,然后将最后的导管通入水中,微热大试管,若看到从导管中出现气泡,且停止加热后在导管中上升一段水柱,则证明气密性好。
②用浓盐酸检验NH3,打开K1,用蘸有浓盐酸的玻璃棒靠近支口,若出现白烟,证明含有NH3,但不能用润湿的石蕊试纸,因为混合气体中含有SO2,SO3,试纸不可能变蓝;装置A与B之间的T型导管中出现白色固体可能是SO2与NH3反应生成的(NH4)2SO3,或SO3与NH3反应生成的(NH4)2SO4,或SO3固体,或酸式盐及以上物质的混合物。
③A试管中残留的白色固体是两性氧化物,则A为Al2O3,与NaOH溶液反应的离子方程式为:Al2O3 +2OH-=2AlO2-+H2O或Al2O3 +3H2O +2OH-=2Al(OH)4-。
④打开止水夹K1 倒吸的液体由支口出流出,关闭止水夹K2,导管被关闭,所以防止倒吸的方法为:B或C,或BC。
(3)根据氧化还原反应中化合价升高的总价数与降低的总价数相等,可得:6n(N2)=2n(SO2),可得n(N2):n(SO2)=1:3,相同条件下气体物质的量之比等于体积之比,所以V(N2):V(SO2)=1:3。
本题难度:困难
3、选择题 下列有关实验的说法中错误的是?
[? ]
A.向无水乙醇中加入浓H2SO4,加热至170°C产生的气体通入酸性KMnO4溶液,红色褪去,并不能证明一定产生了乙烯
B.检验C2H5Cl中的氯元素:先将C2H5Cl与NaOH溶液混合后加热,再加硝酸酸化,然后加入AgNO3溶液
C.苯中混有苯酚可加入过量浓溴水过滤除去
D.作为重结晶实验的溶剂,杂质在此溶剂中的溶解度受温度影响应该很大
参考答案:CD
本题解析:
本题难度:一般
4、实验题 碘是人体必需的元素之一,海洋植物如海带、海藻中含有丰富的、以化合态形式存在的碘元素。在实验室中,从海藻里提取碘的流程和实验装置如下:
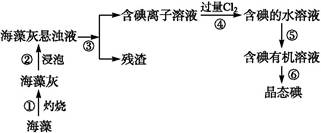
(1)指出上述提取碘的过程中有关实验操作的名称:步骤③ ,步骤⑤ 。?
(2)写出步骤④对应反应的离子方程式: 。?
(3)提取碘的过程中,可供选择的有机试剂是 。(填编号)?
A.酒精? B.醋酸? C.四氯化碳? D.苯
(4)步骤④除了加入过量Cl2,下列氧化剂最好选用 (填代号)。?
A.浓硫酸? B.H2O2溶液? C.KMnO4溶液
理由是____________________________。?
(5)为了使海藻灰中的碘离子转化为碘的有机溶液,即完成步骤③至⑤,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器和物品,尚缺少的玻璃仪器是 。?
(6)从含碘的有机溶剂中提取碘和回收有机溶剂,还需要经过蒸馏。指出下图实验装置中存在的错误之处: 。?
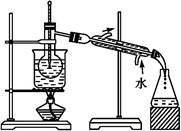
参考答案:(1)过滤 萃取、分液(每空1分)
(2)Cl2+2I- I2+2Cl-(2分)
I2+2Cl-(2分)
(3)CD(1分)
(4)B(1分)
过氧化氢是绿色氧化剂,在氧化过程中不会引进杂质,也不产生污染(2分)
(5)分液漏斗、普通漏斗(2分)
(6)温度计水银球的位置不对(2分)
本题解析:(1)从流程图中可知操作③是过滤,操作⑤是萃取、分液。(2)Cl2的氧化性大于I2,可发生反应Cl2+2I- I2+2Cl-。(3)根据萃取原理,要从含碘的水溶液中萃取碘,所选萃取剂一定要和水互不相溶或很难相溶,且溶质在萃取剂中溶解度要比在水中大得多。在选项中酒精、醋酸皆与水互溶。因此C、D正确。(4)氧化剂选过氧化氢,因为它是绿色氧化剂,反应过程中无污染物产生。(5)按照流程图考虑每一步需要的仪器还缺少普通漏斗和分液漏斗。(6)检查实验装置的错误,要按实验进程逐一检查。由图示装置可看出温度计水银球的位置不对。
I2+2Cl-。(3)根据萃取原理,要从含碘的水溶液中萃取碘,所选萃取剂一定要和水互不相溶或很难相溶,且溶质在萃取剂中溶解度要比在水中大得多。在选项中酒精、醋酸皆与水互溶。因此C、D正确。(4)氧化剂选过氧化氢,因为它是绿色氧化剂,反应过程中无污染物产生。(5)按照流程图考虑每一步需要的仪器还缺少普通漏斗和分液漏斗。(6)检查实验装置的错误,要按实验进程逐一检查。由图示装置可看出温度计水银球的位置不对。
本题难度:一般
5、选择题 除去下列溶液中的杂质(括号内是杂质)所用试剂不正确的是( )
A.NaOH溶液[Ba(OH)2]:用Na2SO4溶液
B.NaCl溶液[Na2SO4]:用Ba(NO3)2溶液
C.KOH溶液[K2CO3]:用Ca(OH)2溶液
D.HNO3溶液[HCl]:用AgNO3溶液
参考答案:B
本题解析:
本题难度:一般