微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 I、某化学课外活动小组对污染大气的部分非金属氧化物进行探究。请根据题目要求回答下列问题。
(1)写出用硝酸制取NO的离子方程式?。
(2)查资料得知,HCOOH CO+H2O。实验室有如图l所示的装置,制取CO气体可选用的装置为
CO+H2O。实验室有如图l所示的装置,制取CO气体可选用的装置为
?(填序号),实验室利用该装置还可制取的常见气体有 ??(写一种气体的分子式)。
(3)查资料得知,利用催化剂可使汽车尾气中的一氧化碳和氮氧化物大部分发生反应转化为二氧化碳和氮气。该小组在实验室模拟汽车尾气处理,设计了如图2所示装置(部分夹持和装置已略去)。

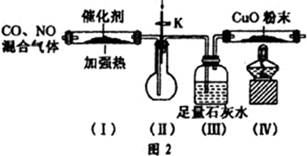
①实验前,关闭旋塞K,先通氮气排净装置中的空气,其目的是?。
②装置(III)的主要作用是?。
③该套装置中有不完善之处,还应在装置(Ⅳ)后补充?装置。
II、该课外小组设计的从ZnSO4、FeCl3的混合溶液中制取ZnSO4・7H2O过程如下:
a.在混合液中加入6 mol/L NaOH溶液,至pH=8为止。
b.过滤后得到沉淀,用蒸馏水多次洗涤沉淀。
c.向洗涤后的沉淀中加入2 mol/L的硫酸,保持溶液的pH在4~6,加热煮沸,趁热过滤,滤液即为ZnSO4溶液。
d.滤液中加入2 mol/L的硫酸,使其pH=2。
已知部分阳离子以氢氧化物的形式开始沉淀至完全沉淀时溶液的pH见下表,回答下列问题:
沉淀物
| Fe(OH)3
| Zn(OH)2
|
pH
| 1.5~3.2
| 6.4~8.0
|
?
(1)步骤b中如何检测沉淀已经洗涤干净??。
(2)步骤d中加入硫酸,使其pH=2的目的是?;要制得ZnSO4・7H2O的步骤d还缺少的操作是?,所用的主要硅酸盐仪器是?。
参考答案:I.(1)3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O(2)
(2)A、Cl2(答案合理即可)(共1分,共2分)?(3)①防止CO与空气混合加热爆炸(2)
②检验CO是否转化为CO2(2)?③尾气处理装置(2)
Ⅱ.(1)取最后一次洗涤液少量,滴加硝酸银溶液,若无白色沉淀,说明已经洗涤干净(合理即给分)(2分)
(2)抑制Zn2+水解 (1分);将溶液加热浓缩,冷却结晶 (2分);
蒸发皿,酒精灯,玻璃棒(3分)
本题解析:I.(1)硝酸具有强氧化性,能氧化单质铜,同时还有NO和水生成,所以用铜屑和稀硝酸为原料制取硝酸铜的离子方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O。
(2)该反应为液体加热制气装置,需要分液漏斗和酒精灯。因此选择装置A。根据装置特点可知,该装置还可以用用浓盐酸和二氧化锰加热可制取氯气。
(3)①CO是可燃性气体,加热时易发生爆炸,所以实验前,关闭旋塞K,先通氮气排净装置中的空气的目的是防止可燃性气体与空气或氧气混合加热发生爆炸。
②CO2遇澄清的石灰水变浑浊,而一氧化碳不能,所以装置(III)中澄清石灰水的主要作用是检验CO是否转化为CO2。
③一氧化碳有毒,所以要注意防止一氧化碳泄漏从而污染环境,所以还应在装置(Ⅳ)后补充尾气处理装置。
II.(1)由于沉淀表面有吸附的氯离子,所以检验沉淀是否洗净的实验操作是:取最后一次洗涤液少量,滴加硝酸银溶液,若无白色沉淀,说明已经洗涤干净。
(2)因为Zn2+完全沉淀时的pH为6.4~8.0,所以步骤d中加入硫酸,使其pH=2的目的是抑制Zn2+水解;要制得ZnSO4?7H2O还需要将溶液加热浓缩,冷却结晶;加热蒸发需要使用硅酸盐仪器是蒸发皿,酒精灯,玻璃棒。
本题难度:困难
2、实验题 除去下列溶液的少量杂质,根据要求填空。
物质
| 杂质
| 选用试剂
| 离子方程式
|
NaNO3
| NaCl
| ?
| ?
|
KCl
| K2CO3
| ?
| ?
|
NaHCO3
| Na2CO3
| ?
| ?
|
?
参考答案:
选用试剂
离子方程式
AgNO3
Ag++Cl-=AgCl↓
HCl
2H++CO2-3=CO2↑+H2O
CO2
CO2-3+CO2+H2O=2HCO-3
本题解析:略
本题难度:简单
3、选择题 海水中提取的食盐经精制(除去Ca2+、Mg2+和SO42-后,含有少量的氯化钾等杂质,为了提纯并得到更多的食盐,用某液体洗涤,该液体最好是
[? ]
A.蒸馏水
B.饱和食盐水
C.饱和氯化钾溶液
D.75%的酒精溶液
参考答案:B
本题解析:
本题难度:简单
4、选择题 现有一瓶A和B的混合液,已知A和B的某些性质如下:
| 物质 | 分子式 | 熔点℃ | 沸点℃ | 密度g?cm-3 | 水溶性
A
C3H6O2
-98
57,5
0,93
可溶
B
C4H8O2
-84
77
0,90
可溶
|
由此,分离A和B的最佳方法是( )
A.萃取
B.升华
C.分馏
D.分液
参考答案:由表中数据可知,A和B沸点不同,且相差较大,可用蒸馏的方法分离,而二者都溶于水,则不能用过滤、分液的方法分离.
故选C.
本题解析:
本题难度:一般
5、选择题 向碘水中加入适量CCl4并振荡,静置后观察到的现象是
[? ]
A.形成均匀的无色溶液
B.形成均匀的紫红色溶液
C.液体分层,下层呈紫红色
D.液体分层,上下层均呈无色
参考答案:C
本题解析:
本题难度:简单