微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列事实,不能用勒夏特列原理解释的是(?)
A.对2HI(g) H2(g)+I2(g),平衡体系增大压强可使颜色变深
H2(g)+I2(g),平衡体系增大压强可使颜色变深
B.溴水中有下列平衡Br2+H2O HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅
HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅
C.CO+NO2 CO2+NO(正反应为放热反应),升高温度可使平衡向逆反应方向移动
CO2+NO(正反应为放热反应),升高温度可使平衡向逆反应方向移动
D.往H2S水溶液中加碱有利于S2-的增加
参考答案:A
本题解析:A项:2HI(g) H2(g)+I2(g)反应前后总的体积不变,压强对化学平衡没有影响,故选A。
H2(g)+I2(g)反应前后总的体积不变,压强对化学平衡没有影响,故选A。
点评:本题考查的是勒夏特列原理的应用,学生需要值得注意的是只有化学平衡移动,才能用勒夏特列原理来解释。
本题难度:简单
2、选择题 恒温条件下,把 装入带活塞的密闭容器中,当反应
装入带活塞的密闭容器中,当反应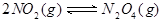 达到平衡后,慢慢压缩,下列叙述正确的是
达到平衡后,慢慢压缩,下列叙述正确的是
A.体积减半,则压强为原来的两倍
B.平衡向右移动,混合气体的颜色一定会变浅
C.体积减半,压强增大,但小于原来的2倍
D.平衡向右移动,混合气体密度不变
参考答案:C
本题解析:A错,体积减半,这个瞬间压强为原来的两倍,增大了压强,平衡向气体体积减小的方向移动,即该平衡将向正反应方向移动,压强在两倍的基础上将会减小;
B错,平衡向右移动混合气体的颜色不一定会变浅,如增加N2O4的浓度,平衡向左移动,但N2O4的浓度增大。
C,正确;D错,平衡向右移动,气体总物质的量减小,而气体的总质量不变,即,混合气体的密度会增大。
本题难度:一般
3、选择题 可逆反应N2(g)+3H2(g)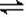 2NH3(g)在体积不变的密闭容器中反应,达到平衡状态的标志是(?)
2NH3(g)在体积不变的密闭容器中反应,达到平衡状态的标志是(?)
①单位时间内生成n mol N2的同时,生成3n mol H2
②断开1mol H-H键的同时断开2 molN-H键
③用N2、H2、NH3的浓度变化表示的反应速率之比为1:3:2
④混合气体的压强不再改变
⑤混合气体的密度不再改变
A.②④
B.①④
C.①③④
D.②③④⑤
参考答案:A
本题解析:化学反应达到平衡状态时,正逆反应速率相等,各物质的浓度不变,由此衍生的一些物理量不变。
①同位逆反应速率,故错;③无论是否达到平衡状态,化学反应速率之比都等于化学计量数之比,故错;⑤反应前后气体的质量不变,容器的体积不变,无论是否达到平衡状态,气体的密度都不变,不能作为判断是否达到平衡状态的依据,故错。
故选A。
点评:本题考查考查化学平衡状态的判断,题目难度中等,本题注意正逆反应速率关系的确定,为易错点,做题时注意把握化学方程式的特征。
本题难度:简单
4、选择题 mA(s)+nB(g) pC(g)的可逆反应,在室温条件下φ(B)与压强(p)的关系如图4所示,则下列有关叙述正确的是(? )
pC(g)的可逆反应,在室温条件下φ(B)与压强(p)的关系如图4所示,则下列有关叙述正确的是(? )
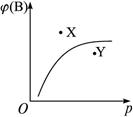
图4
A.m+n<p
B.n>p
C.X点时混合物的正反应速率大于逆反应速率
D.X点比Y点混合物的反应速率慢
参考答案:CD
本题解析:由图示可看出,随p增大,φ(B)也增长,所以,p增大时,平衡向左移动,所以n<p(注意物质A是固体,所以在此不应涉及m),选项A、B均不正确。
在曲线上,当p一定时,φ(B)也一定,所以曲线上每一点均表示达平衡状态,而曲线外各点均不是平衡状态。在曲线上方的任一点(如X点)φ(B)比平衡状态时大,则在达到平衡状态的过程中,必须使φ(B)减小,则必须是正反应速率大于逆反应速率。
由于Y点的压强比X点的压强大,所以Y点比X点混合物的反应速率大。
本题难度:简单
5、填空题 (6分)如图所示,某温度下,物质的量分别是1.2mol的气体X和物质的量为1.0mol的气体Y,在2L密闭容器中反应生成气体Z,反应5min后测得n(X) =0.4mol,n(Y)=0.2mol,生成的n(Z)=1.6mol,则该反应的反应物为?该反应的化学方程式可表示为??,反应在10分钟内的化学反应速率用Z来表示则V(Z)=?。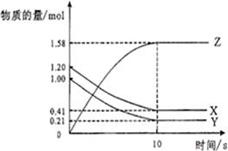
参考答案:X?和 Y ;? X + Y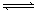 2Z ;? 0.079 mol /(L・min)
2Z ;? 0.079 mol /(L・min)
本题解析:由图像可知X和Y的物质的量减少,Z的物质的量增加,所以X和Y是反应物,Z是生成物。到达平衡时X、Y、Z的物质的量的变化量分别是0.79mol、0.79mol、1.58mol,因为变化量之比就是相应的化学计量数之比,所以方程式为X + Y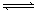 2Z。反应速率通常用单位时间内浓度的变化量来表示,所以用Z表示的反应速率是
2Z。反应速率通常用单位时间内浓度的变化量来表示,所以用Z表示的反应速率是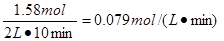 。
。
本题难度:一般