微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 【化学与技术】
以黄铁矿为原料(主要成分是FeS2)为原料,生产硫酸的简要流程图如下:
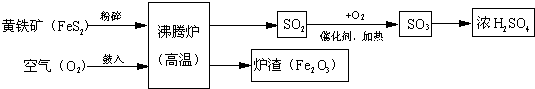
(1)写出流程图中一种氧化物的名称?。?
(2)将黄铁矿粉碎,目的是?。
(3)流程中SO2转化为SO3的化学方程式为?。
(4)炉渣(Fe2O3)在工业上可用来?。
参考答案:(1)二氧化硫或三氧化硫或三氧化二铁
(2)增大反应物的接触面积
(3)
(4)做冶铁原料
本题解析:(1)二氧化硫或三氧化硫或三氧化二铁都是由两种元素组成,一种元素是氧元素,属于氧化物。
(2)反应物接触面积越大,反应越剧烈,黄铁矿粉碎会增大反应物的接触面积,加快反应速度;
(3)反应物是二氧化硫和氧气,生成物是三氧化硫,用观察法配平,反应条件是催化剂和加热,所以方程式是:
(4)做冶铁原料。
本题难度:一般
2、选择题 实验室中洗涤附着在试管内壁上的硫应选择的试剂是
[? ]
A.二硫化碳
B.水
C.盐酸
D.酒精
参考答案:A
本题解析:
本题难度:简单
3、填空题 (16分)Y是由硫的含氧酸盐组成的纯净物或者混合物,该物质可溶于水,食品工业常将它用作漂白剂、防腐剂、疏松剂、护色剂及保鲜剂等。化学兴趣小组在实验室对Y中硫元素的价态进行探究:①将过量的稀硝酸加入少量样品中,振荡;②取少许反应后的溶液,滴加硝酸钡溶液,出现白色沉淀。甲认为不能由此确定Y中硫的价态为+6价。
(1)上述实验中产生的沉淀是?。
(2)你认为甲的判断是否正确?(填“是”或“否”),作出这种判断的依据是?。
(3)请完成对硫元素价态的探究:
限定实验仪器与试剂:烧杯、试管、玻璃棒、药匙、滴管和试管架;1mol・L-1H2SO4、2mol・L-1 HCl、2mol・L-1HNO3、3%H2O2、0.5mol・L-1BaCl2、品红试纸、蒸馏水。
①提出合理假设
假设1,硫的价态是+4价
假设2,硫的价态是+6价
假设3,?
②设计实验方案证明你的假设
③实验过程
根据②的实验方案,进行实验。请写出实验步骤、预期现象与结论。
实验操作
| 预期的现象与结论
|
操作1
| ?
|
操作2
| ?
参考答案:(1)BaSO4(2分)
(2)是(2分);SO42-被HNO3氧化为S O2-4,生成的白色沉淀也不溶于HNO3(2分) O2-4,生成的白色沉淀也不溶于HNO3(2分)
(3)①硫的价态既有+4价也有+6价(2分)
③
实验操作
预期的现象与结论
操作1:用药匙取少量样品于试管中,用胶头滴管滴加2mol・L-1盐酸至不再产生气泡为止,同时将蒸馏水润湿的品红试纸放在试管口上方
(1)若有气泡产生,湿润的品红试纸褪色,则假设1或假设3成立
(2)若无气泡产生,湿润的品红试纸不褪色,则假设2成立
操作2:取操作I的溶液少许于另一试管中,滴加0.5mol・L-1BaCl2溶液
结合操作I中的(1):
(1)若有白色沉淀,则假设3成立
(2)若无白色沉淀,则假设1成立
(每空2分,其它合理答案也对)
本题解析:略
本题难度:简单
4、计算题 某化学小组为了测定石膏(CaSO4・xH2O)的组成,即测定x值,做如下实验:将石膏加热使之脱水,加热过程中固体的质量与时间的变化关系如下图所示。数据表明当固体的质量为2.72g后不再改变。
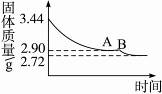
求(必须写出计算过程):
(1)石膏的化学式。
(2)图象中AB段对应化合物的化学式。
参考答案:(1)CaSO4・2H2O?(2)2CaSO4・H2O或CaSO4・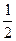 H2O H2O
本题解析:(1)CaSO4・xH2O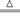 CaSO4+xH2O CaSO4+xH2O
136+18x?136?18x
3.44g?2.72g0.72g
x=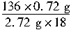 =2 =2
该化合物化学式为CaSO4・2H2O。
(2)实验数据和图象AB段说明在石膏受热分解过程中,有一固定组成的化合物存在。
CaSO4・2H2O 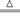 ?CaSO4・yH2O+(2-y)H2O ?CaSO4・yH2O+(2-y)H2O
172? 136+18y
3.44g? 2.90g
解得y=0.5
该化合物化学式为2CaCO4・H2O(或CaSO4・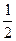 H2O)。 H2O)。
本题难度:简单
5、选择题 雷雨天闪电时空气中有臭氧(O3)生成。下列说法中正确的是
A.相同质量的O2和O3原子个数比为2:3
B.O2和O3化学性质完全相同
C.在相同温度与压强下,等体积的O2和O3含有相同的分子数
D.O2和O3的相互转化是物理变化
参考答案:C
本题解析:氧气和臭氧是氧元素的两种同素异形体,因此在质量相同的条件下,氧原子的个数是相同的。二者的结构不同,化学性质不可能完全相同,根据阿伏加德罗定律可知选项C是正确的。同素异形体间的转化是化学变化,所以答案是C。
本题难度:一般
|