微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 有aA3+和bBn-两种离子,它们的电子层结构相同,则n值是?(?)
A.a-3-b
B.b-3-a
C.a+3-b
D.a-3+b
参考答案:A
本题解析:电子层结构相同的粒子具有相同数目的电子数,所以可得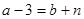 ,得
,得
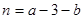 ;
;
本题难度:简单
2、选择题 已知质量数为A的某阳离子Rn+,核外有X个电子,则核内中子数为
A.A-x
B.A-x-n
C.A-x+n
D.A+x-n
参考答案:B
本题解析:阳离子Rn+,质量数为A,核外有X个电子,所以其质子数Z=X+n,由于中子数=质量数-质子数,故质子数=A-(X+n)=A-x-n。
故选B。
点评:本题考查质子数、核外电子数、离子电荷的关系以及质量数、质子数、中子数的关系,难度较小,掌握好相互之间的关系即可顺利解答.要理解、熟记相互间的关系。
本题难度:简单
3、选择题 下列物质属于纯净物的是
A.洁净的空气
B.食盐水
C.浮有冰块的水
D.糖水
参考答案:C
本题解析:
本题难度:困难
4、填空题 (14分)下表是元素周期表的短周期部分,表中字母分别表示一种元素。请回答下列问题:
(1) f元素在周期表中的位置是第?周期第?族。
(2) e 与f两元素最高价氧化物的水化物相互反应的化学方程式为
_________________________________________________
(3)e在空气中燃烧的产物所含化学键的类型为__________、__________。
(4) 化合物ca3的电子式为?,c和d两种元素氢化物的稳定性更强的是 _______(填物质的化学式)。
参考答案:(每空2分,共14分)(1) 3? IIIA? (4分)? (2)NaOH+Al(OH)3=NaAlO2+2H2O ?(2分)?
(3) 离子键、共价键 (4分)? (4) 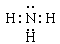 (2分)? H2O(2分)
(2分)? H2O(2分)
本题解析:考查元素周期表的结构及元素周期律的应用。根据元素在周期表中的位置可判断,a~g分别是H、C、N、O、Na、Al、S。
(1)铝元素位于第三周期第ⅢA。
(2)氢氧化铝是两性氢氧化物,能和氢氧化钠反应,方程式为NaOH+Al(OH)3=NaAlO2+2H2O。
(3)钠在空气中的燃烧产物是过氧化钠,其中含有离子键和非极性键。
(4)氨气是含有极性键的共价化合物,电子式为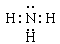 。同周期自左向右非金属性逐渐增强,相应氢化物的稳定性也逐渐增强,所以水的稳定性要强于氨气的
。同周期自左向右非金属性逐渐增强,相应氢化物的稳定性也逐渐增强,所以水的稳定性要强于氨气的
本题难度:一般
5、计算题 9.6克A原子与4.2克B原子含有相同的原子数,A、B原子核中各自的质子数和中子数相等,已知A元素在其最高价氧化物中的质量分数为40%,在其氢化物中的质量分数为94.1%,试通过计算确定:
(1)A、B的元素符号及在元素周期表中的位置;
(2) A、B的相对原子质量。
参考答案:(1)A:S,第三周期第Ⅵ族;B:N,第二周期,第Ⅴ族
(2)A:32;B:14
本题解析::推出A的氢化物分子式为HxA,最高价氧化物分子式应该是A2O8-x,通过题给的条件求出A的相对原子质量:A/(x+A)=94.1%,A/(A+16*(8-x)/2)=40%,可解得x=2,A=32。再利用题目中A、B质量关系和原子数关系求出B的原子量:由于9.6g元素A与4.2g元素B含有相同的原子数,设B的原子量为y,由9.6/32="4.2/y,y=14" 。最后根据两种元素原子的质子数确定在周期表中的位置。
点评:本题考查质量分数的计算,依据题意求出相对原子质量,并判断元素在周期表中的位置,综合性较强,题目难度较大。
本题难度:一般