��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���з�Ӧ���������ȷ�Ӧ����
A.п����ϡ������
B.������طֽ�
C.������ԭ����ͭ
D.̼��ˮ�����ڸ����·�Ӧ
�ο��𰸣�A
���������
�����Ѷȣ�����
2��ѡ���� ���и��鷴Ӧ��ʵ�ʶ���ȡ����Ӧ����
A.�����������Ӻ���ˮ��Ӧ��������Ӧ��֬��Ӳ��
B.����ˮ�⣬������Ӧ���Ҵ�����±�ᷴӦ���Ҵ���Ũ���������140 ��ʱ�ķ�Ӧ
C.����������������������ǣ�ȩ��������ԭ
D.��ά��ˮ�⣬Ũ������Ҵ���170 ��ʱ�ķ�Ӧ��������ˮ��
�ο��𰸣�B
�����������֬��Ӳ���Ǻ����������ӳɷ�Ӧ��ȩ��������ԭ����ȡ����Ӧ��Ũ������Ҵ���170 ��ʱ������ϩ����ȥ��Ӧ��������ȷ�Ĵ���B��
�����Ѷȣ�����
3������� ��10�֣�
ij��ɫ����Һ�п��ܴ�������Ag����Mg2����Fe3���еļ������ӡ�
(1)�����κ�ʵ��Ϳ��Կ϶�ԭ��Һ�в����ڵ�������?��
(2)ȡ����ԭ��Һ�������ϡ���ᣬ�а�ɫ�������ɣ��ټ������ϡ���ᣬ��ɫ��������ʧ��˵��ԭ��Һ�п϶��е�����?��?�йص����ӷ�ӦʽΪ?��
(3)ȡ(2)����Һ�������NaOH��Һ�����ְ�ɫ������˵��ԭ��Һ�п϶����ڵ�������?��
(4)ԭ��Һ�п��ܴ������ڵ�������������A��D�еģ�����ţ�??��
A��Cl��
B��NO3��
C��CO32��
D��OH��
�ο��𰸣�(1) Fe3��?(2) Ag��? Ag����Cl����AgCl��?(3) Mg2��?(4)B
�����������
�����Ѷȣ�һ��
4������� ��6�֣�ij��Һ�п��ܺ���OH����CO32����AlO2����SiO32����SO42����K+��Na+��Fe3+��Mg2+��Al3+�����ӣ�������Һ����μ���һ�����ʵ���������ʱ�����ɳ������ʵ����������������Ĺ�ϵ��ͼ��ʾ��

�ش��������⣺����֪��AlO2��+HCO3��+H2O=Al��OH��3��+ CO32����
��1��ԭ�����Һ��һ�����е������ǣ�___________________________________��
��2��AB�η�Ӧ�����ӷ���ʽ�ǣ�____________________________________________��
(3)����AB�η�Ӧ�������뷢��BC�η�Ӧ�������������ʵ���֮��Ϊ��____________��
�ο��𰸣���1��OH����CO32����AlO2����SiO32��?��2��H++ CO32��= HCO3��? H++ HCO3��=CO2��+H2O
��3��n��CO32������n[Al��OH��3]=3��4
�����������������ۣ�һ��ʼû�г������ɣ���˵��ԭ��ҺΪ���ԣ�һ�����ڴ�����OH�����ų�Fe3+��Mg2+��Al3+�Ĵ������ڣ�
���������ܽ⣬˵��һ������AlO2����SiO32����
SiO32����2H��=H2SiO3��������ܽ��ᣩ
AlO2����H����H2O=Al(OH)3��? Al(OH)3��3H��=Al3����3H2O
��A��B�εĴ��ڣ�˵��ԭ��Һ�д���CO32����H++ CO32��= HCO3��? H++ HCO3��=CO2��+H2O
ע����AlO2��+HCO3��+H2O=Al��OH��3��+ CO32����֪��AlO2������HCO3�����H������CO32�����H����������̼���Al��OH��3���ܽ��ڹ�����������
(3)���������������֪��
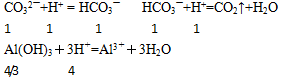
����n��CO32������n[Al��OH��3]=3��4
�����Ѷȣ���
5������� (14��)����п�������ᡢ�´ɡ����¡�ҽҩ�����ӡ���ѧ�ȹ�ҵ����Ҫԭ�ϡ�����
��п��ƷΪԭ���Ʊ���������п�����������������£�

��1��.��������õ���������Һ�к���Zn2����SO42����������Fe2����Cu2����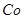 ����Mn2����
����Mn2����
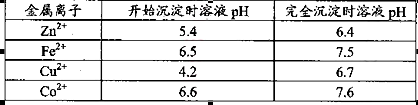
���ʡ�����A�������ǵ�����Һ��pH��5 4������A���ѡ��________��
A��NH3.H2O
B��Na2CO3
C��H2SO4
D��ZnO
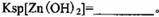 ��
�� ������1
������1 ����Һ��Fe2�������ĵ�KMnO4������Ϊ________g��������λ��Ч���֣���
����Һ��Fe2�������ĵ�KMnO4������Ϊ________g��������λ��Ч���֣��� 2���������û���Ӧ��ȥ��������B��_________��
2���������û���Ӧ��ȥ��������B��_________�� �����ɸó����Ļ�ѧ����ʽΪ________��
�����ɸó����Ļ�ѧ����ʽΪ________��