微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知:C(s)+O2(g)=CO2(g)?△H1
CO2(g)+C(s)=2CO(g)?△H2
2CO(g)+O2(g)=2CO2(g)?△H3
4Fe(s)+3O3(g)=2Fe2O3(s)?△H4
3 CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s)?△H5
下列关于上述反应焓变的判断正确的是
A.△H1>0,△H3<0
B.△H2>0,△H4>0
C.△H1=△H2+△H3
D.△H3=△H4+△H5
参考答案:C
本题解析:A、碳和CO燃烧均是放热反应,△H1<0,A不正确;B、二氧化碳与碳反应是吸热反应,铁在氧气中燃烧是放热反应,△H4<0,B不正确;C、②CO2(g)+C(s)=2CO(g)?△H2,③2CO(g)+O2(g)=2CO2(g)?△H3,则根据盖斯定律可知②+③即得到C(s)+O2(g)=CO2(g) ,△H1=△H2+△H3,C正确;D、已知④4Fe(s)+3O3(g)=2Fe2O3(s)?△H4,⑤3CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s)?△H5,则根据盖斯定律可知(④+⑤×2)÷3得到2CO(g)+O2(g)=2CO2(g),则△H3= ,D不正确,答案选C。
,D不正确,答案选C。
本题难度:一般
2、选择题 已知胆矾溶于水时溶液温度降低,胆矾分解的热化学方程式为:CuSO4・5H2O(s)=CuSO4(s)+5H2O(l)ΔH=Q1kJ・mol-1;室温下,若将1mol无水硫酸铜溶解为溶液时放热Q2kJ,则:
[? ]
A.Q1>Q2
B.Q1=Q2
C.Q 1<Q2
D.无法比较
参考答案:A
本题解析:
本题难度:一般
3、选择题 下列说法不正确的是?
[? ]
A.在化学反应进行的过程中放出或吸收的热量称为反应热
B.对于吸热反应,反应物所具有的总能量总是低于生成物所具有的总能量
C.在25℃、101 kPa时,1 mol纯物质完全燃烧生成稳 定氧化物时,所放出的热量叫做该物质的燃烧热
D.在稀溶液中,1mol酸跟1 mol碱发生中和反应所 放出的热量叫做中和热
参考答案:D
本题解析:
本题难度:简单
4、选择题 已知Mg(OH)2和Al(OH)3是工业上常用的阻燃剂,Mg(OH)2的分解温度范围为340~490 ℃,氢氧化铝的分解温度范围为190~230 ℃,它们的热化学方程式分别为:
Mg(OH)2(s)=MgO(s)+H2O(g) ΔH1=+81.5 kJ・mol-1
Al(OH)3(s)=1/2Al2O3(s)+3/2H2O(g) ΔH2=+87.7 kJ・mol-1
下列说法不正确的是
[? ]
A.Mg(OH)2和Al(OH)3高温下不分解,所以可做工业阻燃剂
B.等质量Mg(OH)2和Al(OH)3相比,Mg(OH)2阻燃效果较好
C.Mg(OH)2比Al(OH)3热稳定性高
D.Mg(OH)2和Al(OH)3作为工业阻燃剂与它们分解吸热及生成物具有耐高温性有关
参考答案:A
本题解析:
本题难度:一般
5、填空题 目前,消除氮氧化物污染有多种方法。
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ・mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1160 kJ・mol-1
③H2O(g)=H2O(l) ΔH=-44.0 kJ・mol-1
写出CH4 (g)与NO2 (g)反应生成N2 (g) ,CO2(g)和H2O(l)的热化学方程 式_____________________
(2)用活性炭还原法处理氮氧化物。有关反应为:C(s)+2NO(g) N2(g)+CO2(g)某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温(T。C)条件下反应,反应进行到不同时间测得各物质的浓度如下
N2(g)+CO2(g)某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温(T。C)条件下反应,反应进行到不同时间测得各物质的浓度如下
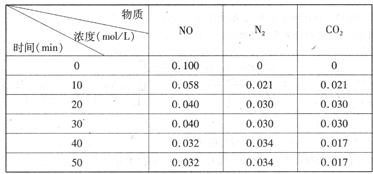
①不能作为判断反应达到化学平衡状态的依据?是_______
A.容器内CO2的浓度保持不变
B.v正(N2)="2" v正(NO)
C.容器内压强保持不变?
D.混合气体的密度保持不变
E.混合气体的平均相对分子质量保持不变
②在T。C时.该反应的平衡常数为_______(保留两位小数);
③在30? min,改变某一条件,反应重新达到平衡,则改变的条件是_______
(3)科学家正在研究利用催化技术将超音速飞机尾气中的NO和CO转变成CO2和N2,其反应为:
2CO+2NO N2+2CO2?ΔH<0研究表明:在使用等质量催化剂时,增大催化剂的比表面积可提高化学反应速率.为了分别验证温度、催化剂的比表面积对化学反 应速率的影响规律、某同学设计了三组实验,部分实验条件已经填在下表中。
N2+2CO2?ΔH<0研究表明:在使用等质量催化剂时,增大催化剂的比表面积可提高化学反应速率.为了分别验证温度、催化剂的比表面积对化学反 应速率的影响规律、某同学设计了三组实验,部分实验条件已经填在下表中。
 ?
?
①上表中:a=_______,b=________,e=________
②请在给出的坐标图中,画出上表中实验II和实验III条件下混合气体中NO浓度随时间变化的趋势曲线图,并标明相应的实验编号
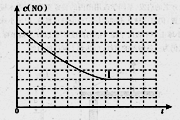 ?
?
参考答案:
(1) CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) ΔH=-955 kJ・mol-1。
(2) ①BC②0.56③减小CO2浓度
(3) ①280? 1.20×10-3?5.80×10-3 ②
本题解析:(1)根据盖斯定律可知,①+②+③即得到CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(l) ΔH=-955 kJ・mol-1。(2) ①在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态,所以选项B正确;根据方程式可知,反应前后体积是不变的,所以压强始终是不变的,则a不能说明;b中反应速率的方向相反,但不能满足速率之比是相应的化学计量数之比,不正确;密度是混合气的质量和容器容积的比值,在反应过程中容积始终是不变的,但质量是变化的;②反应进行到40min时,各种物质的浓度不再发生变化,说明反应已经达到平衡状态,则该反应的平衡常数K=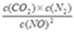 =
=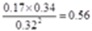 ;③由表中的数据可以看到,在40min的时候,NO的浓度变小,说明反应向右进行,则N2和CO2增加,结果是只有N2增加,而CO2反而变小,只能说明是由于减小 CO2的浓度造成反应向右进行,且向右进行使CO2增加的量没有比CO2减小的量多。(3)①因Ⅰ、Ⅱ比表面积不同,则应控制温度相同,所有浓度应控制相同来验证催化剂比表面积对速率的影响;Ⅱ、Ⅲ比表面积相同,温度不同,则所有浓度应控制相同来验证反应温度对速率的影响;故答案为:280; 1.20×10-3;5.80×10-3;②因Ⅰ、Ⅱ温度相同,催化剂对平衡移动无影响,则平衡不移动,但Ⅱ的速率大,则Ⅱ先达到化学平衡,Ⅰ、Ⅱ达平衡时NO的浓度相同;而Ⅲ的温度高,则反应速率最大且平衡逆移,即达到化学平衡时c(NO)增大,故答案为:
;③由表中的数据可以看到,在40min的时候,NO的浓度变小,说明反应向右进行,则N2和CO2增加,结果是只有N2增加,而CO2反而变小,只能说明是由于减小 CO2的浓度造成反应向右进行,且向右进行使CO2增加的量没有比CO2减小的量多。(3)①因Ⅰ、Ⅱ比表面积不同,则应控制温度相同,所有浓度应控制相同来验证催化剂比表面积对速率的影响;Ⅱ、Ⅲ比表面积相同,温度不同,则所有浓度应控制相同来验证反应温度对速率的影响;故答案为:280; 1.20×10-3;5.80×10-3;②因Ⅰ、Ⅱ温度相同,催化剂对平衡移动无影响,则平衡不移动,但Ⅱ的速率大,则Ⅱ先达到化学平衡,Ⅰ、Ⅱ达平衡时NO的浓度相同;而Ⅲ的温度高,则反应速率最大且平衡逆移,即达到化学平衡时c(NO)增大,故答案为: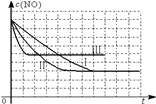
本题难度:困难