微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 对于可逆反应M+N Q 达到限度的标志是(?)
Q 达到限度的标志是(?)
A.M、N、Q三种物质的浓度一定相等
B.M、N全部变成了Q
C.M、N、Q三种物质的浓度不再变化
D.反应已经停止
参考答案:C
本题解析:可逆反应达到限度,是指该反应达到平衡状态,而不是指反应停止了。反应达到平衡状态时,各物质的浓度不再变化,但是不一定相等。
点评:化学平衡是历年高考重中之重,考生一定要系统备考此知识点。
本题难度:简单
2、选择题 若在加入铝粉能放出H 的溶液中,下列各组离子一定不能大量共存的是(?)
的溶液中,下列各组离子一定不能大量共存的是(?)
A.Na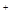 、Fe
、Fe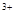 、SO
、SO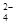 、Cl
、Cl
B.Ba 、Mg
、Mg 、HCO
、HCO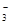 、NO
、NO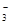
C.Na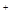 、K
、K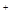 、NO
、NO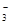 、CO
、CO
D.K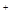 、NO
、NO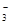 、AlO
、AlO 、OH
、OH
参考答案:B
本题解析:离子间如果发生化学反应,则不能大量共存,反之是可以的。能和金属铝反应生成氢气的溶液可以显酸性,也可以显碱性。如果溶液显酸性,则CO32-、HCO3-、AlO 、OH
、OH 不能大量共存。由于在酸性条件下NO3-和金属铝反应得不到氢气,NO3-也不能大量共存;如果溶液显碱性,则Fe
不能大量共存。由于在酸性条件下NO3-和金属铝反应得不到氢气,NO3-也不能大量共存;如果溶液显碱性,则Fe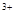 、Mg2+、HCO3-都不能大量共存,所以正确的答案选B。
、Mg2+、HCO3-都不能大量共存,所以正确的答案选B。
点评:该题是高考中的高频题,属于中等难度的试题,试题侧重考查学生的能力。该题需要明确离子不能大量共存的一般情况,即(1)能发生复分解反应的离子之间;(2)能生成难溶物的离子之间;(3)能发生氧化还原反应的离子之间;(5)能发生络合反应的离子之间(如 Fe3+和 SCN-);解决离子共存问题时还应该注意题目所隐含的条件,题目所隐含的条件一般有:(1)溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;(2)溶液的颜色,如无色时可排除 Cu2+、 Fe2+、Fe3+、MnO4-等有色离子的存在;(3)溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;(4)是“可能”共存,还是“一定”共存等。
本题难度:一般
3、选择题 在下列各溶液中,离子一定能大量共存的是
[? ]
A.强酸溶液中:K+、Fe2+、MnO4-、SO42-
B.含有0.1mol・L-1HCO3-的溶液中:K+、Ca2+、OH-、NO3-
C.含有0.1mol・L-1Cu2+的溶液中:Na+、K+、S2-、SO42-
D.室温下,pH=14的溶液中:Na+、K+、NO3-、CO32-
参考答案:D
本题解析:
本题难度:一般
4、选择题 下列各组离子在指定的环境中能大量存在的是 (?)
A.pH=1的无色溶液中:SO42-、Cu2+、Na+、Cl-
B.能使酚酞试液变红色的溶液中:Na+、K+、S2-、CO32-
C.加入铝粉能产生H2的溶液中:NH4+、Na+、Fe2+、NO3-
D.水电离出的c(H+)=1×10-12mol/L的溶液中:K+、Na+、Cl-、HCO3-
参考答案:B
本题解析:A.Cu2+的水溶液是蓝色的,在无色溶液中不能存在。错误。B.能使酚酞试液变红色的溶液是碱性溶液,在碱性溶液中这些离子能够电离共存。正确。C.加入铝粉能产生H2的溶液可能呈酸性也可能呈碱性。在酸性溶液中发生反应:4H++ 3Fe2++NO3-=3Fe3++NO↑+2H2O,不能共存;在碱性溶液中:Fe2++2OH―=Fe(OH)2↓,也不能大量共存。错误。D.室温下纯水电离产生的H+的浓度为水C(H+)= C(OH―) =10-7mol/L.现在电离出的c(H+)=1×10-12mol/L<10-7mol/L.说明水的电离受到了抑制。溶液可能外加了酸或碱。在酸性溶液中:H++HCO3-= H2O+ CO2↑。不能大量共存;在碱性溶液中:OH-+HCO3-= H2O+ CO32-。也不能大量存在。错误。
本题难度:一般
5、选择题 在无色透明溶液中,能大量共存的离子组是( )
A.Mg2+、Na+、SO42-
B.K+、H+、HCO3-
C.Cu2+、NO3-、SO42-
D.Ba2+、NO3-、CO32-
参考答案:A.因该组离子之间不反应,则能大量共存,且离子均为无色,故A正确;
B.因H+、HCO3-能结合生成水和气体,则不能共存,故B错误;
C.该组离子之间不反应,能共存,但Cu2+为蓝色,与无色溶液不符,故C错误;
D.因Ba2+、CO32-能结合生成沉淀,则不能共存,故D错误;
故选A.
本题解析:
本题难度:简单