微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (创新预测题)已知25 ℃时弱电解质的电离平衡常数:
Ka(CH3COOH)=1.8×10-5,Ka(HSCN)=0.13。
(1)将20 mL 0.10 mol・L-1 CH3COOH溶液和20 mL 0.10 mol・L-1的HSCN溶液分别与0.10 mol・L-1的NaHCO3溶液反应,实验测得产生CO2气体体积(V)与
时间t的关系如图所示。
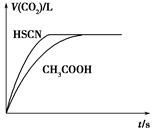
反应开始时,两种溶液产生CO2的速率明显不同的原因是________;反应结束后所得溶液中c(SCN-)______c(CH3COO-)(填“>”、“=”或<)。
(2)2.0×10-3 mol・L-1的氢氟酸水溶液中,调节溶液pH(忽略调节时体积变化),测得平衡体系中c(F-)、c(HF)与溶液pH的关系如图所示。则25 ℃时,HF电离平衡常数为Ka(HF)=________(列式求值)。
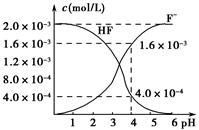
(3)难溶物质CaF2溶度积常数为Ksp=1.5×10-10,将4.0×10-3 mol・L-1 HF溶液与4.0×10-4 mol・L-1的CaCl2溶液等体积混合,调节溶液pH=4(忽略调节时溶液体积变化),试分析混合后是否有沉淀生成?________(填“有”或“没有”),简述理由:_____________________________________。
参考答案:(1)Ka(HSCN)>Ka(CH3COOH),溶液中c(H+):HSCN>CH3COOH,
c(H+)大反应速率快 >
(2) 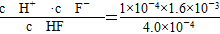 =4×10-4
=4×10-4
(3)有 溶液中离子积Qc=c(Ca2+)・c2(F-)=5.12×10-10>Ksp(CaF2)=1.5×
10-10
本题解析:(1)由Ka(CH3COOH)、Ka(HSCN)的数据知,相同物质的量浓度溶液HSCN的酸性比CH3COOH强,HSCN溶液中c(H+)大,所以反应开始时HSCN溶液与NaHCO3溶液反应的速率快。反应结束后所得两溶液分别为CH3COONa溶液和NaSCN溶液,由于HSCN的酸性比CH3COOH强,则SCN-的水解程度比CH3COO-弱,所以c(SCN-)>c(CH3COO-)。(2)当pH=4时,由图像可知,c(F-)=1.6×10-3 mol・L-1,c(HF)=4.0×10-4mol・L-1,c(H+)=1×10-4mol・L-1,代入Ka(HF)=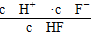 即可。(3)当pH=4时,溶液中的c(F-)=1.6×10-3 mol・L-1,溶液中c(Ca2+)=2.0×10-4 mol・L-1,溶液中离子积Qc=c(Ca2+)・c2(F-)=5.12×10-10>Ksp(CaF2)=1.5×10-10,故有沉淀产生。
即可。(3)当pH=4时,溶液中的c(F-)=1.6×10-3 mol・L-1,溶液中c(Ca2+)=2.0×10-4 mol・L-1,溶液中离子积Qc=c(Ca2+)・c2(F-)=5.12×10-10>Ksp(CaF2)=1.5×10-10,故有沉淀产生。
本题难度:困难
2、选择题 在C(HCO3-)="0.1" mol・L-1的溶液中, 可以大量共存的离子组是(? )?
A.Ca2+、NO3-、NH4+、Cl?
B.Na+、SO42-、C1?、Ca2+
C.H+、Ba2+、Cl?、NO3-
D.Cl?、CO32?、Na+、OH-
参考答案:A
本题解析:略
本题难度:一般
3、选择题 下列各组离子中,在给定条件下能大量共存的是
A.在pH = 1的溶液中:NH4+、K+、ClO-、Cl-
B.有SiO32-存在的溶液中:Na+、Mg2+、Al3+、Cl-
C.有NO3-存在的强酸性溶液中:NH4+、Ba2+、Fe2+ 、Br-
D.在c(H+) = 1.0×10-13 mol・L-1的溶液中:Na+、S2-、AlO2-、SO32-