微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列处理方法正确的是
A.为除去污水中的重金属离子Hg2+,向其中加入足量充分反应后过滤
B.为降低能耗,工业电解熔融态的Al2O3制Al时,加入冰晶石
C.为充分利用原料,氯碱工业中,将阳极室的饱和氯化钠溶液电解为水后导出
D.为保护公路两旁的铁护栏,将其与电源的负极相连
参考答案:B
本题解析:A项:加入Pb粉虽能置换出Hg,但Pb2+会留在溶液中,故错。C项:应该为:电解后的淡盐水从阳极导出,可重新用于配制食盐水,故错。D项:铁护栏连上电会很危险,故错。故选B。
点评:本题重点考查的是电解原理的相关知识,学生要弄清楚电解原理才能正确的解答出本题。电解是将电流通过电解质溶液或熔融态物质,(又称电解液),在阴极和阳极上引起氧化还原反应的过程,电化学电池在外加电压时可发生电解过程。电流流进负电极(阴极),溶液中带正电荷的正离子迁移到阴极,并与电子结合,变成中性的元素或分子;带负电荷的负离子迁移到另一电极(阳极),给出电子,变成中性元素或分子。
本题难度:简单
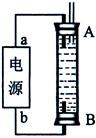
2、实验题 在玻璃圆筒中盛有两种无色的互不相容的中性液体。上层液体中插入两根石墨电极,圆筒内还放有一根下端弯成环状的玻璃搅棒,可以上下搅动液体,装置如右图。接通电源,阳极周围的液体呈现棕色,且颜色由浅变深,阴极上有气泡生成。停止通电,取出电极,用搅棒上下剧烈搅动。静置后液体又分成两层,下层液体呈紫红色,上层液体几乎无色。根据上述实验回答:

(1)阳极上的电极反应式为?。
(2)阴极上的电极反应式为?。
(3)原上层液体是?。
(4)原下层液体是?。
(5)搅拌后两层液体颜色发生变化的原因是?。
(6)要检验上层液体中含有的金属离子?,现象是?。
参考答案:(1)2I-―2e-=I2 。(2)2H++2e?- = H2↑。(3)NaI或KI。(4)四氯化碳。(5)I2易溶于四氯化碳,难溶于水。(6)焰色反应。若焰色为亮黄色为NaI,通过蓝色钴玻璃观察,若焰色为紫色为KI。
本题解析:略
本题难度:一般
3、填空题 碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是一种理想,更是一种值得期待的新的生活方式。
(1)甲烷燃烧放出大量的热,可作为能源用于人类的生产和生活。
已知:①2CH4(g)+3O2(g)=2CO(g)+4H2O(l) △H=" ―1214" kJ/mol
②2CO(g)+O2(g)=2CO2(g) △H=" ―566" kJ/mol
则表示甲烷燃烧热的热化学方程式 。
(2) 将两个石墨电极插入KOH溶液中,向两极分别通入CH4和O2,构成甲烷燃料电池。其负极电极反应式是: 。
(3)某同学利用甲烷燃料电池设计了一种电解法制取Fe(OH)2的实验装置(如下图所示),通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法中正确的是 (填序号)
A.电源中的a一定为正极,b一定为负极
B.可以用NaCl溶液作为电解液
C.A、B两端都必须用铁作电极
D.阴极发生的反应是:2H+ + 2e-= H2↑
(4)将不同量的CO(g)和H2O(g)分别通入体积
为2L的恒容密闭容器中,进行反应:
CO(g)+H2O(g)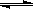 CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
实验组
| 温度/℃
| 起始量/mol
| 平衡量/mol
| 达到平衡所需时间/min
|
H2O
| CO
| CO2
|
1
| 650
| 2
| 4
| 1.6
| 5
|
2
| 900
| 1
| 2
| 0.4
| 3
|
3
| 900
| 1
| 2
| 0.4
| 1
|
①实验1中,以v (H2)表示的平均反应速率为 。
②实验3跟实验2相比,改变的条件可能是 (答一种情况即可)
参考答案:(1)CH4(g)+2O2(g) CO2(g)+2H2O(l) △H1=―890KJ.mol-1
CO2(g)+2H2O(l) △H1=―890KJ.mol-1
(2)CH4-8e-+ 10 OH- CO32-+ 7H2O;
CO32-+ 7H2O;
(3) B、D ;
(4)① 0.16mol/(L・min) ②使用了催化剂;加大了压强(任答一种)
本题解析:(1)甲烷完全燃烧生成二氧化碳气体和液态水,所以甲烷燃烧热的热化学方程式中甲烷的物质的量是1mol,将①②相加除以2可得,答案是CH4(g)+2O2(g) CO2(g)+2H2O(l) △H1=―890KJ.mol-1
CO2(g)+2H2O(l) △H1=―890KJ.mol-1
(2)负极发生氧化反应,所以甲烷在负极发生氧化反应,结合电解质溶液,负极的电极反应式为CH4- 8e-+ 10 OH- CO32-+ 7H2O;
CO32-+ 7H2O;
(3)A、电解过程中两极分别是H+和Fe放电生成氢气和亚铁离子,所以两极哪端都可以生成氢气,a不一定为正极,b不一定为负极,但a为正极,b为负极,效果较好,错误;B、在装置中铁一定作阳极,所以氯化钠溶液是电解质溶液,不影响阳极Fe放电生成亚铁离子,阴极H+放电生成氢气,正确;C、装置中铁一定作阳极,阴极可以是铁,也可以是其他惰性电极,错误;D、阴极H+放电生成氢气,正确,答案选BD。
(4)①实验1中,CO2的浓度增加0.8mol/L,所以氢气浓度也增加0.8mol/L,v (H2)= 0.8mol/L/5min=0.16mol/(L・min);
②实验3跟实验2相比,到达平衡时间缩短,说明反应速率加快,反应温度、各物质的物质的量均未变,所以可能是使用了催化剂或增大压强。
考点:考查盖斯定律得应用,电化学理论的应用,反应速率的计算及条件对反应速率的影响判断
本题难度:困难
4、选择题 电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如下图所示,其中阴极和阳极均为惰性电极。测得同温同压下,气体甲与气体乙的体积比约为1∶2,以下说法正确的是(?)
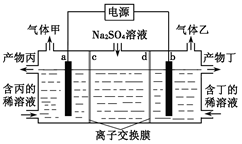
A.a极与电源的负极相连
B.产物丙为硫酸溶液
C.离子交换膜d为阴离子交换膜
D.a电极反应式:2H2O+2e-= H2↑+2OH-
参考答案:B
本题解析:电解硫酸钠溶液,阴极为氢离子放电,产生氢气,阳极为氢氧根离子在放电,产生氧气,因气体甲与气体乙的体积比约为1∶2,故气体甲为氧气,气体乙为氢气,产物丙为硫酸溶液,产物丁为氢氧化钠溶液。故A错误;a极为阳极,与电源的正极相连,A错误;b为阴极,与电源的负极相连;离子交换膜c为阴离子交换膜,允许氢氧根离子通过, 离子交换膜d为阳离子交换膜,允许氢离子通过,C错误;a电极反应式:2H++2e-= H2↑,D错误。
点评:电解池是历年高考常考知识点,注重考查学生分析问题、解决问题的能力。
本题难度:一般
5、选择题 两只串联的电解池,左池放CuSO4溶液,右池放一定量的某硝酸盐稀溶液,电解时,当左池析出1.6g铜时,右池析出0.45g固体,则右池中的溶质为( )
A.AgNO3
B.NaNO3
C.Mg(NO3)2
D.Al(NO3)3
参考答案:左池盛有足量的CuSO4溶液,电解过程中,阴极上的电极反应为:Cu2++2e-=Cu,
当左池析出1.6gCu,物质的量=1.6mol64g/mol=0.025molCu时,转移电子为0.025mol×2=0.05mol,
由选项可知,金属阳离子只有银离子放电,即生成的银为0.45g,转移电子物质的量=0.45g108g/mol×1=0.0042mol<0.05mol,说明氢离子还放电,故右池中的溶质为硝酸银,故选A.
本题解析:
本题难度:简单