微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 根据热化学方程式(在101 kPa时):S(s)+O2(g)====SO2(g) ΔH=-297.23 kJ・mol-1,分析下列说法中不正确的是
[? ]
A.S的燃烧热为297.23 kJ・mol-1
B.S升华是吸热过程
C.S(g)+O2(g) ==SO2(g)放出的热量小于297.23 kJ
D.形成1 mol SO2的化学键释放的总能量大于断裂1 mol S(s)和1 mol O2(g)的化学键所吸收的总能量
2、填空题 氨的合成是最重要的化工生产之一。
I.工业上合成氨用的H2有多种制取的方法:
① 用焦炭跟水反应: C(s)+ H2O(g) CO(g)+ H2(g);
CO(g)+ H2(g);
② 用天然气跟水蒸气反应:CH4(g)+ H2O(g) CO (g)+ 3H2(g)
CO (g)+ 3H2(g)
已知有关反应的能量变化如下图,则方法②中反应的ΔH =__________ ___。
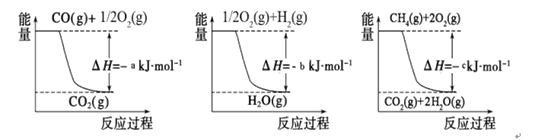
Ⅱ.在3个1L的密闭容器中,同温度下、使用相同催化剂分别进行反应:
3H2(g)+ N2(g) 2NH3(g),按不同方式投入反应物,保持恒温、恒容,反应达到平衡时有关数据为:
2NH3(g),按不同方式投入反应物,保持恒温、恒容,反应达到平衡时有关数据为:
容 器
| 甲
| 乙
| 丙
|
反应物投入量
| 3 mol H2、2 mol N2
| 6 mol H2、4mol N2
| 2 mol NH3
|
达到平衡的时间(min)
| t
| 5
| 8
|
平衡时N2的浓度(mol・L-1)
| c1
| 3
|
|
N2的体积分数
| ω1
| ω2
| ω3
|
混合气体密度(g・L-1)
| ρ1
| ρ2
|
|
(1)下列能说明该反应已达到平衡状态的是
a.容器内N2、H2、NH3的浓度之比为1
3、选择题 下列热化学方程式或离子方程式中,正确的是
[? ]
A.甲烷的标准燃烧热△H为-890.3kJ/mol,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)?△H=-890.3kJ/mol
B.500℃、30MPa下,将0.5molN2(g)和1.5mol?H2(g)置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) 2NH3(g)? △H=?-38.6kJ/mol
2NH3(g)? △H=?-38.6kJ/mol
C.?向明矾溶液中加入过量的氢氧化钡溶液:
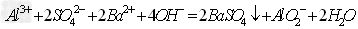 ?
?
D.?用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO42-?+?6H+?+?5H2O2?=?2Mn2+?+?5O2↑?+?8H2O?
4、选择题 已知充分燃烧ag乙炔气体时生成1mol二氧化碳气体和液态水,并放出热量bkJ,则乙炔燃烧的热化学方程 式正确的是
[? ]
A.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H = -2bkJ/mol
B.C2H2(g)+5/2O2(g)=2CO2(g)+H2O(l) △H =2bkJ/mol
C.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H=-4bkJ/mol
D.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H =bkJ/mol
5、简答题 按要求完成各题
(1)已知,1mol?N2(g)与足量O2(g)起反应,生成2mol?NO2(g),吸收68kJ的热量.该反应的热化学方程式可表示为:
______
(2)写出下列各物质的电离方程式:CH3COOH______;NH3?H2O______
(3)写出下列各物质水解的离子方程式:NaHCO3______;AlCl3______
(4)把足量的碳酸钙粉末放入水中,建立的溶解平衡可表示为:______.