微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在一定条件下,RO3-与R-可发生反应:RO3-+5R-+6H+===3R2+3H2O,下列关于R元素的叙述中,正确的是
[? ]
A.元素R位于周期表中第ⅤA族?
B.RO3-中的R只能被还原
C.R2在常温常压下一定是气体
D.若1?mol?RO3-参与该反应,则转移的电子的物质的量为5?mol?
参考答案:D
本题解析:
本题难度:简单
2、填空题 (6分)化合物BrFx与水按物质的量之比为3∶5发生反应,其产物为溴酸、氢氟酸、单质溴和氧气。(1)BrFx中,x=?。
(2)该反应的化学方程式是?。
(3)此反应中的氧化剂是_________和还原剂是_________。
参考答案:(1)3(2分)?(2)2BrF3+5H2O===HBrO3+9HF+Br2+O2↑?(2分)
(3)BrF3为氧化剂;还原剂为H2O、BrF3。?(各1分)
本题解析:
3BrFX+5H2O===(10-3x)HBrO3+3XHF+yBr2+zO2↑
原子守恒:O: 5=3(10-3x)+2z
Br: 3=(10-3x)+2y
电子守恒:4z+(1-3x)(5-x)=2yx
X=3,y=1,z=1
⑴3(2)3BrF3+5H2O===HBrO3+9HF+Br2+O2↑?(2分)
(3)BrF3为氧化剂;还原剂为H2O、BrF3。
本题难度:一般
3、填空题 (10分)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:?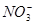 +4H++3e-=NO+2H2O 。?已知Cu2O能使上述还原过程发生。
+4H++3e-=NO+2H2O 。?已知Cu2O能使上述还原过程发生。
(1)写出并配平该氧化还原反应的化学方程式:______________?。
(2)反应中硝酸体现了________、_________的性质。
(3)反应中若产生0.2 mol气体,则转移电子的物质的量是___________mol。
(4)若1 molCu2O与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是__________? ?_。
?_。
参考答案:(10分)
(1)14HNO3+3Cu2O====6Cu(NO3)2+2NO↑+7H2O(2分)
(2)酸性(2分)氧化性(2分)
(3)0.6(2分)
(4)使用了较浓的硝酸,产物中有部分二氧化氮生成(2分)
本题解析:略
本题难度:一般
4、选择题 在浓盐酸中H3AsO3与SnCl2反应的离子方程式为:3SnCl2+12Cl-+2H3AsO3+6H+===2As+3SnCl+6M,关于该反应的说法中正确的组合是? ( )
①氧化剂是H3AsO3 ②还原性:Cl->As ③每生成7.5 g As,还原剂失去的电子为0.3 mol ④M为OH- ⑤SnCl是氧化产物
A.①③⑤
B.①②④⑤
C.①②③④
D.①③
参考答案:A
本题解析:
分析:离子方程式3SnCl2+12Cl-+2H3AsO3+6H+=2As+3SnCl62-+6M中,Sn的化合价由+2价升高到+4价,As元素的化合价由+3价降低到0价,从化合价的角度分析氧化还原反应,判断有关氧化剂、还原剂等概念,并判断物质的性质,从守恒的角度判断M的组成.
解:①H3AsO3中As元素的化合价降低,H3AsO3为氧化剂,故①正确;
②反应中Cl元素的化合价没有发生变化,不能比较二者的还原性强弱,故②错误;
③H3AsO3中As元素的化合价由+3价降低到0价,每生成1molAs,反应中转移电子的物质的量为3mol,故③正确;
④根据离子方程式的电荷守恒可知M不带电荷,从质量守恒的角度分析可知应为H2O,故④错误;
⑤SnCl2→SnCl62-,Sn元素的化合价升高,SnCl62-是氧化产物,故⑤正确.
故选A.
本题难度:简单
5、选择题 三聚氰酸[C3N3(OH)3]可用于消除汽车尾气中的NO2。其反应原理为:
C3N3(OH)3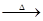 3HNCO;8HNCO+6NO2
3HNCO;8HNCO+6NO2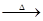 7N2+8CO+4H2O。
7N2+8CO+4H2O。
下列说法止确的是
A.C3N3(OH)3与HNCO为同一物质
B.1mol HNCO与NO2反应时转移3mol电子
C.HNCO是强氧化剂
D.反应中CO2是氧化产物
参考答案:B
本题解析:A、由方程式C3N3(OH)3 3HNCO可知,C3N3(OH)3与HNCO的化学式不同,反应属于化学变化,则C3N3(OH)3与HNCO为不同物质,故A错误;B、1mol?HNCO与NO2反应时转移电子=1mol×[0-(-3)]=3mol,故B正确;C、HNCO在反应中N元素的化合价升高,则HNCO是还原剂,故C错误;D、该反应中碳元素的化合价不变,所以二氧化碳既不是氧化产物也不是还原产物,故D错误,答案选B。
3HNCO可知,C3N3(OH)3与HNCO的化学式不同,反应属于化学变化,则C3N3(OH)3与HNCO为不同物质,故A错误;B、1mol?HNCO与NO2反应时转移电子=1mol×[0-(-3)]=3mol,故B正确;C、HNCO在反应中N元素的化合价升高,则HNCO是还原剂,故C错误;D、该反应中碳元素的化合价不变,所以二氧化碳既不是氧化产物也不是还原产物,故D错误,答案选B。
本题难度:一般