��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���й���������˵���У��������
A�������������֣�Ŀ���dz�ȥ�����ж����̼����������
B�������� ��֧��ȼ�գ�˵���������п�ȼ��
C���������Թ�������������Ϊ���������ʷ�Ӧ���ͷ�������ά�������
D����������ڷ������ã�����Ϊ�¶����ߣ�������ˮ���ܽ�������
�ο��𰸣�B
���������A�������ֵ�������Ǻ�̼����ͬ���������������dz�ȥ�����ж����̼��������������ȷ�ģ�����ȷ��
B����������֧��ȼ�գ�˵������������ȼ�ԣ������ǿ�ȼ�ԣ��ʴ���
C���������Թ�������������Ϊ���������ʷ�Ӧ���ͷ�������ά���������˵����ȷ������ȷ��
D������������ܽ�����¶ȳɷ��ȣ������¶ȸߣ��������ܽ��С��������������ȷ�ģ�����ȷ��
��ѡB��
�����Ѷȣ�һ��
2��ѡ���� ��ұ��ҵ�ϣ���������ͨ����ѧ��ԭ���ƵõĽ�������(����)��
A��Na��Mg��Al
B��Na��K��Zn��Fe
C��Zn��Fe��Cu��Ag
D��Mg��Al��Zn��Fe
�ο��𰸣�A
������������ݽ����Ļ��˳��������ұ���������ٴ�K��Al���õ�ⷨ����Zn��Cu�û�ԭ��(��H2��CO��)��ԭ������Hg��Ag�ü��ȷֽⷨ2HgO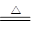 2Hg��O2����
2Hg��O2����
�����Ѷȣ���
3��ѡ���� ��ͭ�ۺ��������ۼ��뵽�ȵ�Ũ�����У���ַ�Ӧ����Һ�д������ڵĽ�����������?��?��
A��ֻ��Fe2+
B��ֻ��Fe3+
C����Fe2+��Cu2+
D����Fe3+��Cu2+
�ο��𰸣�A
��������� Ũ�������ǿ�����ԣ��ȵ�Ũ����ɽ�Fe��Cu�ֱ�������Fe3+��Cu2+��������������Fe2+��Cu2+��Ӧ����Fe2+��Cu�����Գ�ֺ���Һ�д������ڵĽ���������ΪFe2+����ѡA��
Ũ�������ǿ�����ԣ��ȵ�Ũ����ɽ�Fe��Cu�ֱ�������Fe3+��Cu2+��������������Fe2+��Cu2+��Ӧ����Fe2+��Cu�����Գ�ֺ���Һ�д������ڵĽ���������ΪFe2+����ѡA��
�����Ѷȣ�һ��
4��ѡ���� ��֪�������������ܷ������з�Ӧ��Cu���� Cu��Cu2��(δ��ƽ)��NH4CuSO3��������2mol��L-1������Һ����ȣ����������������Ϻ�ɫ�������ɣ����д̼�����ζ�������������Һ����ɫ���ݴ��ж�����˵��һ����������
A���÷�Ӧ��ʾ�����������
B��NH4CuSO3����Ԫ�ر�����
C���̼�����ζ�������Ƕ�������
D����Ӧ��������������
�ο��𰸣�AC
���������
����������������֪Aѡ������ȷ�ģ��������д̼�����ζ�Ƕ�����������ǰ�����Ҫԭ���Ǹ���ҺΪ������Һ����������Ӧ������ֻ��ͭԪ�صĻ��ϼ۷����仯����B��Dѡ��Ǵ���ġ�
����;��������֪ʶ�����Ӧ��
�����Ѷȣ�һ��
5������� ����ս̰滯ѧ1��75ҳ�ϡ����������Խ������������������ᡢ����ͭ��Һ�ȣ���Ӧת��Ϊ+2�����Ļ��������������Խ�ǿ������������������˫��ˮ�ȣ���Ӧ��ת��Ϊ+3�۵Ļ��������������ѧ�о���ѧϰС����ͨ������ʵ��̽�������ƵĻ�ԭ�����ۺ�����ķ�Ӧ���������������������̽�����ش��й����⣺
��1������KSCN��H2O2��ҩƷ���鷴Ӧ��Ļ��Һ�к��ж�������ʵ�鷽����������______������ʵ���������ֿ�����ɫѸ����ȥ��ͬʱ��Һ�ʻ�ɫ������ܵ�ԭ����______��ѧ������ʵ��ʱ�����μ�˫��ˮ��Ũ�ȹ����߹�����������Ѹ�ٲ����������ݣ�д������������Ļ�ѧ����ʽ��______��
��2�������Ͻ��ܡ�ȡ������ӦҺ�������������ȵμ��������Ʊ�����ˮ��Ȼ��μ�KSCN��Һ������Ѫ��ɫ�����ٵμӹ���������ˮ��ȴ���ֺ�ɫ��ȥ��ͬѧ�Ժ�ɫ��ȥ��ԭ��������Եļ��裮ijͬѧ�ļ����ǣ���Һ�е�+3����������Ϊ���ߵļ�̬�������+3����������ΪFeO42-����д���÷�Ӧ�����ӷ���ʽ______��
��3��̽��������ص�ij�����ʣ�
��ʵ��һ��������K2FeO4����ֱ��ܽ���pH?Ϊ?4.74��7.00��11.50?��ˮ��Һ�У����FeO42-Ũ��Ϊ?1.0mmol?L-1��1mmol?L-1=10-3mol?L-1�������������ã����첻ͬ��ʼ?pH?��ˮ��Һ��K2FeO4ij�����ʵ�Ӱ�죬�����ͼ1��ע��800min��������Һ�и�����ص�Ũ�Ȳ��ٸı䣩��


���������������?K2FeO4�ܽ���pH=4.74?��ˮ��Һ�У����Ƴ�FeO42-Ũ��Ϊ?1.0mmol?L-1?���������������ֱ�����?20�桢30�桢40���?60��ĺ���ˮԡ�У����첻ͬ�¶ȶ�K2FeO4ij�����ʵ�Ӱ�죬�����ͼ2����
��ʵ��1��Ŀ����______��
��ʵ��2�ɵó��Ľ�����______��
�۸��������ˮ�еķ�ӦΪ4FeO42-+10H2O?4Fe��OH��3+8OH-+3O2������ͼ1��֪��800minʱ��pH=11.50����Һ�и����������Ũ�ȱ�pH=4.74����Һ�иߣ���Ҫԭ����______��
�ο��𰸣���1�����������Ӿ��л�ԭ�ԣ���������KSCN��Һ��Ѫ��ɫ����KSCN��H2O2��ҩƷ���鷴Ӧ��Ļ��Һ�к��ж�������ʵ�鷽�����������ȼ����軯����Һ���������ٵμ�˫��ˮ������������Һ��Ѫ��ɫ����ʵ���������ֿ�����ɫѸ����ȥ��ͬʱ��Һ�ʻ�ɫ������ܵ�ԭ�������������������ʵ��ʱ�����μ�˫��ˮ��Ũ�ȹ����߹�����������Ѹ�ٲ����������ݣ�����2H2O2?FeCl3?.?2H2O+O2����
�ʴ�Ϊ���ȼ����軯����Һ���������ٵμ�˫��ˮ������������Һ��Ѫ��ɫ���������������2H2O2?FeCl3?.?2H2O+O2����
��2������Ϣ��֪�������ӱ���������ΪFeO42-�����ᣬ�����ӷ�ӦΪ2Fe3++3Cl2+8H2O�T2FeO42-+6Cl-+16H+��
�ʴ�Ϊ��2Fe3++3Cl2+8H2O�T2FeO42-+6Cl-+16H+��
��3������ʵ��һ��֪��pH��ͬ��FeO42-�ȶ��Բ�ͬ����ʵ��1��Ŀ��Ϊ�о�FeO42-�ڲ�ͬpH��Һ�е��ȶ��ԣ���Ӧ�����ʣ���
�ʴ�Ϊ���о�FeO42-�ڲ�ͬpH��Һ�е��ȶ��ԣ���Ӧ�����ʣ���
����ͼ2��֪���¶Ȳ�ͬ��FeO42-�ȶ��Բ�ͬ������ʵ��2�ɵó��Ľ������¶�Խ�ߣ�FeO42-Խ���ȶ�������ˮ��Ӧ������Խ�죩��
�ʴ�Ϊ���¶�Խ�ߣ�FeO42-Խ���ȶ�������ˮ��Ӧ������Խ�죩��
����ͼ1��֪��800minʱ��pH=11.50����Һ�и����������Ũ�ȱ�pH=4.74����Һ�иߣ���pH=11.50����Һ��OH-����Ũ�ȴ�ʹ4FeO42-+10H2O?4Fe��OH��3+8OH-+3O2��ƽ�������ƶ���
�ʴ�Ϊ��pH=11.50����Һ��OH-����Ũ�ȴ�ʹƽ�������ƶ���
���������
�����Ѷȣ�һ��