��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����ʵ���н����������������ȫ�ܽ����
A��1 molͭƬ�뺬2 mol H2SO4��Ũ���Ṳ��
B��1 mol MnO2��ĩ�뺬2 mol H2O2����Һ����
C��������1 mol��ƬͶ��������Ũ������
D��������1 molͭƬͶ�뺬4 mol HNO3��Ũ������
�ο��𰸣�D��?
���������A��Cu��ŨH2SO4��Ӧ�����淴Ӧ�Ľ��У���Һ��ϡ��Cu��ʣ�࣬B��MnO2ΪH2O2�ֽ�Ĵ�����C��Al�ڳ����£���Ũ�����жۻ���D��Cu��4HNO3(Ũ)===Cu(NO3)2��2NO2����2H2O������n(Cu)��n(HNO3)��1��4�����淴Ӧ�Ľ��У�ŨHNO3��ϡ��������Ӧ3Cu��8HNO3(ϡ)===3Cu(NO3)2��2NO����4H2O����ʱn(Cu)��n(HNO3)��3��8>1��4����HNO3����ʣ�࣬Cu��ȫ�ܽ⡣
�����Ѷȣ�һ��
2��ѡ���� ������������Ͷ�뵽�ܽ������������ͭ����Һ��,��ַ�Ӧ��,ʣ�������ĩ��������ԭ�������۵��������,��ԭ��Һ��H+��SO42-�����ʵ���Ũ��֮��Ϊ
A��1:4
B��2:7
C��1:2
D��3:8
�ο��𰸣�A
������������ա���������������
���۷����ķ�ӦΪ��������ͭ������ֱ�Ϊxmol��ymol����
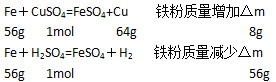
�������֪��8x=56y����x:y=7��1
��ɼ����ԭ��Һ��H+��SO42-�����ʵ���Ũ��֮��Ϊ��2��1����7+1��=1��4
��ΪA
�����Ѷȣ�һ��
3��ѡ���� ���������У���̼����ߵ���
A����̼��
B������
C����̼��
D���Ͻ��
�ο��𰸣�D
����������Ͻ����̼�ĺ�����2����4��֮�䣬��̼�ظ���̼�İٷֺ�����0.3����2��֮�䡣
�����Ѷȣ���
4��ѡ���� ��һ�������׳����죬��������ɫ�����Ϳ�ϣ����Ļ�ѧʽΪ(? )
A��FeO
B��Fe2O3
C��Fe
D��Fe3O4
�ο��𰸣�B
���������
����������ʴʱ�������⣬��Ϊԭ���ԭ��������2Fe-4e-=2Fe2+,����4e-+O2+2H2O=4OH-���ܷ�Ӧʽ2Fe+O2+2H2O=2Fe(OH)2�������������������е���������Ϊ�������������������ٷֽ�����������Fe2O3�����Ǻ�ɫ���ʣ��׳����졣
�����Ѷȣ���
5������� ��2.0 mol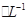 CuSO4��1.0 mol
CuSO4��1.0 mol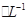 H2SO4��Һ�������ϣ������Ϻ����Һ��������ڻ��ǰ������Һ�����֮�ͣ����㣺?
H2SO4��Һ�������ϣ������Ϻ����Һ��������ڻ��ǰ������Һ�����֮�ͣ����㣺?
��1�������Һ��CuSO4��H2SO4�����ʵ���Ũ��
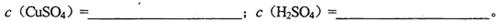
��2�����Һ�к͵����ʵ���Ũ��

��3������Һ�м������ۣ������㹻����ʱ�䣬������ʣ�ࡣ��ʱ��Һ�е����ʵ���Ũ�ȡ�c(Fe2��)=_______________________��
�ο��𰸣���1��1.0mol/L��0.5mol/L��
��2��1mol/L��1.5mol/L����3��1.5mol/L
�����������1����2.0mol?L-1CuSO4��1.0mol?L-1H2SO4��Һ�������ϣ�����ϡ�Ͷ��ɣ�ϡ��ǰ�����ʵ����ʵ������䣬���Ϻ���Һ��c��CuSO4��="1/2��1.0mol/L=1.0" mol/L��c��H2SO4��=1/2��1.0mol/L=0.5mol/L��
��2����Ϻ���Һ��c��H+��=2c��H2SO4��=2��0.5mol/L=1mol/L��
��Һ���������Դ������ͭ��������룬�� c��SO42-���Tc��CuSO4��+c��H2SO4��=1mol/L+0.5mol/L=1.5mol/L��
��3������Һ�м������ۣ������㹻����ʱ�䣬������ʣ�࣬������ͭ�����ᶼ��ȫ��Ӧ����ʱ��Һ������ΪFeSO4����c��Fe2+��=c��SO42-��=1.5mol/L��
�����Ѷȣ�һ��