��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��2 L�ܱ������ڣ�800 ��ʱ��Ӧ��2NO(g)+O2(g) 2NO2(g)����H��0��ϵ�У�n(NO)��ʱ��ı仯�����
2NO2(g)����H��0��ϵ�У�n(NO)��ʱ��ı仯�����
ʱ��(s)
| 0
| 1
| 2
| 3
| 4
| 5
|
n(NO)(mol)
| 0.020
| 0.010
| 0.008
| 0.007
| 0.007
| 0.007
|
��1����O2��ʾ��0~2s�ڸ÷�Ӧ��ƽ������v=?��
 ��2����ͼ�б�ʾNO2Ũ�ȵı仯��������?��
��2����ͼ�б�ʾNO2Ũ�ȵı仯��������?��
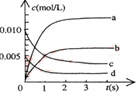
��3����˵���÷�Ӧ�Ѵﵽƽ��״̬����?��
A��v(NO2)=2v(O2)?B��������ѹǿ���ֲ���
C��v��?(NO)=2v�� (O2)?D���������ܶȱ��ֲ���
��4��Ϊʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ�����?��
A����ʱ�����NO2����?B���ʵ������¶�?
C������O2��Ũ��?D��ѡ���Ч����
�ο��𰸣�(1)0.0015? (2)b? (3)BC? (4) c
�����������1����Ӧ����ͨ���ɵ�λʱ����Ũ�ȵı仯������ʾ����0~2s��NO������0.020mol��0.008mol��0.012mol������������0.006mol����O2��ʾ��0~2s�ڸ÷�Ӧ��ƽ������v�� ��
��
��2��NO2���������2sʱ���ݣ�1����֪������0.012mol����Ũ��Ϊ0.006mol/L����������b��ȷ��
��3��NO2�ĺ������ķ�Ӧ����֮��ʼ����2�U1��A����ȷ����Ӧǰ������DZ仯�ģ���ѹǿҲ�DZ仯�ģ�����B����˵������ѡ��C�з�Ӧ���ʵķ������෴�ģ�����������֮������Ӧ�Ļ�ѧ������֮�ȣ���ȷ���ܶ����������������������ı�ֵ����Ϊ�ڷ�Ӧ����������������������������䣬�����ܶ�ʼ�ղ��䡣
��4��A�н���������Ũ�ȣ���Ӧ���ʽ��͡������¶ȣ�ƽ�����淴Ӧ�����ƶ����������ܸı�ƽ��״̬������Ӧ��Ũ�ȣ�ƽ��������Ӧ�����ƶ�����ȷ�����Դ���C��
�����Ѷȣ���
2��ѡ���� ��һ���¶��£���a L����̶����ܱ������м���1 mol X�����2 mol Y���壬�������·�Ӧ��X(g) + 2Y(g)  3Z(g)������˵������ȷ����
3Z(g)������˵������ȷ����
A��������ѹǿ����ʱ��仯���仯
B��ijһʱ�̣������ڸ����ʵ�Ũ���п������
C���ﵽƽ��ʱ����λʱ��������3n mol Z��ͬʱ���� 2n mol Y
D��X��Y��ת�������
�ο��𰸣�B
���������A��ȷ���÷�ӦΪ�������Ӧ����Ӧǰ������������ʵ������䣬������ѹǿ���䡣
B����������X��Y�����ʵ���Ϊ1 mol X�����2 mol Y���壬�뻯ѧ��������ֵ��ȣ����ԣ�X��Y�����ʵ�ת������ȣ��仯������ȣ������ܻ����ijһʱ�̣������ڸ����ʵ�Ũ����ȵ������
C��ȷ����λʱ��������3n mol Z������Y2n mol����ͬʱ��������2n mol Y��Y��Ũ�Ȳ��䣬���ﵽ��ƽ�⣻
D��ȷ��X��Y��ת�������
�����Ѷȣ�һ��
3��ѡ���� �п��淴ӦmA(s)+nB(g)? pC(g)+qD(g)����Ӧ�����У���������������ʱ��C�������������¶ȣ�T����ѹǿ��P���Ĺ�ϵ��ͼ��ʾ������ͼ�����߷������ж����������У���ȷ����
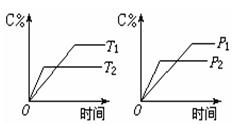
A������ƽ�����ʹ�ô�����C��������������
B��ƽ����������¶ȣ�ƽ�������淴Ӧ�����ƶ�
C��ƽ�������A���������������A��ת����
D����ѧ����ʽ��һ����n��p+q
�ο��𰸣�B
�����������
�����Ѷȣ���
4��ѡ���� ���ڿ��淴Ӧ4NH3+5O2 4NO+6H2O(g)��������������ȷ���� ��?��?
4NO+6H2O(g)��������������ȷ���� ��?��?
A���ﵽƽ��ʱ��4v��O2����=5v��NO����
B���ﵽƽ��״̬��NH3��O2��NO ��H2O(g)�����ʵ������ֲ��䡣
C���ﵽƽ��״̬ʱ�������������������Ӧ��������
D������λʱ������xmolNO��ͬʱ������xmolNH3����Ӧ�ﵽƽ��״̬
�ο��𰸣�C
���������A���ﵽƽ��ʱ��4v��O2����=5v��NO���棬��ȷ��B���ﵽƽ��״̬��NH3��O2��NO ��H2O(g)�����ʵ������ֲ��䣬��ȷ��C���ﵽƽ��״̬ʱ������������������൱�ڼ�Сѹǿ����Ӧ���ʼ�С������D������λʱ������xmolNO��ͬʱ������xmolNH3����Ӧ�ﵽƽ��״̬����ȷ��
�����Ѷȣ�һ��
5�������� ��9�֣������£���a mol N2��b mol H2��һ��������ϣ�����ͬ״�������ܶ���H2�� 3.6����ȡ5mol�û������ͨ���ܱ������ڣ�ʹ֮������Ӧ����һ�������´ﵽƽ�⡣��֪��Ӧ�ﵽƽ���������ѹǿ����ͬ�����·�Ӧǰѹǿ��0.92��������
��1����Ӧǰ���������N2��H2�������a�sb=__________��
��2���ﵽƽ��ʱ��������е�H2��NH3�����ʵ����ֱ���_____mol��?mol��
����С�����������̣�
��3��ƽ��ʱN2��ת����[nת��(N2)��n��ʼ(N2)֮��]________________��
�ο��𰸣���1��1��4��2�֣�
��2��3.4��0.4
��3��20%��2�֣�
���������
��1��1��4��2�֣�
��2��3.4��0.4
������̣����ƽ��ʱת����N2�����ʵ���Ϊx
N2 �� 3H2 2NH3
2NH3
��ʼ/mol? 1? 4? 0
ת��/mol ? x?3x?2x
ƽ��/mol 1��x? 4��3x? 2x
��������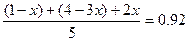 ����x=0.2
����x=0.2
n(H2)= 4��3x="3.4?" n(NH3)=2x=0.4�����2�֣�����3�֣�����������̺���Ҳ���֣�
��3��20%��2�֣�
�����Ѷȣ���