微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某小组为研究原电池原理,设计如图装置,下列叙述正确的是
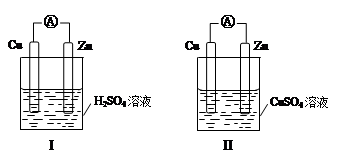
A.装置I,铜片上有O2逸出
B.装置I,锌片溶解,发生还原反应
C.装置II,电池反应为:Zn+ Cu2+= Zn2++ Cu
D.装置II,外电路中,电子从锌电极流向铜电极
参考答案:CD
本题解析:A、装置I为原电池,铜片上有氢气逸出,错误;B、装置I为原电池,锌片溶解作负极,错误;C、装置II中锌作负极,铜作正极,电池反应为锌与铜离子的置换反应,正确;D、原电池装置中,电子从外电路的负极流向正极,正确,答案选CD。
本题难度:一般
2、填空题 (12分)近年来北京市汽车拥有量呈较快增长趋势,汽车尾气已成为重要的空气污染物。
(1)汽车内燃机工作时引起反应:N2(g)+O2(g)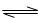 2NO(g),是导致汽车尾气中含有NO的原因之一。T℃时,向容积为2 L的密闭容器中充入10molN2与5molO2,达到平衡后NO的物质的量为2mol,则T℃时该反应的平衡常数K=?。(计算结果保留小数点后两位数字)
2NO(g),是导致汽车尾气中含有NO的原因之一。T℃时,向容积为2 L的密闭容器中充入10molN2与5molO2,达到平衡后NO的物质的量为2mol,则T℃时该反应的平衡常数K=?。(计算结果保留小数点后两位数字)
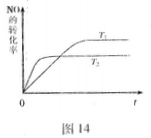
(2)一定量的NO发生分解的过程中,NO的转化率随时间变化的曲线如图14所示。(已知: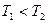 )
)
①反应2NO(g)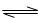 N2(g)+O2(g)为(填“吸热”或“放热)?反应。
N2(g)+O2(g)为(填“吸热”或“放热)?反应。
②一定温度下,能够说明反应2NO(g)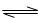 N2(g)+O2(g)已达到平衡的是(填序号)?。
N2(g)+O2(g)已达到平衡的是(填序号)?。
a.容器内的压强不发生变化
b.NO、N2、O2的浓度保持不变
c.NO分解的速率和NO生成的速率相等
d.单位时间内分解4mol NO,同时生成2 mol N2
(3)①当发动机采用稀薄燃烧时,尾气中的主要污染物为NOx,可用CxHy(烃)催化还原NOx消除氮氧化物的污染。
已知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)?△H1=-574kJ・mol-1
CH4(g)+4NO(g)=2N2(g)=CO2(g)+2H2O(g)?△H2
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)?△H3=-867kJ・mol-1
△H2=?.
②使用催化剂可以将汽车尾气的主要有害成分一氧化碳(CO)和氮氧化物(NO2)转化为无毒气体,该反应的化学方程式为?。
参考答案:
(1)0.11(1/9给分)? ………………………………………………2分
(2)①放热?………………………………………………………2分
②bc? …………………………………………………………2分
(3)①-1160 kJ・mol-1? ………………………………………………………3分
(不写单位、“-”扣1分)
② 2x CO + 2NOx ?2x CO2 + N2? ………………………………………3分
?2x CO2 + N2? ………………………………………3分
本题解析:略
本题难度:一般
3、选择题 关于原电池的叙述中正确的是
A.构成原电池的电极是两种不同的金属
B.原电池是将化学能转化为电能的装置
C.原电池负极发生的电极反应是还原反应
D.原电池的正极是还原剂,总是溶液中的阳 离子在此被还原
离子在此被还原