|
|
|
高中化学知识点总结《原电池原理》答题技巧(2017年最新版)(五)
2017-08-22 15:27:58
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
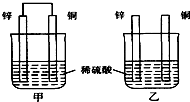
1、选择题 将纯锌片和纯铜片按图示方式插入同浓度同体积的稀硫酸中一段时间,以下叙述正确的是( )
A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯的溶液中H+浓度均减小
D.乙装置中化学能转化为电能
| 
2、选择题 在理论上不能用于设计原电池的化学反应是
[? ]
A.HCl(aq)+ NaOH(aq)= NaCl(aq)+ H2O(l) △H < 0
B.2CH3OH(l)+3O2(g)= 2CO2(g)+ 4H2O(l) △H < 0
C.4Fe(OH)2 (s)+ 2H2O(l)+ O2 (g)= 4Fe(OH)3 (s) △H < 0
D.2H2(g)+ O2(g)= 2H2O(l) △H < 0
3、填空题 (17分)I.工业上有一种用CO2来生产甲醇燃料的方法:
将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如下图所示(实线)。图中数据a(1,6)表示:在1 min时H2的物质的量是6 mol。
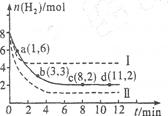
(1)a点正反应速率?(填“大于”“等于”或“小于”)逆反应速率。其化学平衡常数K=?
(2)下列时间段平均反应速率最大的是?,
A.O~1 min
B.1~3 min
C.3~8 min
D.8~11 min
|
(3)仅改变某一实验条件再进行两次实验测得H2的物质的量随时间变化如图中虚线所示。曲线I对应的实验条件改变是
?,曲线Ⅱ对应的实验条件改变是
??,体积不变再充入3molCO2和4 mol H2,H2O(g)的体积分数
?(填“增大”“不变”或“减小”)
Ⅱ.某实验小组欲探究反应速率与温度的关系,现有1mol/L的KI溶液、0.1mol/L的H2S04溶液、淀粉溶液,则实验时这几种试剂的加入顺序为:KI溶液、
?、
?;
反应的方程式为
?Ⅲ. 粗镍样品中含Fe、Zn、Ag、Cu等四种金属杂质,为获得高纯度的镍,某兴趣小组同学拟用铅蓄电池为电源,粗镍及石墨为电极,电解硝酸镍溶液对粗镍进行提纯。
(1)电解结束后,在阳极附近的沉淀物中,主要的金属单质为
??(填化学式)。
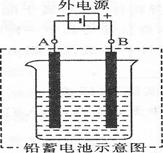
(2) 若按上图所示连接对铅蓄电池进行充电。充电一段时间后。则在A电极上生成
?(填化学式)。B电极上的电极反应式为
?;充电完毕。铅蓄电池的正极是
?极(填“A”或“B”)。
(3)如用甲烷燃料电池为电源,在25℃、101 kPa时,若CH4在氧气中直接燃烧生成1 mol水蒸气放热401 kJ,而l g水蒸气转化成液态水放热2.445 kJ,则CH4的燃烧热为
?(取整数)kJ・mol-。
4、选择题 下列有关电化学的示意图正确的是(?)
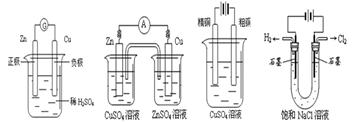
A? B?C (电解精炼铜) D
5、填空题 因“召回门”而闹得沸沸扬扬的丰田Prius属第三代混合动力车,可以用电动机、内燃机或二者结合推动车轮。汽车上坡或加速时,电动机提供推动力,降低了汽油的消耗;在刹车和下坡时电动机处于充电状态。
(1)混合动力车的内燃机以汽油为燃料,汽油(以辛烷C8H18计)和氧气充分反应,每生成1mol水蒸气放 热569.1 kJ。则该反应的热化学方程式为___________________
(2)混合动力车的电动机目前一般使用的是镍氢电池, 镍氢电池采用镍的化合物为正极,储氢金属(以M 表示)为负极,碱液(主要为KOH)为电解液。
①镍氢电池充放电原理如图所示(图中MH为吸附了氢原子的储氢合金),其总反应式是____________________。
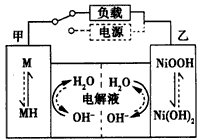
②根据所给信息判断,混合动力车下坡或刹车时,甲电极的电极反应式为_________________;混合动力车上坡或加速时,乙电极的电极反应式为____________________
(3)汽车尾气中的一氧化碳是大气污染物,可通过如下反应降低其浓度:CO(g) +1/2O2(g) CO2(g)
CO2(g)
①某温度下,在两个容器中进行上述反应,容器中各物质的起始浓度及正、逆反应速率关系如下表所 示。请填写表中的空格。

②相同温度下,某汽车尾气中CO、CO2的浓度分别为1.0×10-5mol/L和1.0×10-4mol/L。若在汽车的排气管上增加一个补燃器,不断补充O2并使其浓度保持为1.0×10-4mol/L,则最终尾气中CO的浓度为____mol/L。




 CO2(g)
CO2(g) 