| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学必考知识点《水的电离平衡》考点预测(2017年强化版)(六)
参考答案:B 本题解析:溶液呈酸性实质是c(H+)>c(OH-),A、pH<7,不一定显酸性,如水在100℃时,PH=6呈中性,错误;B、溶液中存在电荷守恒c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A 2-),c(Na+)=c(A2-),则 c(H+)>c(OH-),正确;C、溶液中可能不存在HA-、H2A ,H2A可能是强酸,如NaHSO4溶液中不存在H2SO4,错误;D、溶液可与等体积等物质的量浓度的NaOH溶液恰好反应,说明该物质为酸式盐,但不能说明溶液中氢离子和氢氧根离子浓度相对大小,所以不能说明原溶液呈酸性,错误。 本题难度:一般 3、选择题 下列电离方程式中,正确的是( ? ) | D.Na2CO3=Na++CO32- 参考答案:B 本题解析: 本题难度:简单 4、实验题 (11分)草酸晶体的组成可用H2C2O4・xH2O表示,为了测定x值,进行如下实验: |
参考答案:(1) 2KMnO4 +5H2C2O4 + 3H2SO4 = K2SO4 + 10CO2↑ +2MnSO4 + 8H2O
(2) H2C2O4 H++HC2O4-、HC2O4-
H++HC2O4-、HC2O4- H++C2O42-,第一步电离产生的氢离子抑制第二步电离 22.0 D
H++C2O42-,第一步电离产生的氢离子抑制第二步电离 22.0 D
(3)酸 无影响 无色 紫红
(4)0.1aVmol/L
(5)84.00%
本题解析:(1)高锰酸钾和草酸溶液反应化学方程式为2KMnO4 +5H2C2O4 + 3H2SO4 = K2SO4 + 10CO2↑ +2MnSO4 + 8H2O。
(2)草酸电离方程式为:H2C2O4 H++HC2O4-、HC2O4-
H++HC2O4-、HC2O4- H++C2O42-,第一步电离产生的氢离子抑制第二步电离。
H++C2O42-,第一步电离产生的氢离子抑制第二步电离。
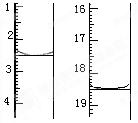
量筒刻度由下向上逐渐增大,每一格表示2.0mL,量筒中液体的体积为22.0mL;滴定管刻度从上到下增大,最大刻度下面还有部分液体,滴定管中液体的体积一定大于(25-a)mL。
(3)高锰酸钾溶液有强氧化性,应盛装在酸式滴定管中,若在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,再继续滴定至终点,则所测得的x值无影响,终点现象是滴加最后一滴高锰酸钾溶液,溶液由无色变为紫红色且30s不褪色。
(4)2KMnO4 ~ 5H2C2O4
2 5
0.001avmol 0.025c
c=0.1avmol/L
(5)消耗高锰酸钾溶液体积为16.00mL。设草酸晶体物质的量为nmol。
5H2C2O4・2H2O~2 KMnO4
5 2
nmol 0.02×0.016mol
n=0.0008mol
H2C2O4・2H2O质量分数为84%。
考点:电离方程式 化学实验 氧化还原滴定
点评:用高锰酸钾溶液滴定草酸因高锰酸钾溶液本身有颜色,不需外加指示剂。
本题难度:一般
5、填空题 (7分)NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,
用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛.请回答下列问题: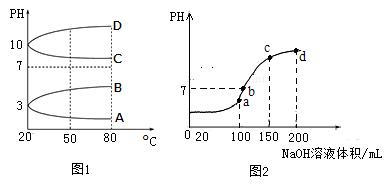
(1)相同条件下,相等物质的量浓度的NH4Al(SO4)2中c(NH4+) (填“=”、“>”“<”)NH4HSO4中c(NH4+)。
(2)如图1是0.1mol?L
参考答案:
本题解析:
本题难度:困难
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点整理《原电池原理.. | |