��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��ijԭ�ӵ���Χ�����Ų�ʽΪ4d15s2��������˵����ȷ����
[? ]
A.��Ԫ�ػ�̬ԭ���й���36������
B.��Ԫ��ԭ�Ӻ�����5�����Ӳ�
C.��Ԫ��ԭ������㹲��3������
D.��Ԫ��ԭ��M�ܲ㹲��8������
�ο��𰸣�B
���������
�����Ѷȣ���
2��ѡ���� X��Y��Z���ֶ�����Ԫ�أ�XԪ�ص�ԭ�������ֻ��һ�����ӣ�YԪ�ص�ԭ��M���Ӳ�ĵ�����ΪK��L�ϵ���������һ�룬ZԪ�ص�ԭ��L���������Yԭ��L���������2������������Ԫ����ɵĻ�����Ļ�ѧʽ�����ǣ�������
A��X3YZ4
B��X2YZ3
C��XYZ2
D��X2YZ4
�ο��𰸣�AC
���������
�����Ѷȣ�һ��
3��ѡ���� �����ƺ��⻯�ƶ������ӻ������ˮ��Ӧ�Ļ�ѧ����ʽ(δ��ƽ)���£�Na3N+H2O��NaOH+NH3��
NaH+H2O��NaOH+H2���й����ǵ����������Ӱ뾶Na+>N3->H+������ˮ��Ӧ����������ԭ��Ӧ������ˮ��Ӧ�����Һ���Լ��ԣ��������ᷴӦ��ֻ����һ���Σ������ֻ������е��������Ӿ�������ͬ�ĵ��Ӳ�ṹ��������ȷ����
[? ]
A���ڢۢܢ�
B���٢ۢ�
C���ڢ�
D����
�ο��𰸣�D
���������
�����Ѷȣ�һ��
4������� �������߷ֱ��ʾԪ�ص�ij��������˵�����Ĺ�ϵ��XΪ�˵������YΪԪ�ص��й����ʣ�����������Ԫ���йص�������������߱��������Ӧ�ĺ����У�
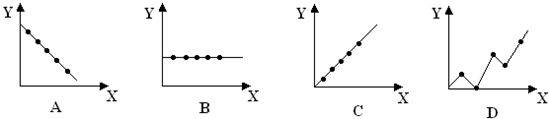
��1����VIA��Ԫ�ص�������������______
��2����������Ԫ�ص�����ϼ���______
��3��O2-��F-��Na+��Mg2+��AL3+�����Ӱ뾶��______��
�ο��𰸣���1����ͬһ����Ԫ�ص�������������ȣ��ʴ�Ϊ��B��
��2����Ԫ�ص��������=����������=��������ͬһ����Ԫ�ص�����ϼ������ʴ�Ϊ��C��
��3�������������ͬ�������������Խ��뾶ԽС���������Ӱ뾶Ϊ��O2-��F-��Na+��Mg2+��Al3+���ʴ�Ϊ��A��
���������
�����Ѷȣ�һ��
5������� ��֪A��B��C��D��E��F��G��H��ԭ��������������İ���Ԫ�أ�AԪ�������ڱ���ԭ�Ӱ뾶��С��Ԫ�أ�B��C��Dͬ���ڣ�E��F��Gͬ���ڣ�A��E?ͬ���壬D��G��Hͬ���������ڣ�B�ĵͼ���������C���ʷ��ӵĵ���������ȣ�F��G�ĺ˵�������4��G��2�ۼ�������Arԭ�ӵĵ��Ӳ�ṹ��ͬ������������Ϣ��գ�
��1��GԪ�صĶ������ӵ����ӽṹʾ��ͼΪ______��H��Ԫ�ط���Ϊ______��HԪ�������ڱ��е�λ����______��
��2��C����̬�⻯��ռ乹����______��A��B�γɵ���ԭ�ӷǼ��Է��ӵĽṹʽ��______��
��3���ݱ���������������Ԫ��B��F��Ni����Ԫ�صľ�����г����ԣ��þ���ľ����ṹ��ͼ����д���þ���Ļ�ѧʽ______

��4����A��C��D��G����Ԫ���γɵ�ǿ�����ʽ�ε�ˮ��Һ�и�����Ũ���ɴ�С��˳��Ϊ______��
��5����ѧ����C��D��E����Ԫ���γɵĻ�����ECD3��E2D����573Kʱ��Ӧ�Ƶ������ӻ�����E3CD4�����ⶨE3CD4�и�ԭ�ӵ��������Ӷ��ﵽ��8�����ȶ��ṹ����CD43-�ĵ���ʽΪ______��E3CD4��ˮ�ܾ��ҷ�Ӧת��Ϊ�������ʣ�д����Ӧ�Ļ�ѧ����ʽ��______��
�ο��𰸣�AԪ�������ڱ���ԭ�Ӱ뾶��С��Ԫ�أ���AΪH��G��2�ۼ�������Arԭ�ӵĵ��Ӳ�ṹ��ͬ��D��G��Hͬ���������ڣ���GΪS��DΪO��HΪSe��A��E?ͬ���壬��EΪNa��B�ĵͼ���������C���ʷ��ӵĵ���������ȣ���CΪN��BΪC��F��G�ĺ˵�������4����FΪMg��
��1�������ӽṹʾ��ͼΪ
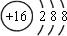
��H��Ԫ�ط���Ϊ Se��λ�ڵ������ڵڢ�A�壬�ʴ�Ϊ��
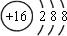
��Se���������ڵڢ�A�壻
��2�������Ŀռ�ṹΪ�����Σ�̼�����γɵ���ԭ�ӷǼ��Է��Ӽ�Ϊ��Ȳ���ṹʽ�ǣ�H-C��C-H���ʴ�Ϊ�������Σ�H-C��C-H��
��3�����ݾ���ľ����ṹ��ÿ����������һ��Mg������Ni����Ϊ��6��12=3������C����Ϊ��8��18=1���ʸþ���Ļ�ѧʽΪ��MgCNi3���ʴ�Ϊ��MgCNi3��
��4�������������������ˮ���Σ�NH4HSO4�TNH4++H++SO42-��笠�������ˮ�⣬��Һ�е������ӻ���ˮ�����һС���֣�������Ũ�ȴ�С˳��Ϊ��c��H+����c��SO42-����c��NH4+����c��OH-�����ʴ�Ϊ��c��H+����c��SO42-����c��NH4+����c��OH-����
��5��NO43-�еĻ�ѧ��ȫ��Ϊ���ۼ���Na3NO4��ˮ��Ӧʱ��ת��Ϊ�������ʣ�����ԭ���غ㣬�õ�����ʽΪ��Na3NO4+H2O�TNaNO3+2NaOH���ʴ�Ϊ��
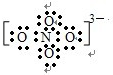
��Na3NO4+H2O�TNaNO3+2NaOH��
���������
�����Ѷȣ�һ��